TÜRKİYE CUMHURİYETİ
ANKARA ÜNİVERSİTESİ
TIP FAKÜLTESİ
OVERİN SERÖZ ADENOKARSİNOMLARI VE SERÖZ
BORDERLİNE TÜMÖRLERİNDE RAS/RAF/MEK/MAPK
YOLAĞINDAKİ MOLEKÜLER DEĞİŞİKLİKLERİN
İMMÜNHİSTOKİMYASAL OLARAK ARAŞTIRILMASI
Dr. Cevriye CANSIZ
PATOLOJİ ANABİLİM DALI
TIPTA UZMANLIK TEZİ
DANIŞMAN
Prof. Dr. Ayşe SERTÇELİK
“Bu tez, Ankara Üniversitesi Rektörlüğü Araştırma Fonu tarafından,
20070809039HPD Proje numarası ile desteklenmiştir.”
ANKARA
2008
i
ÖNSÖZ
Başta tez danışmanım Prof. Dr. Ayşe Sertçelik, immünhistokimyasal boyanma
aşamasındaki destekleri için Prof. Dr. Işınsu Kuzu olmak üzere tez çalışmam esnasındaki bilgi
ve manevi destekleri ve Patoloji Anabilim Dalı’nda asistan eğitimim boyunca eğitimime
katkıları için tüm değerli hocalarıma, tezimin hemen tüm aşamalarında desteği ve emeği olan
Uzm. Dr. Gülşah Kaygusuz, Uzm. Dr. Ebru Erol’a, manevi destekleri için tüm uzman ve
asistan arkadaşlarıma teşekkür ederim.
Ayrıca çalışmamın hazırlık aşamasındaki yardımlarından ötürü Alahattin Alptekin ve
Dilek Şanver’e, immünhistokimyasal kesitlerin hazırlanması ve boyaların yapılma aşamasında
her türlü desteği ve emeği için İmmünpatoloji laboratuarı çalışanlarına ve çalışmamın
istatistiksel değerlendirmesinin yapılmasında emeği geçen Zeynep Bıyıklı’ya teşekkür ederim.
Tez çalışmam süresince manevi desteklerini hiçbir zaman esirgemeyen, her zaman
yanımda olan aileme teşekkür ederim.
Dr. Cevriye CANSIZ
ii
İÇİNDEKİLER
Sayfa No
KABUL VE ONAY…………………………………………………………………………..i
ÖNSÖZ…………………………………………………………………….............................ii
İÇİNDEKİLER……………………………………………………………………………...iii
SİMGELER VE KISALTMALAR………………………………………………………..vii
1. GİRİŞ ve AMAÇ…………………………………………………………………………..1
2. GENEL BİLGİLER……………………………………………………………………….3
2.1. Overin Anatomi, Embriyoloji ve Histolojisi……………………………………...3
2.2. Over Tümörlerinde WHO Klasifikasyonu………………………………………..5
2.3. Epidemiyoloji……………………………………………………………………..7
2.4. Etyoloji ve patogenez…………………………………………………………….8
2.4.1. Yaş ve Genetik Faktörler…………………………………………….....8
2.4.2. Reprodüktif Faktörler; Risk Faktörleri, Koruyucu Faktörler…………..8
2.4.3. Patogenez……………………………………………………………….9
iii
2.5. Yüzey Epiteli Kökenli Over Tümörleri …………………………………………11
2.5.1. Müsinöz Tümörler……………………………………………………..11
2.5.2. Endometrioid Tümörler………………………………………………..12
2.5.3. Şeffaf Hücreli Tümörler……………………………………………….12
2.5.4. Brenner Tümörü……………………………………………………….12
2.5.5. Adenosarkom ve Malign Mikst Müllerian Tümör…………………….13
2.6. Seröz Tümörler……………………………….…………………………………13
2.6.1. Benign seröz tümörler…………………………………………………13
2.6.2. Borderline Seröz Tümörler……………………………………………14
2.6.2.1. Mikropapiller Varyant……………………………………….17
2.6.3. Seröz Adenokarsinomlar………………………………………………18
2.7. Klinik Bulgular, Prognoz, Evreleme ve Tedavi Yaklaşımları…………………..19
2.8. RAS/ RAF/ MEK / MAPK Yolağı ve Tez Çalışmasında Kullanılan
İmmünhistokimyasal Belirteçler……………………………………………….22
3. MATERYAL ve METOD………………………………………………………………28
3.1.Olgu Seçimi ve Doku Mikro&Makroarray (TMA) Bloklarının Hazırlanması…28
3.2.Klinik ve Histopatolojik İnceleme………………………………………………29
iv
3.3.İmmünhistokimyasal İnceleme…………………………………………………29
3.3.1. Kullanılan Antikorların özellikleri…………………………………29
3.3.2. İmmünhistokimyasal Boyama……………………………………...30
3.3.3. İmmünhistokimyasal Boyanmaların Değerlendirilmesi……………30
3.3.3.1.İmmünhistokimyasal Markerların Boyanma Şekilleri……..30
3.3.3.2. İmmünhistokimyasal Markerların Boyanma Skorları……..30
3.4.Bloklarında Doku Silindirlerinin Değerlendirilmesi…………………………...31
3.5.İstatistiksek Değerlendirme…………………………………………………….31
4. BULGULAR…………………………………………………………………………....31
4.1. Klinik Bulgular………………………………………………………………...31
4.2. Histopatolojik Bulgular………………………………………………………..32
4.3. İmmünhistokimyasal Bulgular………………………………………………...32
4.3.1. İmmünhistokimyasal Markerların Sonuçları………………………………...32
4.3.1.1. c-Fos……………………………………………………………….32
4.3.1.2: c-Myc………………………………………………………………34
4.3.1.3. c-Jun………………………………………………………………..36
v
4.3.1.4. p38…………………………………………………………................38
5. TARTIŞMA……………………………………………………………………………….46
6. SONUÇLAR………………………………………………………………………………54
7. ÖZET……………………………………………………………………………………...55
8. SUMMARY……………………………………………………………………………….57
9. KAYNAKLAR…………………………………………………………………………....59
vi
SİMGELER VE KISALTMALAR DİZİNİ
TMA
: Doku Mikroarray
ERK
: Ekstrasellüler sinyal regülasyon protein kinaz
MAPK
: Mitojen-aktive protein kinaz
IHK
: İmmmünhistokimya
H.E
: Hematoksilen Eozin
SAK
: Seröz Adenokarsinom
SBT
: Seröz Borderline Tümör
MPSC
: Mikropapiller Seröz Karsinom
FIGO
: Jinekoloji ve Obstetrik İnternasyonel Federasyonu
Vii
1. GİRİŞ VE AMAÇ:
Over kanserleri kadınlarda en ölümcül tümörlerden biri olup, dünyada her yıl
yaklaşık 205.000 yeni olgu tanımlanmaktadır (1). Jinekolojik malignitelerin %30’unu
oluşturan over kanserleri jinekolojik maligniteler nedeniyle ölümlerin ise en sık
nedenidir. Gelişmiş ülkelerde korpus uteri (%35) ve invaziv serviks kanseri (%27) kadar
sık rastlanmaktadır (2).
Over tümör patogenezinde son yıllarda iki iki farklı yolaktan söz edilmekte ve bu
modelde yüzey epiteli kökenli over tümörleri iki ana kategoriye ayrılmaktadır. Tip I ve
Tip II olarak ayrılan bu tümörler patogenezde iki farklı yolaktan gelişmektedir. Tip I
tümörler düşük dereceli tümörlerdir ve bunların borderline tümörlerden geliştikleri
düşünülmektedir. Tip II tümörler ise yüksek dereceli tümörlere karşılık gelmektedir ki
bu tümörlerin tanımlanabilir bir prekürsör lezyonları bulunamamıştır. Seröz tümörler,
overin en sık izlenen epitelyal tümörleri oldukları için düşük dereceli seröz karsinomlar
tip I tümörlerin prototipini oluştururlar. Yüksek dereceli seröz karsinomlar da tip II
tümörlerin prototipidir. Düşük dereceli seröz karsinomlar yanı sıra müsinöz karsinomlar,
endometrioid karsinomlar, malign Brenner tümörleri ve Clear hücreli karsinomlar da tip
I tümörleri oluşturmaktadırlar. Farklı epitel türlerinden oluşan bu tümörler de kendi
içlerinde benign, borderline ve malign olmak üzere, davranışlarını belirleyebilmek için
ayrılmıştır. Müsinöz ve endometrioid borderline tümörler çoğu kez invaziv
karsinomlarla birliktelik gösterirlerken, seröz borderline tümörlerde böyle bir durum
gözlenmemektedir. Bu nedenle seröz borderline ve seröz karsinomaların ilişkisiz
oldukları düşünülmüştür (5).
Tip I tümörlerde tip II tümörlerde izlenmeyen ayrı genetik değişiklikler
bildirilmektedir. Bunlar seröz karsinomlarda BRAF ve KRAS mutasyonları, müsinöz
karsinomlardaki KRAS mutasyonu, endometriod tümörler için ise β-catenin, PTEN ve
mikrosatellit instabilitesidir. Tip II tümörler ise yüksek gradeli seröz karsinomlar yanı
sıra malign mikst mezodermal tümör (karsinosarkom) ve undiferansiye karsinomlar yer
almaktadır. Tip II tümörlerde moleküler değişiklikler konusunda sınırlı bilgi bulunmakla
birlikte p53 mutasyonu seröz karsinomlarda ve karsinosarkomlarda sık izlenirler (5).
BRAF veya KRAS mutasyonu hedef molekülü olan Mitogen-activated protein
kinase (MAPK)’ın fosfolilasyonuna yani aktivasyonuna neden olur. Ekstrasellüler sinyal
regülasyon protein kinaz (ERK) olarak da bilinen Mitojen-aktive protein kinaz (MAPK);
değişen ekstrasellüler uyarılar ile kompleks bağlantılar eşliğinde çeşitli kinaz
substratlarını aktive eden dört kinaz komponenti mevcuttur. MAP kinaz aktivasyonu
AP-1, p53, Elk-1, Ets-1, c-Myc ve STAT gibi çeşitli sitozolik substratların
fosforilasyonu ve nükleusa translokasyonu ile sonuçlanır (4). Net sonuç hücrelerde
büyüme, diferansiasyon ve proliferasyondur.
Bu çalışmada overin yüzey epiteli kökenli seröz adenokarsinomları, seröz
borderline tümörleri ve benign lezyonlarında RAS/RAF/MEK/MAPK yolağındaki
değişikliklerin immünhistokimyasal olarak gösterilmesi amaçlanmıştır. Bu amaç
doğrultusunda RAS/RAF/MEK/MAPK yolağında değişik
basamaklarda olduğu
bildirilen moleküller; MAP Kinaz (p38), c-fos, c-jun ve c-myc araştırılmıştır. Tümörlü
bloklardan elde edilen kesitlerde immünhistokimyasal olarak nükleer ve sitoplazmik
boyanmaları arasındaki fark değerlendirilmiştir.
2. GENEL BİLGİLER:
2.1. OVERİN ANATOMİ, HİSTOLOJİ ve EMBRİYOLOJİSİ:
Overler, oval, 5-8 gr ağırlığında, pelviste tubanın üst kısmında, ligamentum
latumun yaprakları arasında ve rektumun ön tarafında sağda ve solda yer alırlar.
Overlerin; ön ve arka iki yüzü, alt ve üst iki kenarı ve lateral iki ucu vardır. Overin
arterleri aorta abdominalisten gelir. Venleri hilusta toplanır ve utero-ovarian venlere
dökülür. Lenfatikleri venleri izler ve lumbal lenf düğümlerine dökülür.
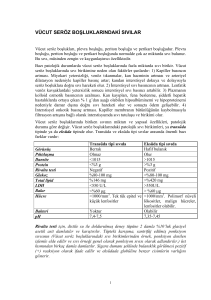
Over çölom epiteli ile örtülüdür. Korteks ve medulla olmak üzere iki kısımdan
ibarettir. Korteks fusiform bağ dokusu hücrelerinden yapılmıştır. Bu hücreler girdap
yapacak şekilde dizilmişlerdir. Stroma içerisinde değişik olgunlaşma evrelerinde
folliküller yer alır. Medulla gevşek bağ dokusundan yapılmıştır. Damarları, lenfatikleri,
sinirleri, hilus hücrelerini ve embriyoner artıkları içerir.
Şekil 2.1. H.Ex10 kesitte overin histolojisi
Gonadlar üç yerden köken alarak gelişirler:
1.
Posterior karın duvarını döşeyen çölom epiteli (mesothelium)
2.
Çölom epiteli altındaki mezanşim
3.
İlkel cinsiyet hücreleri (primordial germ hücreleri)
Gonad gelişmesi ilk olarak gelişimin 5. haftasında, mezonefrozun medialinde,
sağ ve solda, sölom epitelinin çoğalması ve altındaki mezenşimin yoğunlaşmasıyla
oluşan, uzunluğuna iki adet gonadal yada genital kabartıyla dikkati çeker. Gelişmenin 4.
haftasında, büyük yuvarlak ilkel cinsiyet hücreleri, allantois kesesine yakın vitellüs
kesesi endoderm hücreleri arasında görülmeye başlarlar. Embriyonun
kıvrılması
sırasında, vitellüs kesesinin dorsal kısmı embriyon içine alınır. Bu katılma olurken, ilkel
cins hücreleri, son bağırsağın dorsal mezenteri yoluyla 6. haftada ameboid hareketlerle
gonad kabartılarına göç ederler.
Erken fötal dönemde, kortikal kordonlar denilen ikinci cinsiyet kordonları,
gelişmekte olan gonadın yüzey sölom epitelinden başlayarak, altındaki mezanşime
doğru gelişmeye başlar. Sölom epitelinin çoğalmasıyla kortikal kordonlar kalınlaşırken,
ilkel cinsiyet hücreleri kordonlar içine karışırlar. Yaklaşık 16. haftada bu kordonlar,
primordial follikül denilen ayrı hücre gruplarına bölünürler. Her bir grup, ortada ilkel
cinsiyet hücrelerinden köken almış oogonyum ve onun çevresinde, kortikal kordon
sölom epiteli kökenli tek sıra follikül hücrelerinden meydana gelir. Fötal dönemde
milyonlarca oogonyum aktif mitozla oluşurlar. Doğum öncesi, oogonyumların bir kısmı
dejenere olurken, büyük bir kısmı büyüyerek primer oositleri yaparlar.
2.2. OVER TÜMÖRLERİNDE WHO KLASİFİKASYONU
OVER TÜMÖRLERİ (1993 WHO Klasifikasyonu)
YÜZEY EPİTELİ-STROMAL TÜMÖRLER
Seröz Tümörler
Benign (kistadenoma)
Borderline seröz tümör
Malign (seröz kistadenokarsinoma)
Müsinöz Tümörler, endoservikal benzeri ve intestinal tip
Benign
Borderline
Malign
Endometrioid Tümörler
Benign
Borderline
Malign
Epitelyal-stromal
Adenosarkoma
Mezodermal (müllerian) mikst tümör
Clear hücreli
Benign
Borderline
Malign
Transizyonel Hücreli
Brenner tümör
Borderline brenner tip
Malign brenner tip
Transizyonel hücreli karsinoma (non-brenner tip)
SEKS KORD STROMAL TÜMÖRLER
GRANULOZA-STROMAL HÜCRELİ TÜMÖRLER
Granuloza hücreli tümör grubu
Erişkin
Juvenil
Tekoma
Fibroma
Sellüler fibroma
Fibrosarkoma
Minor seks kord elemanlar içeren stromal tümörler
Sklerozan stromal tümör
Taşlı yüzük- stromal tümör
Sınıflandırılamayan (fibrotekoma)
SERTOLİ STROMAL HÜCRELİ TÜMÖRLER:
Sertoli- Leydig hücreli tümör grubu (Andrablastoma)
İyi diff
Orta diff
Heterolog eleman içeren varyant
Az diff
Heterolog eleman içeren varyant
Retiform
Heterolog eleman içeren varyant
Sertoli hücreli tümör
Stromal-Leydig hücreli tümör
MİKST VEYA SINIFLANDIRILAMAYAN HÜCRE TİPLERİ İÇEREN SEKS KORD
STROMAL TÜMÖRLER:
Annuler tubuller içeren seks kord stromal tümörler
Gynandroblastoma
Sınıflandırılamayan SCST
STEROİD HÜCRELİ TÜMÖRLER:
Stromal Luteoma
Leydig hücreli tümör grubu
Hilus hücreli tümör
Leydig hücreli tümör, non-hiler tip
Leydig hücreli tümör, NOS
Steroid hücreli tümör, NOS
İyi diferansiye
Malign
GERM HÜCRELİ TÜMÖRLER
Primitif germ hücreli tümörler
Disgerminom
Yolk Sac tümör
Embriyonel Karsinom
Poliembriyoma
Non-gestasyonel Koryokarsinom
Mikst Germ Hücreli Tümör
Bifazik-Trifazik Teratom
İmmatür Teratom
Matür Teratom
Monodermal Teratom ve Dermoid Kist asosiye Somatik Tip Tümörler
Germ hücreli Seks Kord-Stromal Tümörler
SINIFLANDIRILAMAYAN TÜMÖRLER
SEKONDER TÜMÖRLER
2.3. EPİDEMİYOLOJİ:
Dünya çapında over karsinomları kadınlarda, altıncı en sık tümördür Düşük
doğum oranının bulunduğu endüstriel ülkelerde daha sık gözlenmektedir. Yıllık oran
Brezilya, Tayland, Hindistan ve Cezayir gibi ülkelerde 100.000’de 5’in altında
bildirilirken, İngiltere, Amerika, Almanya, Norveç, Danimarka ve İsveç gibi ülkelerde
ise 100.000’de 13’ün üzerinde izlenmektedir (1). Jinekolojik malignitelerin %30’unu
oluşturmaktadır. Jinekolojik maligniteler nedeniyle ölümlerin ise en sık nedenidir.
Gelişmiş ülkelerde korpus uteri (%35) ve invaziv serviks kanseri (%27) kadar sık
rastlanmaktadır (2).
Türkiye'de ilk nüfus tabanlı kanser kayıt sistemi 1992'de İzmir'de kurulmuş ve
1993-1994 yıllarına ait insidans verileri 2001'de yayınlanmıştır. Kadınlarda over kanseri
yüzbinde 5.9 görülme sıklığı ile en sık görülen 3. kanser olmuştur (11).
2.4. ETYOLOJİ ve PATOGENEZ:
2.4.1. Yaş ve Genetik Faktörler:
Over tümörleri görülme sıklığı yaş ile artar. Amerika’da 30 yaş altında
100.000’de 3 oranında izlenirken, 75 yaş ve üzerinde 100.000’de 54 oranına
yükselmektedir. Over kanserlerinin izlendiği ortalama yaş grubu ise 60’dır.
Over kanserlerinin yaklaşık 10%’unde genetik geçiş mevcuttur ve bunların
90%’ında BRCA1 ve BRCA2 mutasyonlar gözlenmektedir. BRCA1 ve BRCA2, DNA
hatalarının iletiminde, DNA tamirinin aktivasyonunda, apopitozisin indüksiyonunda ve
hücre siklus kontrol noktalarında önemli görevlere sahiptir (12). Herediter over
karsinomlarının yaklaşık 10%’u, DNA tamir mekanizmalarının bozulduğu, Lynch
sendromu veya herediter non-polipozis kolon kanseri sendromlarında izlenmektedir. Bu
sendromlara
sahip
hastaların
over
karsinomu
geliştirme
riski
12%
olarak
bildirilmektedir (13). Diğer familyal sendromlar ise Peutz-Jeghers Sendromu (STK 11
geni mutasyonu, 21% risk) ve Gorlin Sendromudur (PTCH mutasyonu, 20% risk).
2.4.2. Reprodüktif Faktörler; Risk Faktörleri ve Koruyucu Faktörler:
Yüksek doğum sayısı, doğum kontrol hapı kullanımı, artmış emzirme süresi
özellikle müsinöz olmayan over tümörlerinde koruyucu faktörler olduğu saptanmıştır.
Erken menarş, geç menapoz ve yüksek sosyoekonomik düzeyin artmış over karsinom
riski ile ilişkili olduğunu bildiren çalışmalar mevcuttur. Ovulasyonun over yüzey
epitelini travmatize ettiği, proliferasyonu stimüle ettiği ve aktif prolifere epitelde malign
transformasyonun görülebileceği öne sürülmektedir. Bunlar dışında ilk çocuğu doğurma
yaşı, hormon replasman tedavisi, emzirme öyküsü, kilo, diyet, talk, sigara kullanımı,
çocukluk çağında geçirilmiş belirli viral enfeksiyonların varlığı ve iyonize radyasyon
gibi daha bir çok faktör ile ilişkili olduğu düşünülmektedir (14, 17-18).
İnfertilite tedavisine bağlı olarak da epitelyal over karsinomu riskinin 2,8 kat ve
borderline tümör riskinin ise 4,0 kat arttığı savunulmaktadır (14). Ancak yapılan bir
vaka kontrol çalışmasında gonadotropin kullanımı ile epitelyal over karsinomu gelişimi
arasında ilişki bulunamamış, infertilitenin, infertilite ilaçları kullanımından daha önemli
bir risk faktörü olduğu savunulmuştur (15-16). Gonadotropinlerin kanser gelişimine
neden olmak yerine progresyonunda etkili olduğu savunulmaktadır.
2.4.3. Patogenez:
Primer over tümörleri 3 ana kategoride incelenmektedir:
1. Epitelyal tümörler (yüzey epiteli, epitelyal inklüzyonlar veya endometriozis
odaklarından)
2. Seks cord stromal tümörler (ovaryan stromadan, seks kord türevlerinden)
3. Germ hücreli tümörler (germ hücrelerinden)
Bunlar dışında yumuşak doku tümörleri, lenfomalar da overde gelişebilir.
Ekstraovaryan primer tümörlerin metastazı da izlenebilir.
Over yüzey epiteli kökenli tümörleri histolojik alt tiplere ayrılmaktadır. Her bir
hücre tipine göre farklı etyopatogenez mevcuttur. Ovaryan tümörogenezde son yıllarda
iki iki farklı yolaktan söz edilmekte ve bu modelde yüzey epiteli kökenli over tümörleri
iki ana kategoriye ayrılmaktadır. Tip I ve Tip II olarak ayrılan bu tümörler tümör
patogenezinde iki farklı yolağa uymaktadır. Tip I tümörler düşük gredeli tümörlerdir ve
bunların borderline tümörlerden geliştikleri düşünülmektedir. Tip II tümörler ise yüksek
gradeli tümörlere karşılık gelmektedir ki bu tümörlerin tanımlanabilir bir prekürsör
lezyonları bulunamamıştır. Düşük gradeli seröz karsinomlar yanı sıra müsinöz
karsinomlar, endometrioid karsinomlar, malign Brenner tümörleri ve Clear hücreli
karsinomlar da tip I tümörleri oluşturmaktadırlar. Farklı epitel türlerinden oluşan bu
tümörler de kendi içlerinde benign, borderline ve malign olmak üzere davranışlarını
belirleyebilmek için ayrılmıştır. Müsinöz ve endometrioid borderline tümörler çoğu kez
invaziv karsinomlarla birliktelik gösterirlerken seröz borderline tümörlerde böyle bir
durum gözlenmemektedir (5). Tip I tümörlerde tip II tümörlerdekinden ayrı genetik
değişiklikler bildirilmektedir (Tablo 2.4.1). Tip II tümörler yüksek dereceli seröz
karsinomlar malign mikst mezodermal tümör (karsinosarkom) ve undiferansiye
karsinomlardır. Tip II tümörlerde moleküler değişiklikler konusunda sınırlı bilgi
bulunmaktadır (Tablo 2.4.1).
Tip I tümör
Prekürsör
Düşk gradeli SAK
Seröz Kistadenoma
Moleküler genetik değişiklik
BRAF/KRAS mutasyonu(~67%)
Adenofibroma
Atipik proliferatif seröz tümör
Müsinöz karsinom
Müsinöz kistadenom
KRAS mutasyonu (>60%)
Atipik proliferatif müsinöz tm
İntraepitelyal karsinom
Endometrioid k.
Endometriozis
Endometiroid adenofibrom
LOH / PTEN mutasyonu(20%)
β-catenin mutasyonu(16-54%)
Atipik proliferatif endmetrioid tm
KRAS mutasyonu(4-5%)
İntraepitelyal karsinom
MI(13-50%)
Clear cell karsinom Endometriozis
KRAS mutasyonu(5-16%)
Clear cell adenofibrom
MI(~13%)
Atipik proliferatif clear hcli tm
TGF-β R II (66%)
İntraepitelyal karsinom
Malign Brenner tm
Brenner tümör
Tanımlanmamış
Atipik proliferatif Brenner tm
Tablo 2.4.1. Tip I over tümörlerinde moleküler genetik değişiklikler ve prekürsör
lezyonlar
Müsinöz karsinomlarda K-RAS mutasyonu varlığı benign, borderline ve malign
formlarında bilinmekte ve bu tümörlerin progresyonunda etkisi olduğu düşünülmektedir.
Ancak seröz karsinomlardaki spektrumda moleküler olarak ayrı oldukları ve benign
lezyonlardan karsinoma progresyonu öne sürülememektedir. Ancak seröz karsinomların
spesifik düşük gradeli formu olan mikropapiller seröz karsinomlarda borderline
tümörleri ile ilişkili olabileceğini gösteren kanıtlar bulunmaktadır. Mikropapiler seröz
karsinomların 90%’ı borderline tümör alanları içermektedir.
Tip II tümör
Prekürsör
Yüksek gradeli SAK
Tanımlanmamış
Moleküler genetik değişiklik
p53 mutasyonu (50-80%)
HER2/neu(10-20%) amplif.
AKT2(12-18%) amplif.
p16 inaktivasyonu(10-17%)
Undiferansiye karsinom
Malign Mikst Mezodermal
Tanımlanmamış
Tanımlanmamış
Tanımlanmamış
p53 mutasyonu(>90%)
Tümör (karsinosarkom)
Tablo 2.4.2. Tip II over tümörlerinde moleküler genetik değişiklikler ve prekürsör
lezyonlar
2.5. YÜZEY EPİTELİ KÖKENLİ OVER TÜMÖRLERİ
Yüzey epiteli kökenli diğer over tümörlerinin histopatolojik özelliklerine kısaca
değinilecek, seröz tümörleri ayrı bir başlık altında anlatılacaktır.
2.5.1. Müsinöz Tümörler:
Tüm over tümörlerinin 25%’ini oluştururlar. 30-40 yaşlarda daha sık izlenirler.
Müsinöz tümörlerin 80%’i benign veya borderline olarak izlenirken, 15%’i maligndir.
Overin borderline neoplazilerinin 30-50%’si ve over karsinomlarının 6-10%’u müsinöz
tiptir. Benign olanların 5% kadarı ve malignlerin ise 10% kadarı bilateraldir. Müsinöz
tümörlerde benign-borderline-malign gelişim sırası izlenir. KRAS düzeyi benignden
maligne doğru artış gösterir. Benign olanları overin en büyük tümörleridir. Kist içeriği
müsinöz karakterdedir. Papillomatöz gelişimler daha nadir görülür. Serozal penetrasyon
ve solid alanların varlığı maligniteyi düşündürür. Mikroskopik olarak kistik yapıları
döşeyen epitelin apikal yüzlerinde sekresyon vakuolleri izlenen, silyasız, yüksek
prizmatik epitel hücrelerinden oluştuğu gözlenir.
Endoservikal epitele benzeyenler endoservikal-benzeri (müllerian) ve kolon epiteline
benzeyenler ise intestinal tip olarak müsinöz borderline tümörler ikiye ayrılmaktadır.
85% oranında intestinal tip, 15% oranında endoservikal tip izlenir.
2.5.2. Endometrioid Tümörler:
Tüm over karsinomlarının 20% kadarını oluşturmaktadır. Solid veya kistik
olabilirler. Tümörü olan hastaların 15%’inde eş zamanlı endometriozis bulunur.
Genellikle kötü seyirlidir. Yaklaşık 30%’u çift taraflıdır. Tümörlü hastaların 1530%’unda eş zamanlı endometrium karsinomu bulunmaktadır. Mikroskopik olarak
endometriumda görülenlere benzer tübüler gland yapıları ve kribriform alanlar gözlenir.
Hafif veya orta derecede atipi gösteren yüksek kolumnar epitel ile döşelidirler.
Skuamoid diferansiasyon izlenebilir. Tüm tümörlerinde 5 yıllık sağ kalım 40-50%
arasındadır. Borderline tipi nadir görülmektedir.
2.5.3. Şeffaf Hücreli Tümörler:
Geniş şeffaf epitel hücreleri ile karakterlidirler. Solid, papiller veya tübülokistik
paternde izlenebilirler. Dens hyalinize eozinofilik bir stroma gözlenir, poligonal, şeffaf
veya eozinofilik sitoplazmalı hücrelerden oluşurlar. Daha çok solid özelliktedir. Kistik
olarak da izlenebilir. Solid tümörlerde hücreler adalar veya tübüller yaparlar. Kistik
olanlarda ise kistin iç yüzeyini döşerler. Genellikle kötü gidişlidirler. 5 yıllık sağ kalım
50% kadardır. Benign ve borderline tipleri nadirdir.
2.5.4. Brenner Tümörü:
Nadir rastlanan, solid, genellikle iyi seyirli, üriner sistem değişici epiteline
benzer epitel adaları içeren stromadan zengin bir tümördür. Transizyonel hücreli
karsinomlar kalın fibrovasküler kor içeren papillalar ve bu papillaları döşeyen stratifiye
epitelden oluşurlar. Nükleer atipi genellikle belirgindir. Genellikle düzgün yüzeyli ve
kapsüllüdürler. 90%’ı tek taraflıdır. Kesit yüzleri gri beyaz renktedir. Solid veya kistik
olabilirler. Fibröz stroma normal overdekine benzer ancak nadir olmayarak teka
hücrelerine benzeyen şişkin fibroblastlar içerebilirler. Böyle tümörler hormonal aktivite
gösterebilirler. Yüzey epiteli kaynaklı olabilecekleri gibi embriyogenez sırasında
germinal çıkıntı içinde sıkışan ürogenital epitelden de kaynaklanabilecekleri ileri
sürülmüştür. Borderline (proliferatif Brenner tümörü) ve malign tipleri mevcuttur. Evre
Ia tümörlerde 5 yıllık sağ kalım 88% oranlarında belirtilmektedir.
2.5.5. Adenosarkom ve Malign Mikst Müllerian Tümör:
Müllarian adenosarkom; bifazik karakterdeki bu tümörde epitelyal elemanlar
benign, stromal elemanlar ise malign karakterdedir. Malign Mikst Müllerian Tümör;
hem epitelyal, hem de stromal malign hücrelerden oluşur. Homolog tipte stroma malign
fibroblastlara benzeyen iğsi hücrelerden oluşur. Heterolog tipte ise stromada sarkomatöz
alanlar içinde kondrosarkom,
osteosarkom, rabdomyosarkom ve anjiosarkoma
benzeyen alanlar vardır. Her iki tipte de karsinomatöz alanlar seröz, endometrioid,
skuamöz ve şeffaf hücreli epitel izlenir. Genellikle postmenapozal dönemde izlenen bu
tümörlerin prognozları kötüdür (19).
2.6. SERÖZ TÜMÖRLER:
Yüksek kolumnar epitel ile döşeli bu kistik tümörler overin en sık görülen
tümörleridir (65-70%). Çoğu kistik yapıdadır. 60% kadarı benign, 15%’i borderline,
25%’i maligndir. Borderlien seröz tümörler (SBT) ve Seröz adenokarsinomlar (SAK)
tüm over malign tümörlerinin 40%’ nı oluşturmaktadır. Benign ve SBT’ ler 20-50 yaşlar
arasında izlenirken, SAK’ lar daha geç yaşta gözlenirler.
2.6.1: Benign seröz tümörler:
Seröz kistadenomlar; uniloküler veya multiloküler olabilirler. İnce bir duvara
sahip ve berrak bir sıvı içerirler. İç ve dış yüzeyleri genellikle düz olarak izlenir. Ancak
küçük papiller çıkıntılar izlenebilir. Seröz adenofibrom ise solid bir tümördür. Kirli
beyaz kesit yüzüne sahiptir. Küçük kistler izlenebilir ve böylelikle süngerimsi bir kesit
yüzüne
sahip
olabilirler.
kistadenofibromlar
Seröz kistadenofibrom olarak
adenofibromlardan
daha
sık
adlandırılırlar.
karşımıza
çıkarlar.
Seröz
Seröz
kistadenofibromlar uniloküler veya multiloküler olarak izlenirler. Duvarlarında solid
adenofibromatöz alanlar izlenir. Seröz yüzey papilloması ise ender görülen bir
tümördür. Yüzeyde küçük papiller çıkıntılar halinde izlenir.
Benign tümörlerin 20%’si bilateraldir. Mikroskopik olarak benign tümörler silyalı
veya silyasız kısa kolumnar hücrelerle döşelidir. Epitel basıklaşmış olabilir. Glandların
çevresinde fibröz stroma izlenir. Yapılan bir çalışmada seröz kistadenomların yalnızca
14%’ünde monoklonalite saptanmıştır (20).
Küçük foküsler halinde hafif veya orta derecede nükleer atipi veya papiller yapılar
izlenebilmektedir. Bu şekilde küçük odaklar halinde borderline benzeri görünüme sahip
tümörlerin davranışı ile ilgili yeterli çalışma mevcut değildir (21). Ancak bu
değişiklikler tümör dokusunun 5-10%’undan azını ilgilendiriyor ise genellikle klinik
gidiş benign lezyonlardakine benzer olarak izlenmektedir. Bu özelliklerdeki tümörler
fokal düşük derecede atipi veya proliferasyon gösteren seröz kistadenoma,
kistadenofibroma veya adenofibroma olarak adlandırılırlar (22).
2.6.2. Borderline Seröz Tümörler:
1898 yılında Hermann Johannes Pfannenstiel, klinik olarak border malignensi
gösteren papiller ovaryan kistadenomayı tanımlamıştır (23). Carl Abel ise 1901 yılında
benign-malign büyüme paterni arasında diye belirttiği prolifere papiller kistadenomları
tanımlamıştır (24). 1929 yılında Taylor semi-malign terimini kullanmış (25), meslektaşı
Munnell ise borderline katagoriyi ve klinik davranışını tanımlayan bir makale yazmıştır
(26). 1961’de FIGO (Jinekoloji ve Obstetrik İnternasyonel Federasyonu) kanser
komitesi tarafından primer over tümörlerini klasifiye edilmiş, 1970’de kabul edilip,
1971’de de kullanılmaya başlanmıştır. Buna göre primer epitelyal tümörleri 3 gruba
ayrılmış; benign kistadenoma, düşük malignite potansiyelli ve kistadenokarsinomlar
olarak tanımlanmışlardır. 1973 WHO klasifikasyonunda ise borderline/düşük malignite
potansiyelli olarak yer verilmiştir. WHO’ya göre borderline tümörler stromaya belirgin
invazyon oluşturmayan, mitotik aktivite gösteren ve nükleer değişiklikleri benign ve
malign arasında olan tümörler olarak tanımlanmıştır (27). Sonraki 10 yılda düşük
malignite potansiyelli tümör terimi, düşük malignite potansiyelli karsinom terimi yerine
kullanılmaya başlanmıştır. Sonrasında atipik proliferatif tümör terimi de kullanılmaya
başlanmıştır. Borderline tümör terimi ise 2003 WHO sınıflamasında kullanılan
jinekolojik patolog ve onkologlar arasında en sık kullanılan terim olmuştur (28).
SBT’ler tüm seröz neoplazilerin 9-15%’ini oluşturmaktadır. Bu tümörler daha genç
yaşta gözlenmektedir [ortalama 38 (17-77)].
Büyük, genellikle multiloküler kistik neoplazilerdir. Makroskopik olarak
çoğunlukla kistik ve papiller, 2-25 cm arasında değişen (ortalama 10 cm)
uzunluklardalar. 48% vakada eksternal yüzde tümör izlenebilmektedir (Evre Ic ). 3440% bilateraldirler. Fokal veya belirgin papiller yapılar izlenir. Adenofibromatöz
borderline tümörler dışında solid büyüme paterni enderdir. Kanama veya nekroz seyrek
de olsa izlenebilir.
Küçük büyütmede kist lümenine veya over yüzeyine doğru dallanmalar izlenir.
Kompleks papiller veya glandüler patern ve sekonder kist formasyonu izlenebilir.
Papillalar sıralanma artışı gösteren epitel ile döşeli fibrovasküler kora sahiptir. Silyalı
hücreler izlenebilmektedir. Düşük dereceli nükleer atipi gösteten tümör hücreleri
genellikle eozinofilik sitoplazmalı olarak izlenirler. Gebelerde eozinofilik stoplazma
daha belirgin olarak karşımıza çıkmaktadır. Hafif veya orta nükleer atipi gösterirler.
Azında intraepitelyal karsinoma terimini hak eden fokal ağır displazi gözlenebilir.
Mitotik figürler yok yada azdır. 5% kadar tümörde 10BBA’da 4’ten fazla mitoz
gözlenir. Anormal mitotik figürler genellikle gözlenmezler. Psammom cisimcikleri
genellikle stromal mikroinvazyon alanlarında veya kist içerisine dökülmüş hücre
kümelerinde görülür.
Papilla uçlarında belirgin eozinofilik sitoplazmalı metaplastik veya indiferansiye
hücre kümeleri izlenebilir. Gland ve papilladan oluşmuş plak veya nodüller gözlenebilir.
Bunlar desmoplastik peritoneal implantlara benzer ve bunlara otoimplant adı verilir.
Bunlar daha ileri evre tümörlerde izlenmekle birlikte bunların prognostik bir önemi
yoktur (29). SBT’ü seröz adenokarsinomdan ayıran en önemli mikroskopik bulgu diffüz
stromal invazyonun gözlenmiyor olmasıdır.
Borderline tümörlerin 1.3% kadarında stromal mikroinvazyon izlenebilmektedir.
Bu limit maksimum 3 mm uzunluk veya 10 mm² ‘lik alan olarak belirlenmiştir (30).
Mikroinvaziv borderline tümörlerin, borderline tümörde küçük bir odak halinde gelişmiş
karsinomlardan ayırtedilmesi gerekmektedir. Gebelerde stromal mikroinvazyon daha sık
olarak karşımıza çıkmaktadır(31). Mikroinvaziv odaklarda farklı iki patern izlenir.
İlki ve en sık gözleneni; küçük kümeler ve kordlar halinde eozinofilik
sitoplazmalı yuvarlak veziküler nükleuslu belirgin nükleollü atipik hücrelerin gelişigüzel
kist duvarının veya bir papillanın fibröz stromasına dağılması ile ortaya çıkar. Genellikle
bu hücreler etrafında stromal reaksiyon gözlenmez. Mikroinvaziv odak çevresinde şeffaf
zon veya yarıklar izlenebilmektedir. İkinci paterne gelince stromal invazyon papilla,
küçük glandlar, kord veya epitelyal hücre yuvaları şeklindedir (32). Tümör hücreleri
çevresinde inflamasyon veya fibröz stroma izlenir. Küçük şeffaf boşluklar çevreler. Bu
paternde mikroinvazyon izlendiği zaman daha ekstensif alan varlığı ve net invazyon
varlığı mutlak daha ayrıntılı incelenmelidir. Bazı çalışmalarda mikroinvazyon izlenen az
sayıda hastada kötü klinik gidiş varlığı bildirilmiştir. Ancak bunun da hastalık dışı diğer
faktörler ve inkomplet evreleme nedeniyle olduğu savunulmuştur (29).
SBT’ lerde over dışına hastalık yayılımı yüksek oranda izlenmektedir. 20-46%
oranında peritoneal, omental implantlar izlenir (33). Over yüzeyinde ekzofitik gelişen
tümörler ile daha sık birliktedir. İmplant gösteren vakaların 94%’ünde ekzofitik gelişim
izlenmiştir (34).
1970 ve 1980’lerde implantların prognostik önemi olmadığı
düşünülmüş ve mikroskopik görünümlerine göre non-invaziv ve invaziv olmak üzere
ayrılmışlardır (35). Son zamanlarda önemli bir prognostik faktör olduğu sonucunda
çalışmalar mevcuttur (36).
Peritoneal implantlar invaziv ve non-invaziv olarak sınıflandırılmaktadırlar.
Non-invaziv implantlar da epitelyal, desmoplastik veya her ikisi olmak üzere ayrılırlar.
83-96% oranında peritoneal implantlar non-invazivdir. İnvaziv büyüme, ağır sitolojik
atipi ve mitoz varlığı kötü prognozu işaret etmektedir (37). Non-invaziv implantlar
yüzeye yapışmış gibi görünürler. Desmoplastik non-invaziv implantlar selüler fibröz
doku veya granülasyon dokusu benzeri bir görünüm ile küçük tümör grupları, papilla
veya belirgin eozinofilik sitoplazmalı tek hücre şeklinde izlenirler. İnvaziv implantlarda
neoplastik epitelyal hücreler daha geniş, kompleks glandüler, mikropapiller ve
kribriform yapılar meydana getirirler. SBT ile birlikte olan neoplastik ekstraovaryan
tümörlerin ovaryan tümörün implantı mı; yoksa peritondan multisentrik gelişim
sonucunda mı oluştuğu tartışmalıdır (38). Yapılan çalışmalarda KRAS mutasyonu
inklüzyon kistleri ve implantlarda da gözlenmiştir (39). Moore ve arkadaşları Müllarian
inklüzyon kistlerinin istatistiksel olarak belirgin bir şekilde SBT’ler ile birlikteliğini
göstermiştir
(40).
Metastazın
gelişimsel
sürecinde
bir
basamak
olabileceği
savunulmuştur.
Pelvik ve paraaortik lenf nodülü invazyonu 7-23% oranında, cerrahi olarak lenf nodu
diseksiyonu yapılan hastada mevcuttur. Çok az hastada da post operatif servikal ve
skalen lenf nodülünde invazyon gözlenebilir (41-46).
FIGO evreleme sistemine göre 68%’i evre I, 11%’i evre II, 21%’i evre III ve
1%’inden azı da evre IV’tür. 40% hastada bilateral tümör izlenmektedir. Evre I SBT’ler
mükemmel prognoza ve 100%’e varan hastalıksız sağ kalım oranlarına sahipse de
peritoneal implant bulunduran SBT’lerin seyrek gözlenmesi nedeniyle bunların
prognozları ve bu tür hastalara verilecek strandart bir tedavi rejimi bilinmemektedir.
2.6.2.1. Mikropapiller varyant:
Farklı vaka serilerinde 6% ve 12-18% oranlarında bildirilmiştir (47-48). Tipik
borderline tümörler ile karşılaştırıldığında, mikropapiller tümörlerin daha çok bilateral
oldukları, over yüzeyinde daha çok egzofitik gelişim gösterdikleri ve daha ileri evre
oldukları savunulmaktadır. Fibröz papilla yüzeyinden veya direkt kist duvarından çıkan,
hiyerarşik dallanma paterni göstermeksizin gelişen, ince papiller hücre proliferasyonu
şeklinde izlenirler. Prolifere hücreler uzun ince papiller yapılar meydana getirirler.
Papillaların uzunluğu, eninden en az 5 kat daha fazla olmalıdır. Yüksek nükleer atipi
beklenmez. Kübik, “hobnail” şekilli uniform nükleuslu, seyrek mitoz gösteren
hücrelerden oluşurlar. Daha kötü prognozun daha sık izlenen invaziv peritoneal
implantlar nedeniyle olduğu savunulmaktadır (36). Güncel WHO klasifikasyonunda da
SBT’lerin varyantı olarak kabul edilmektedirler.
2.6.3. Seröz adenokarsinomlar:
Genellikle bilateral ve büyük tümörlerdir. Kistik, papiller veya solid büyüme
paterni gösterirler. Solid alanlar kirli beyaz renkte ve hemoraji, nekroz içerir. Ovarian
kapsül sıklıkla tümörlüdür. Ekstensif ekstraovaryan tümörlerde overde fokal (≤0,5 cm)
yüzeyel tümör olması primer peritoneal seröz karsinomun overe infiltrasyonu olarak
yorumlanır (49). Fibrotik stromaya diffüz infiltrasyon söz konusudur. Papiller yapılar
fokal bile olsa genellikle izlenir. Papillalar stratifiye kısa kolumnar hücrelerle döşelidir.
Gland ve solid kordonlar oluşturabilir. Yarıklanmalar tipiktir. Mikrokistik büyüme, taşlı
yüzük benzeri hücreler izlenebilir. Belirgin atipi, artmış mitoz gösterir.
Düşük dereceli seröz karsinomlarda glandlar mikropapiller ve yuvalanmalar oluşturan
orta derecede atipi gösteren tümör hücrelerinin fibröz stromaya invazyonu izlenir.
Düşük dereceli karsinomların borderline tümörler zemininde geliştiği düşünülmektedir.
Gradeleme sistemi Silverberg tarafından kullanılmaya başlanmıştır (50);
Arkitektürel skor:
Glandüler belirgin
1 puan
Papiller belirgin 2 puan
Solid patern
3 puan
Nükleer skor:
Hafif atipi
1 puan
Orta atipi
2 puan
Ağır atipi
3 puan
Mitotik skor:
0-10 mf/10 HPF 1 puan
11-25 mf/10 HPF
2 puan
≥25 mf/10 HPF 3 puan
Tümör grade’i
3-5 puan gradeI
6-7 puan grade II
8-9 puan grade III olarak belirlenir
Sıklık
Düşük dereceli
~25%
Histolojik
Prekürsör
Klinik
Özellikler
Lezyon
Davranış
Mikropapiller
Seröz kistadenom
indolent
arkitektür
Borderline tümör
yavaş seyir
Tanımlanmamış
agresif
KT
Cevabı
zayıf
düşük mitotik
aktivite/low-grade
nükleus
Yüksek dereceli ~75%
Solid adal
iyi
yüksek mitotik
aktivite/high-grade
nükleus
Tablo
2.6.2:
Düşük
ve
Yüksek
Dereceli
Seröz
adenokarsinomların
Klinikopatolojik özeti
2.7. KLİNİK BULGULAR, PROGNOZ, EVRELEME VE TEDAVİ
YAKLAŞIMLARI
Seröz adenokarsinomlar en sık 6. dekatta izlenirken, Seröz borderline tümörler 3.
ve 4. dekatta izlenirler. Tanı anında vakaların 70%’ i ileri evre tümörlerdir. Pelvik ağrı,
abdominal dolgunluk hissi, gastrointestinal sisteme ya da üriner sisteme bası sonucu
gelişen semptomlar, mestrüel anomaliler izlenebilir. Torsiyon ve rüptüre bağlı akut
belirtiler olabilir. Pelvik kaviteye yayılım gösteren tümörlerde, douglas boşluğunda
tümör nodülleri bimanuel rektovajinal muayenede tespit edilebilir. Asit gelişmi
izlenebilir. İleri evre tümörlerde lenfatik yayılım ile inguinal veya sol supraklaviküler
lenf nodüllerine yayılım izlenir. Plevral kaviteye infiltrasyon sonucu malign efüzyon
oluşabilir. İleri dönemde abdominal yayılım ile gatrointestinal sisteme bası ve ileus
sonucu bulantı, kusma ve karın ağrısı izlenebilmektedir.
Prognozda en önemli parametre klinik evredir. Operasyon sonrası geride kalan
tümör hacmi diğer bir önemli prognostik faktördür. Serum CA-125 düzeylerinin
bağımsız bir prognostik faktör olmadığı gösterilmiştir. Postoperatif CA-125 düzeyinin
daha yüksek prognostik önemi olduğu savunulmaktadır.
FIGO EVRELEME SİSTEMİ
Evre I tümör overe sınırlı
Ia tümör bir overe sınırlı; kapsül intakt; over yüzeyinde tümör yok;
asit veya peritoneal yıkamada malign hücre yok
Ib tümör her iki overde sınırlı; kapsül intakt; over yüzeyinde tümör yok;
asit veya peritoneal yıkamada malign hücre yok
Ic tümör bir veya iki overde sınırlı; aşağıdakilerden herhangi biri mevcut
kapsül rüptürü; over yüzeyinde tümör varlığı; asit veya peritoneal yıkamada malign
hücre mevcut
Evre II tümör bir veya her iki overde ve pelvik yayılım
IIa uterus ve/veya fallop tüblerine yayılım ve/veya implantlar;
asit veya peritoneal yıkamada malign hücre yok
IIb diğer pelvik organlara yayılım;
asit veya peritoneal yıkamada malign hücre yok
IIc pelvik yayılım; asit veya peritoneal yıkamada malign hücre mevcut
Evre III tümör veya iki overde; mikroskopik olarak doğrulanan pelvis dışına
peritoneal metastaz ve/veya rejyonel lenf nodülü metastazı
IIIa pelvis dışına mikroskopik peritoneal metastaz
IIIb pelvis dışına ≤2 cm uzun çaplı makroskopik peritoneal implant
IIIc pelvis dışına ≥2 cm uzun çaplı makroskopik peritoneal implant ve/veya
rejyonel lenf nodülü metastazı
Evre IV uzak metastaz
Evre
5
yıllık
sağ
Evre
kalım (%)
5
yıllık
kalım (%)
I
78
IIc
61
Ia
84
III
22
Ib
79
IIIa
52
Ic
73
IIIb
29
II
59
IIIc
18
IIa
65
IV
14
IIb
54
Tablo 2.7: FIGO evresine göre 5 yıllık sağ kalım oranları
sağ
Benign tümörlerde kistektomi ve unilateral salpingooferektomi ile kür
sağlanmaktadır. Borderline tümörlerin 80%’i tek overlerde sınırlıdırlar. Borderline
tümörler için standart cerrahi tedavi yaklaşımı TAH+BSO, omentektomi ve
ekstraovaryan tümör implantlarının rezeksiyonudur. Reprodüktif çağdaki kadınlarda
kistektomi unilateral ooferektomi tercih edilebilmekte, ancak bu hastalarda karşı overde
rekürrens riski %25 olarak belirtilmekte. Rekürren tümör borderline seröz tümör
olabildiği gibi yüksek gradeli seröz karsinoma olarak da karşımıza çıkabilmektedir.
Seröz adenokarsinom tedavisinde cerrahi ve kemo/radyoterapi uygulanır.
Standart cerrahi yaklaşım; TAH+BSO, omentektomi, pelvik ve paraaortik lenf nodülü
diseksiyonu,
evreleme
biyopsileri
ve
endikasyon
dahilinde
apendektomidir.
Ekstraovaryan olabildiğince fazla tümör eksizyonu amaçlanır. Böylelikle kemoterapi ve
radyoterapiye duyarlılığı artırmak amaçlanır. Evre Ia’lı genç hastalarda unilateral
salpingo-ooferektomi,
omentektomi
fertilitenin
korunması
amacıyla
uygulanabilmektedir. İleri evrede cerrahi yaklaşımı kolaylaştırmak amacıyla neoadjuvan
kemoterapi uygunabilmektedir.
2.8. RAS/ RAF/ MEK / MAPK YOLAĞI VE TEZ ÇALIŞMASINDA
KULLANILAN İMMÜNHİSTOKİMYASAL BELİRTEÇLER
Şekil 2.8.1: MAPK yolağı
Hormonlar, büyüme faktörleri, diferansiasyon faktörleri ve tümör promoter
maddeler RAS/RAF/MEK/MAPK sinyal yolunu kullanırlar. Bu iletim yolu RAS
aktivasyonu ile başlar ve sırasıyla RAS(= MAPKKK), MEK (= MAPKK) ve Erk (=
MAPK) proteinleri ile kinaz kaskadı ilerler. RAS ve RAF protoonkogendir.
RAS, membrana bağlı bir G proteinidir ve birçok tirozin kinaz reseptörünü
aktive etmektedir. Serin treonin ve tirozin non-reseptör kinaz kaskadını aktive eder.
Erk1 ve Erk2 transkripsiyon faktörlerini fosforile ve aktive eder.
RAS proteinlerinin aktif hale gelmesi için translasyon ve modifikasyondan sonra
membrana yerleşmesi gerekir. İstirahat halindeki hücrelerde RAS proteinleri inaktif
(RAS-GDP) halde bulunurlar. Hücrenin uyarılması ile GDP’nin yerine GTP bağlanarak
aktif konformasyona dönüşüm (RAS-GTP) tetiklenir. RAS aktivasyonu tersinir bir
süreçtir. Bu aktivasyonda rol oynayan moleküller, SOS (son of sevenless) ve Grb2
(growth-factor-receptor-bound protein 2) adaptör proteinleridir. Bu sinyal yolunun
efektör molekülleri, SOS üzerinde negatif düzenleyici etki ile RAS aktivasyonunu
sonlandırmaktadır. Aktive olan RAS proteinleri RAF kinazlara yüksek afinite ile
bağlanırlar ve RAF kinazların hücre membranına yerleşimini ve aktivasyonunu sağlarlar
(51-52).
İnsan tümörlerinin %30’unda RAS/RAF/MEK/ERK yolunun aşırı aktivasyonu
söz konusudur (51). Bu oran tümörlerdeki RAS mutasyonu sıklığı ile uyumludur.
Mutant RAS proteinleri, aktif RAS-GTP formunda kalırlar; bu nedenle, hücrenin
kontrolsüz uyarılmasından sorumlu tutulmaktadırlar.
RAS iletim yolu ile tetiklenen transformasyon sürecinde sinerjik etkileşim de
önem taşır. Normal koşullarda, EGF ve PDGF gibi büyüme faktörlerinin fosfoinozitid-3
kinaz (PI-3K) yolunu uyarmalarında RAS’ın etkinliği minimal düzeydedir. Buna
karşılık onkojenik RAS, PI-3K yolunun güçlü bir aktivatörüdür. Onkojenik RAS bu
yolu aktive ederek apoptozisi baskılar (53). İnsan kanserlerinin önemli bir bölümü epitel
hücrelerinden köken alır. Dolayısıyla, bu hücrelerde apoptozisin baskılanması
karsinogenez sürecinde kritik etkenlerden birini oluşturur. Ayrıca, onkojenik RAS
uyarısı, transforme hücrelerde normal hücrelerden farklı genlerin ekspresyonunu da
uyarabilir.
İnsan tümörlerinde tek en sık dominant onkogen anormalliği RAS geninde
mutasyondur. GF ile indüklenen mitogenez olayında RAS önemli rol oynar. RAS
blokajı GF’lerin proliferatif cevabını önler. RAS, GF ile aktive olunca GDP’den GTP’ye
döner aktive olur ve RAF’ı hareketlendirir. RAF ise MAP kinaz yolunu uyararak
mitogenez başlatır. GTP’az aktivitesi ile GTP, GDP’ye döner ve RAS sakin hale gelir.
RAS’ın düzenli işlemesi GDP ile GTP arasındaki olaylara bağlıdır. Bu olaylar
enzimatiktir.
Aktive olan RAS diğer protein olan RAF’a bağlanır bu da MAP kinaz (Mitojen
aktive eden protein kinaz) uyarı sistemi yolunu aktive ederek uyarı nükleusa iletilir.
Uyarı nükleusa girince transkripsiyon faktörleri olan c-jun ve c-fos fosforile olur. Bu
uyarılarla siklusun S fazına girmesi sağlanır. BRAF somatik mutasyonu ile aktivasyonu
birçok kanserde bildirilmiştir. Kutanöz melanom ve tiroidin papiller karsinomlarında
yüksek oranlarda bildirilmiştir (54).
Mutasyon 80% oranında kinaz domaindeki
1796’ncı nükleotid pozisyonunda T yerine A gelmesi ile oluşur. Böylelikle 599’ncu
aminoasit pozisyonuna valin yerine glutamik asit geçer. KRAS’ta da kodon 12 ve 13 ‘te
değişiklikler saptanır.
MAP kinazlar, “Mitogen-activated protein kinases” süper ailesinde yer alırlar
(55). Ökaryotik hücrelerin tümünde mevcut olan bu proteinler hücre membranından
çekirdeğe bilgi aktarılmasında büyük önem taşımaktadır. Bu sinyal iletimi kaskadları,
embriyogenezis,
yaşama,
çoğalma,
diferansiasyon
ve
apoptozis
işlevlerinin
düzenlenmesinde rol alır. MAP kinazlar üç ana gruba ayrılır (56).
1. p38 MAP kinaz ailesi,
2. “Extracellular signal regulated kinase (ERK)” ailesi,
3. “c-Jun NH2- terminal kinase (JNK)” ailesi
MAPK’ lar Thr ve Tyr domainlerden dual fosforilasyon ile aktive olurlar. ThrGlu-Tyr (ERK), Thr-Pro-Tyr (JNK) veya Thr-Gly-Tyr (p38) katalitik domainin
subdomain VIII’inden aktive olurlar. Bu
fosforilasyon MAPK kinaz kinaz
fosforilasyonu ve devamlılığında MAPK kinaz aktivasyonu ile MAPK aktive olur.
JNK’ın MKK4 ve MKK7 tarafından aktive olduğu, p38’in MKK3, MKK6 ve MKK4
ile, Erk’in ise MKK1 ve MKK2 ile aktive olduğu bilinmektedir.(57).
Şekil 2.8.2: MAPK ailesi ve sinyal iletimi
ATF: “Activating transcription factor”, ERK: “Extracellular signal regulated kinase”, GTP: “Guanosine
triphosphate”, JNK: “c-Jun N-terminal kinase”, MAPK: “Mitogen-activated protein kinase”, MEK:
“Mitogen extracellular signal regulating kinase”, MEKK: “MAPK/ERK kinase kinase”, MKK: “MAPK
kinase”, MKKK: “MAPK kinase kinase”, p38: “p38 kinase”, RTK: “Receptor tyrosine kinase”.
MAPK’ların aktivasyonu ile transkripsiyon faktörlerinin fosforilasyonu ile gen
ekspresyonunu regüle ederler. ERK kaskadı büyüme faktörleri ile aktive olur ve hücre
proliferasyonunda kritik öneme sahiptir. JNK ve p38 ise genotoksik ajanlar, stres ile
ortaya çıkan sitokinler, büyüme arresti ile olur. Apopitozisde önemli rolü vardır.
Büyüme uyarımlarının çoğu MAPK’ı aktive eden kinaz cascade’i üzerinde birleşirler.
ERK1 ve ERK2 de denir. (Extrasellular Sinyal-Regülasyonlu Kinaz 1 ve 2). MAPK
aktive edildikten sonra çekirdeğe girer ve derhal erken genlerin transkripsiyonunu
indükler. MAP kinaz yolu reseptör aracılı uyarının hücre içine iletiminden sorumlu bir
kinaz kaskadı olarak çalışır. Kaskad sistemi hem sinyalin amplifikasyonu hem de
düzenleyici etkileşimler (sinyalin süresi, şiddeti ve kinetiği) açısından önem taşır.
Sinyalin iletimi G-protein aktivasyonu (RAS aktivasyonu) ile başlar ve MAPKKK’nın
(MAP kinaz kinaz kinaz) aktivasyonundan sonra sırasıyla MAPKK (MAP kinaz kinaz)
ve MAPK (MAP kinaz) aktive olur. MAPK ise sitoplazmik substratlarını (hücre iskeleti
elemanları, diğer protein kinazlar) ve/veya nükleusta transkripsiyon faktörlerini
fosforilasyon yoluyla aktive eder ve hücrenin biyolojik cevabı oluşur.
Nükleer transkripsiyon faktörleri, DNA replikasyonu ve hücre bölünmesi için
görev yapan nükleus yerleşimli moleküllerdir. Bunların en önemlileri myc, jun ve fos
molekülleridir.
Myc geni amplifikasyon veya translokasyon şeklinde mutasyona uğrar. Myc
molekülü sentezlenir sentezlenmez nükleusa taşınır, bu taşınma sırasında veya nükleusta
max molekülü ile heterodimer oluşturur. Myc-max heterodimerlerinin potent bir
transkripsiyon aktivatörü olmaları nedeniyle myc-max bağlanmasını engelleyen
mutasyonlar onkojenik aktiviteyi azaltmaktadır. Ayrıca mad isimli bir regülatör protein
de max’a bağlanarak mad-max heterodimerleri oluşturabilmekte ve bunlar da
transkripsiyonu baskılayabilmektedir. Yani transkripsiyon aktivasyonu sadece c-myc
varlığına değil max ve mad proteinlerinin varlığına ve miktarına da bağlıdır. GF ile
sinyal gelmez ise ve myc aktive olursa hücreler apoptozise gider. C-myc amplifikasyonu
meme, kolon, akciğer karsinomlarında bildirilmekte, n-myc ve l-myc ise nöroblastom ve
küçük hücreli akciğer karsinomlarında amplifiye olmaktadır.
Şekil 2.8.3: c-myc protein fonsiyonları
c-Myc, n-Myc ve L-Myc genleri çeşitli transkripsiyon faktörlerini kodlar ve
hücre proliferasyonu, büyümesi, diferansiasyonu ve apopitoziste önemli görevleri
vardır. Myc proteini transkripsiyon aktivasyonu için gerekli olan N-terminal
transaktivasyon domainine ve DNA bağlanmasında ve protein interaksiyonunda kritik
öneme sahip olan C-terminal domainine sahiptir.
c-FOS geninin transkripsiyonu ilk kez 1984 yılında Mike E. Greenberg ve Ed B.
Ziff tarafından büyüme faktörleri ile stimüle ettikleri fibroblastlarda gösterilmiştir (58).
c-FOS geni hücrede herhangi bir uyarana karşı ilk yanıt veren genlerdendir. Bu gruba
giren genler hücre büyümesi, çoğalması, farklılaşması ve apopitozis ile ilgili
transkripsiyon faktörleridir. c-FOS geni nükleer bir transkripsiyon faktörüdür. Hücresel
işlevler yönünden ana anahtar olarak düşünülmektedir (59-60). Bir diğer tanımla nükleer
protoonkogen
olan
c-FOS
hücre
çoğalması
ve
farklılaşması
sırasında
gen
expresyonunun aşamalı düzenlenmesi ile ilgilidir (61). FOS proteinleri c-FOS geninin
ürünü olan çekirdek proteinleridir. Bunların hücrede ekspresyonu ve birikimi herhangi
bir etki olmaksızın görülebilir ancak bu ekspresyon ve birikim çeşitli uyaranlara yanıt
olarak hücre aktivasyonu ile birlikte artar (62).
FOS proteinleri herhangi bir uyarana ilk yanıt veren genlerden olan c-JUN
geninin ürettiği JUN proteinleri ile birlikte transkripsiyon faktör kompleksi Activator
Protein-1 (AP-1) in komponentleri olarak işlev görürler (63). AP-1; FOS proteinleri (cFOS, Fos B, Fra 1 ve Fra 2), JUN proteinleri (c-JUN, Jun B, Jun D) ve bazı ATF
proteinlerinden (ATFa, ATF-2 VE ATF-3) oluşmuştur. Bütün AP-1 proteinleri
fosfoproteinlerdir ve hiperfosforilasyon ve defosforilasyon bu proteinlerin DNAbağlanma ve transaktivasyon aktivitelerini etkileyebilir (64). AP-1 kompleksinin üyeleri
değişik gen ekspresyonlarını modüle ederler ve çok sayıda hücresel süreçte kritik olarak
ilgilidir. Kanser gelişiminde FOS proteinlerin katkısı olduğu bildirilmektedir (65). Bazı
tümör tiplerinde c-FOS ve c-JUN düzeylerinin arttığı gösterilmiş ve bu artışın artan
hücre çoğalmasının bir kanıtı olacağı için tümörogeneziste önemli rol oynadığı ileri
sürülmüştür (66-67). Büyüme faktörleri c-FOS’u ERK (extracellular signal related
kinase) aktivasyonu yoluyla uyarır (68). c-FOS transkripsiyon büyüme faktörleri ile
uyarıldıktan sonra hedef genlerin transkripsiyonunu aktive eder. PEK(proenkefain) ve
TH (tirozin hidroksilaz) genleri c-FOS’un potansiyel hedefleridir (59).
3. MATERYAL VE METOD:
3.1. Olgu Seçimi ve Doku Mikroarray&Makroarray (TMA) Bloklarının
Hazırlanması
Bu çalışmada 2000-2007 yılları arasında, Ankara Üniversitesi Tıp Fakültesi
Patoloji Anabilim Dalı’nda raporlanmış ooferektomi materyalleri incelenmiştir. 12
Borderline Seröz Tümör (SBT), 41 Seröz Adenokarsinom (SAK) ve Seröz Papiller
Kistadenofibrom, Morgagni Kisti, Seröz Kistadenom ve Basit Seröz Kistlerinden oluşan
19 vaka ile birlikte, toplam 72 vaka üzerinde çalışılmıştır. 41 SAK vakası grade II ve
grade III vakaları içermektedir. Grade I olarak izlenen 1 vakanın tümörlü blokları
optimal düzeyde olmadığı için çalışma dışında bırakılmıştır. 19 vakalık benign lezyonlar
tek bir grup kabul edilmiştir. Olguların H.E. boyalı kesitleri ışık mikroskobi ile yeniden
incelenmiş, histopatolojik bulgular kaydedilmiş ve her vaka için tümörlü alanlar cam
kalemi ile çizilerek işaretlenmiştir. Tümörlü alanları çizilmiş bu H.E. boyalı kesitler ile
olguların parafin blokları eşleştirilmiştir.
Mikroarray işlemi için bu tümörlü bloklar verici blokları, normal parafin
bloklardan daha yüksek ve daha enli hazırlanmış, normal parafinden farklı olarak 37
derecede eriyen plastik parafin ile doldurulmuş bloklar ise alıcı blokları oluşturmaktadır.
Alıcı blok düzgün bir yüzey elde edilene kadar tıraşlanmış ve daha sonra ‘Beecher
Instruments Mikroarrayer’ ile alıcı blokta 1,5 mm çap ve 3-4 mm yükseklik gösteren
kuyular açılmıştır. Her bir kuyuya verici bloktan alınan tümörlü doku yerleştirildikten
sonra, her bir doku silindiri arasında 2 mm mesafe kalacak şekilde, aynı sıra ile işleme
devam edilmiştir. Olgular her bir sırada bir kontrol dokusu ve bir TMA bloğunda 6 sıra,
her bir sırada 10 doku silindiri bulunacak şekilde hazırlanmış haritalara göre
yerleştirilmiştir. Tüm vakalardan 3’er tümörlü doku silindiri hazırlanmıştır. Böylelikle 2
adet TMA bloğu hazırlanmıştır.
Bunun dışında daha geniş bir alanı görebilmek amacıyla, benign lezyonlardan ve
borderline tümör bloklarından makroarray blokları yapılmıştır. Bunun için yine
olguların tümörlü alanları işaretlenmiş, her bir tümörden 2 adet, 3 mm çapında dokular
alınmış ve 3 sıra, her sırada 4 doku olacak şekilde yerleştirilmiştir.
Böylelikle makroarray bloklarında 12 adet doku izlenmiştir. Seröz papiller
karsinomlardan iki adet mikroarray bloğu ve iki adet makroarray bloğu, borderline ve
benign lezyonlarından oluşan 5 adet makroarray bloğu ile birlikte toplam 9 adet parafin
blokta inceleme yapılmıştır. Bu bloklardan 4 mikron kalınlığında kesitler alınmış, birer
kesit H.E. boyanmış, diğer kesitler İHK’sal boyamalarda kullanılmıştır.
3.2. Klinik ve Histopatolojik İnceleme
Seröz Borderline, Seröz Adenokarsinom ve benign lezyonların izlendiği
vakaların yaşları ve izlenen tümörün lokalizasyonları kaydedilmiştir. Histopatolojik
olarak arkitektürel, nükleer ve mitotik aktiviteye göre Seröz Adenokarsinomlar iyi
diferansiye grade I, orta diferansiye grade II ve az diferansiye grade III olarak
değerlendirilmiştir.
3.3. İmmünhistokimyasal İnceleme
3.3.1. Kullanılan Antikorların özellikleri:
Kullanılan antikorların klon isimleri, dilüsyonları ve ticari kaynakları Tablo
3.1’de belirtilmektedir.
Antikor
Klon
Dilüsyon
Ticari kaynak
c-Myc
sc-47694
1/1500
Santa Cruz
c-Fos
sc-52
1/100
Santa Cruz
c-Jun
sc-1694
1/150
Santa Cruz
p38
sc-7973
1/100
Santa Cruz
Tablo 3.1: İmmünhistokimyasal antikorların özellikleri
Kullanılan Kontroller:
İHK’sal boyamalarda c-Myc için nöroendokrin karsinom, c-Jun için benign
prostat hiperplazisisi, c-Fos için oral mukoza ve özofagus mukozası, p38 için ise prostat
adenokarsinomu kontrol dokular olarak kullanılmıştır.
3.3.2. İmmünhistokimyasal Boyama:
Ventana i-View DAB Detection kit kullanılarak; c-Myc, c-Fos ve c-Jun Ventana
Benchmark İHK otomatik boyama makinesi ile p38 ise Zymed kit kullanılarak elde
boyama yapılmıştır.
3.3.3. İmmünhistokimyasal Boyanmaların Değerlendirilmesi:
3.3.3.1. İmmünhistokimyasal Markerların Boyanma Şekilleri:
p38, c-Myc, c-Jun ve c-Fos nükleer proteinler oldukları için spesifik boyanma
nükleer boyanma olarak kabul edilip değerlendirilmiştir. Özellikle c-Myc ve c-Jun ile
yapılan bazı çalışmalarda ekspresyon artışında sitoplazmik boyanmanın da olduğu
bildirilmiştir. Bu nedenle sitoplazmik boyanmaları da ayrıca değerlendirilmiştir.
3.3.3.2. İmmünhistokimyasal Markerların Boyanma Skorları:
Yaygınlık ve şiddet olmak üzere iki parametre olarak nükleer ve sitoplazmik
boyanmalar ayrı ayrı skorlanmıştır. Her dört marker için de aynı skorlama sistemi
kullanılmıştır.
Nükleer/Sitoplazmik Boyanma Yaygınlık;
0: Hiç boyanma yok
+1: %1-25 oranında boyanma var
+2: %26-50 oranında boyanma var
+3: %51-75 oranında boyanma var
+4: %76-100 oranında boyanma var
Nükleer/Sitoplazmik Boyanma Şiddet;
0: Hiç boyanma yok
+1: Hafif şiddette boyanma var
+2: Orta şiddette boyanma var
+3: Şiddetli boyanma var
3.4. TMA Bloklarında Doku Silindirlerinin Değerlendirilmesi:
İmmünhistokimyasal markerlar değerlendirilirken her bir doku silindirinin tek
tek boyanma şekli ve boyanma skoru kaydedilmiştir. İstatistiksel inceleme aşamasında
her vaka için alınan 2 ve 3 doku silindirlerinden en yüksek boyanma skoruna sahip olan
alınmıştır. Her vakadan 2 veya 3 adet alınan doku silindirlerinin de uygun olmadığı,
doku silindirlerinin tümüyle nekroz içermesi veya kesit sırasında dökülmesi gibi
durumlarda o vaka değerlendirmeden çıkarılmıştır.
3.5. İstatistiksek Değerlendirme:
Verilerin istatistiksel değerlendirmeleri ‘SPSS 9.0 for Windows’ bilgisayar
programında gerçekleştirilmiştir. Yaş ve lokalizasyon değerlendirmesinde ki-kare testi
kullanılmış, immünhistokimyasal markerların boyanma şiddetleri ve yaygınlıkları ise
Kruskal-Wallis çoklu karşılaştırma testi kullanılarak araştırılmıştır.
4. BULGULAR
4.1. Klinik Bulgular
Çalışma grubunda yer alan toplam 72 olgu içerisinde 12 Borderline Seröz Tümör
(SBT) vakasının yaş ortalaması 44,17 (26-65), 41 Seröz Adenokarsinom (SAK)
vakasının yaş ortalaması 57,49 (22-80) ve 19 benign lezyonundan oluşan vakaların yaş
ortalaması ise 51,68 (29-87) olarak bulunmuştur (Tablo 4.1). İstatistiksel olarak
bakıldığında BST vakaları ile SAK vakaları arasında anlamlı bir fark elde edilmiştir.
Benign grubu oluşturan hastalar arasında Seröz Adenokarsinom hastaları ve Seröz
Borderline tümör hastaları arasında istatistiksel bir farklılık saptanmamıştır [(p: 0,003;
p<0,05) Kruskal-Wallis].
Yaş Ortalama +/-St.Dv.
SBT
SAK
Benign
44,17+/-12,655
57,49+/-
51,68+/-14,576
14,100
Yaş Ortanca (Min.-Max)
46 (26-65)
Tablo 4.1: Olguların yaş ortalaması
58 (22-80)
49 (29-87)
Tümör lokalizasyonlarına gelince 12 SBT vakasının 4’ü sağ (33,3%), 1’i sol (8,3%)
overde izlenirken 7’si bilateral (58,3%) yerleşimli olarak izlenmiştir. SAK’ların 8’i sağ
(19,5%), 4’ü sol (9,8%) ve 29’u bilateral (70,7%) yerleşimlidir. Benign grubun ise 4’ü
sağ (21,1%), 5’i sol (26,3%) ve 10’u bilateral (52,6%) olarak izlenmiştir.
Lokalizasyonlara bakıldığında gruplar arasında anlamlı bir fark izlenmemiştir. (Tablo
4.2)
Sağ
Sol
Bilateral
SBT
4 (3,3%)
1 (8,3%)
7 (58,3%)
SAK
8 (19,5%)
4 (9,8%)
29 (70,7%)
Benign
4 (21,1%)
5 (26,3%)
10 (52,6%)
Total
16 (22,2%)
10 (13,9%)
46 (63,9%)
Tablo 4.2: Vakaların lokalizasyonları dağılımı
4.2. Histopatolojik Bulgular
Üçlü gradeleme sistemine göre; 41 Seröz Adenokarsinom 8’i de grade II olarak
izlenmiştir. Geri kalan 33 vaka ise grade III Seröz Adenokarsinomdur. Grade II
tümörlerde nisbeten papiller arkitektür seçilebilmekte, Grade III SAK’lar ise solid
gelişim paterni göstermekte ve sık mitoz ve nükleer pleomorfizm göstermektedir.
4.3. İmmünhistokimyasal Bulgular
4.3.1. İmmünhistokimyasal Markerların Sonuçları:
4.3.1.1. c-Fos:
Borderline Seröz Tümörlerde (SBT) nükleer boyanma genellikler hafif-orta
şiddete izlenmiştir [şiddet-ortanca:1,00 (1-2)]. Tümör hücrelerinin 50%’ye yakınında
nükleer boyanma elde edilmiştir [yaygınlık-ortanca: 2,00 (1-3)]. Tümör hücrelerinde
izlenen sitoplazmik boyanma yaygınlığı 50% oranında [yaygınlık-ortanca: 2,00 (1-3)].
Sitoplazmik boyanma şiddeti ise genellikle hafif şiddete boyanma şeklinde izlenmiştir
[şiddet-ortanca: 1,00 (1-2)] (Tablo 4.3)
Seröz Adenokarsinom (SAK) vakalarının 25 tanesinde nükleer boyanma
gözlenmezken, geri kalan 16 vakada hafif şiddette [şiddet-ortanca: 0 (0-1)] ve genellikle
fokal nükleer boyanma elde edilmiştir [yaygınlık-ortanca: 0 (0-2)]. SAK vakalarında
sitoplazmik boyanma hafif-orta şiddet izlenmiş [şiddet-ortanca: 1 (0-2)], sitoplazmik
boyanma yaygınlığı genellikle tümör hücrelerinin yaklaşık 50%’sinde görülmüştür [
yaygınlık-ortanca: 2 (0-4)]. (Tablo 4.3)
Benign grubu oluşturan seröz adenofibrom ve basit seröz kistlerde izlenen c-Fos
nükleer boyanma şiddeti genellikle hafif şiddettedir [şiddet-ortanca: 1 (0-3)]. Genel
olarak hücrelerin 50%’sine yakınında nükleer boyanma saptanmıştır [yaygınlık-ortanca:
2 (0-4)]. Sitoplazmik boyanma hafif şiddete izlenirken [şiddet-ortanca: 1 (1-2)],
sitoplazmik boyanma hücrelerin yaklaşık 50%’sine yakınında izlenmiştir [yaygınlıkortanca: 2 (1-4)]. (Tablo 4.3)
SBT
c-Fos N y*
c-Fos N ş*
c-Fos S y*
c-Fos S ş*
1,83 +/-0,937
1,25 +/-0,452
2,42 +/-0,669
1,33 +/-0,492
2 (1-3)
1 (1-2)
2 (1-3)
1 (1-2)
0,41 +/-0,547
0,39 +/-0,494
2,22 +/-1,151
1,05 +/-0,384
0 (0-2)
0 (0-1)
2 (0-4)
1 (0-2)
2,00 +/-1,414
1,42 +/-1,017
2,00 +/-1,054
1,21 +/-0,419
2 (0-4)
1 (0-3)
2 (1-4)
1 (1-2)
Ortalama +/-St.Dv.
SBT
Ortanca (Min-Max)
SAK
Ortalama +/-St.Dv.
SAK
Ortanca (Min-Max)
Benign
Ortalama +/-St.Dv.
Benign
Ortanca (Min-Max)
Tablo 4.3: c-Fos boyanma skorları
* N y: Nükleer yaygınlık; N ş: Nükleer şiddet;
S y: Sitoplazmik yaygınlık; S ş: Sitoplazmik şiddet
İstatistiksel olarak Kruskal-Wallis çoklu karşılaştırma testinde, SBT ve
SAK’ların nükleer boyanma şiddeti ve yaygınlığında anlamlı bir fark saptanmıştır
(p<0,05). SBT ve benign lezyonların oluşturduğu grup arasında anlamlı bir fark
görülmemiştir (p>0,05). SAK ile benign lezyonlar karşılaştırıldığında da yine
istatistiksel olarak anlamlı bir fark saptanmıştır. (p<0,05) (Tablo 4.4)
Fark SBT -SAK
Fark SAK-Benign
Fark SBT - Benign
Nükleer yaygınlık
0,000 (p<0,05)
0,000 (p<0,05)
0,756
Nükleer şiddet
0,000 (p<0,05)
0,000 (p<0,05)
0,888
Tablo 4.4: Nükleer yaygınlık ve Nükleer şiddet Kruskal-Wallis çoklu
karşılaştırma testi sonuçları
Grupların sitoplazmik boyanma ve şiddetleri arasında ise istatistiksel olarak anlamlı
bir boyanma farkı izlenmemiştir [Sitoplazmik boyanma yaygınlığı p: 0,461; p>0,05 ve
sitoplazmik boyanma şiddeti p: 0,085; p>0,05].
4.3.1.2: c-Myc:
12 SBT vakasının 3’ünde tümör hücrelerinin 25% kadarında, 1 vakada yaklaşık
50%’ sinde nükleer boyanma görülmüştür [yaygınlık-ortanca: 0 (0-2)]. Boyanma şiddeti
3 vakada orta şiddete, 1 vakada hafif dir [şiddet-ortanca: 0 (0-2)]. Sitoplazmik boyanma
1 vakada 75% oranında, diğer 11 vakada tümör hücrelerinin 75%’inden fazla hücrede
saptanmıştır [yaygınlık-ortanca: 4 (3-4)]. Sitoplazmik boyanma şiddeti vakaların
yarısında orta şiddetli, diğer yarısında ise şiddetli boyanma şeklinde izlenmiştir [şiddetortanca: 3 (2-3)] (Tablo 4.5)
Seröz Adenokarsinomlardaki boyanmaya gelince, SAK vakalarının hiçbirinde nükleer
boyanma görülmemiştir [yaygınlık-ortanca: 0 (0-0); şiddet-ortanca: 0 (0-0)]. Vakaların
tamamında 75%’den fazla tümör hücresinde sitoplazmik boyanma görülmüş [yaygınlıkortanca: 4 (4-4)], 11 vakada sitoplazmik boyanma hafif şiddette izlenirken, 30 vakada
şiddetli sitoplazmik boyanma saptanmıştır [şiddet-ortanca: 3 (2-3)]. (Tablo 4.5)
Benign lezyonların 3’ünde nükleer boyanma izlenmemiş, 12 tanesinde hücrelerin
25%’inde nükleer boyanma görülmüş, 3 tanesinde hücrelerin 26-50% kadarında
boyanma saptanmış, yalnızca 1 vakada da hücrelerin 51-75%’inde nükleer boyanma
izlenmiştir [yaygınlık-ortanca: 1 (0-3)]. Nükleer boyanmanın izlendiği 16 vakanın 4
tanesinde hafif şiddette boyanma izlenirken, 12 tanesinde orta şiddette nükleer boyanma
saptanmıştır [şiddet-ortanca: 2 (0-2)].
Tüm vakalarda sitoplazmik boyanma görülmüş, 1 vakada yaklaşık 25% hücrede
boyanma saptanmış, 3 vakada 51-75% oranında boyanma görülmüş, 15 vakada da
hücrelerin 75%’inden fazlasında sitoplazmik boyanma elde edilmiştir [yaygınlıkortanca: 4 (1-4)]. Boyanma şiddetine gelince; 2 vakada hafif, 14 vakada orta şiddette ve
3 vakada da şiddetli sitoplazmik boyanma saptanmıştır [şiddet-ortanca: 2 (1-3)]. (Tablo
4.5)
SBT
c- Myc N y*
c- Myc N ş*
c- Myc S y*
c- Myc S ş*
0,42 +/-0,669
0,58 +/-0,900
3,92 +/-0,289
2,50 +/-0,522
0 (0-2)
0 (0-2)
4 (3-4)
3(2-3)
0,00 +/-0,000
0,00 +/-0,000
4,00 +/-0,000
2,73 +/-0,449
0 (0-0)
0 (0-0)
4 (4-4)
3 (2-3)
1,11 +/-0,772
1,47 +/-0,772
3,68 +/-0,749
2,05 +/-0,524
1 (0-3)
2 (0-2)
4 (1-4)
2 (1-3)
Ortalama +/-St.Dv.
SBT
Ortanca (Min-Max)
SAK
Ortalama +/-St.Dv.
SAK
Ortanca (Min-Max)
Benign
Ortalama +/-St.Dv.
Benign
Ortanca (Min-Max)
Tablo 4.5: c-Myc boyanma skorları
İstatistiksel olarak Kruskal-Wallis çoklu karşılaştırma testinde, nükleer
yaygınlıkları karşılaştırıldığında her üç grupta da nükleer yaygınlık ve şiddette anlamlı
fark gözlenmiş (p<0,05), sitoplazmik boyanma yaygınlıklarında anlamlı fark
görülmemiştir (p>0,05). Sitoplazmik şiddetleri karşılaştırıldığında benign lezyonlar ile
hem SBT, hem de SAK’lar arasında fark saptanmış (p<0,05), SBT’ler ile SAK’lar
arasında fark saptanmamıştır (p>0,05). (Tablo 4.6)
Fark SBT -SAK
Fark SAK- Benign
Fark SBT- Benign
Nükleer yaygınlık
0,006 (p<0,05)
0,000 (p<0,05)
0,000 (p<0,05)
Nükleer şiddet
0,006 (p<0,05)
0,000 (p<0,05)
0,000 (p<0,05)
Sitoplazmik yaygınlık
0,651
0,172
0,528
Sitoplazmik şiddet
0,180
0,000 (p<0,05)
0,045 (p<0,05)
Tablo 4.6: Nükleer yaygınlık, Nükleer şiddet, Sitoplazmik yaygınlık ve
Sitoplazmik şiddet Kruskal-Wallis çoklu karşılaştırma testi sonuçları.
4.3.1.3. c-Jun:
c-Jun ile SBT’lerin 4 tanesinde nükleer boyanma gözlenmiştir. 3 vakada izlenen
nükleer boyanma hafif şiddete ve tümör hücrelerinin 25% kadarında gözlenirken, 1
vakada orta şiddette ve tümör hücrelerinin 26-50%’sinde görülmüştür [yaygınlıkortanca: 0 (0-2); şiddet-ortanca: 0 (0-2)]. Sitoplazmik boyanmalarına gelince; 1 vakada
26-50%’sinde, 3 vakada 51-75%’inde ve 9 vakada da tümör hücrelerinin 75%’inden
fazlasında sitoplazmik boyanma saptanmıştır [yaygınlık-ortanca: 4 (2-4)]. Sitoplazmik
boyanma 1 vakada hafif şiddette, 6 vakada orta şiddette ve 5 vakada ise şiddetli
boyanma izlenmiştir [şiddet-ortanca: 2 (1-3)]. (Tablo 4.7)
SAK’ların 7 tanesinde hafif şiddette nükleer boyanma görülmüş [şiddet-ortanca: 0 (01)], bu boyanma tümör hücrelerinin yaklaşık 25%’inde izlenmiştir [yaygınlık-ortanca: 0
(0-1)]. Vakaların 2 tanesinde sitoplazmik boyanma tümör hücrelerinin 51-75%’inde
izlenirken, diğer 39 SAK vakasında yaygın, 75%’in üzerinde sitoplazmik boyanma
saptanmıştır [yaygınlık-ortanca: 4 (3-4)]. Boyanma şiddetine gelince yaygınlığın 5175% oranında izlendiği 2 vakada hafif şiddette boyanma gözlenmiş, 15 vakada orta
şiddette boyanma saptanırken, 24 vakada da şiddetli sitoplazmik boyanma izlenmiştir
[şiddet-ortanca: 3 (1-3)]. (Tablo 4.7)
Benign grupta 11 vakada nükleer boyanma gözlenmemiştir. 6 vakada 25%, 2 vakada
26-50% oranında hücrede gürülmüştür [yaygınlık-ortanca: 0 (0-2)]. 5 vakada hafif, 3
vakada ise orta şiddette boyanma gözlenmiştir [şiddet-ortanca: 0 (0-2)]. 2 vakada 2650%, 5 vakada 51-75% ve 12 vakada ise hücrelerin 75%’inden fazlasında sitoplazmik
boyanma gözlenmiştir [yaygınlık-ortanca: 4 (2-4)]. 3 vakada hafif, 4 vakada orta ve 12
vakada şiddetli sitoplazmik boyanma görülmüştür [şiddet-ortanca: 3 (1-3)]. (Tablo 4.7)
SBT
c- Jun N y*
c- Jun N ş*
c- Jun S y*
c- Jun S ş*
0,42 +/-0,669
0,42 +/-0,669
3,67 +/-0,651
2,33 +/-0,651
0 (0-2)
0 (0-2)
4 (2-4)
2 (1-3)
0,17 +/-0,381
0,17 +/-0,381
3,95 +/-0,218
2,54 +/-0,596
0 (0-1)
0 (0-1)
4 (3-4)
3 (1-3)
0,53 +/-0,697
0,58 +/-0,769
3,53 +/-0,697
2,47 +/-0,772
0 (0-2)
0 (0-2)
4 (2-4)
3 (1-3)
Ortalama +/-St.Dv.
SBT
Ortanca (Min-Max)
SAK
Ortalama +/-St.Dv.
SAK
Ortanca (Min-Max)
Benign
Ortalama +/-St.Dv.
Benign
Ortanca (Min-Max)
Tablo 4.7: c-Jun boyanma skorları
İstatistiksel olarak yalnızca sitoplazmik boyanma yaygınlığında anlamlı fark izlenmiş
(p<0,05), nükleer boyanma yaygınlığı, şiddeti ve sitoplazmik boyanma şiddeti arasında
fark gözlenmemiştir (p>0,05). Sitoplazmik yaygınlık farkı SAK’lar ve benign grup
arasında görülmüş, SAK’lar ve SBT’ler arasında belirgin bir farklılık saptanmamıştır
(Tablo 4.8).
Sitoplazmik yaygınlık
Fark SBT-SAK
Fark SAK- Benign
Fark SBT- Benign
0,252
0,036 (p<0,05)
0,562
Tablo 4.8: Sitoplazmik yaygınlık Kruskal-Wallis çoklu karşılaştırma testi sonuçları
4.3.1.4. p 38:
p 38 ile SBT’lerden 2 vakada 25% kadar hücrede, 7 vakada 26-50% oranında
hücrede ve 3 vakada 51-75% oranına hücrede nükleer boyanma elde edilmiştir
[yaygınlık-ortanca: 2 (1-3)]. Yalnızca 1 vakada orta şiddette nükleer boyanma tespit
edilirken, diğer 11 vakada hafif şiddette boyanma gözlenmiştir [şiddet-ortanca: 1 (1-2)].
İki vakada 25% oranında hücrede sitoplazmik boyanma izlenirken, 7 vakada 26-50%
oranında boyanma gözlenmiş, 3 vakada da 51-75% oranında sitoplazmik boyanma
görülmüştür [yaygınlık-ortanca: 2 (1-3)]. Sitoplazmik boyanma tüm vakalarda hafif
şiddettedir [şiddet-ortanca: 1 (1-1)]. (Tablo 4.9)
Seröz Adenokarsinomlarda 9 vakada nükleer boyanma gözlenmemiş, 2 vakada
26-50% oranında hücrede hafif şiddette nükleer boyanma, geri kalan 30 vakada ise
fokal, 25% oranında hücrede hafif şiddette boyanma gözlenmiştir [yaygınlık-ortanca: 1
(0-2)], [şiddet-ortanca: 1 (0-1)]. 1 vakada sitoplazmik boyanma izlenmezken, 5 vakada
25%, 14 vakada 51-75% ve 21 vakada 26-50% oranında hücrede sitoplazmik boyanma
izlenmiştir [yaygınlık-ortanca: 2 (0-3)]. Boyanma şiddetine gelince, 1 vakada hiç
boyanma izlenmemiş, 28 vakada hafif şiddette ve 12 vakada ise orta şiddette nükleer
boyanma elde edilmiştir [şiddet-ortanca: 1 (0-2)]. (Tablo 4.9)
Benign lezyonlardan 1 vakada nükleer boyanma gözlenmemiştir. 7 vakada 25%,
10 vakada 26-50%’ye varan hücrede boyanma görülmüştür. 1 vakada 51-75% oranında
hücrede nükleer boyanma dikkati çekmiştir [yaygınlık-ortanca: 2 (0-3)]. Boyanmanın
izlediği 18 vakada hafif şiddette nükleer boyanma elde edilmiştir [şiddet-ortanca: 1 (01)]. Yalnızca bir vakada 51-75% oranında hücrede sitoplazmik boyanma görülmüş, 7
vakada 26-50% oranında, 11 vakada 25% kadar hücrede sitoplazmik boyanma
saptanmıştır [yaygınlık-ortanca: 1 (1-3)]. Sitoplazmik boyanma 1 vakada orta şiddette,
18 vakada hafif şiddettedir [şiddet-ortanca: 1 (1-2)]. (Tablo 4.9)
SBT
p38 N y*
p38 N ş*
p38 S y*
p38 S ş*
2,08 +/-0,669
1,08 +/-0,289
2,08 +/-0,669
1,00 +/-0,000
2 (1-3)
1 (1-2)
2 (1-3)
1 (1-1)
0,83 +/-0,495
0,78 +/-0,419
2,17 +/-0,738
1,27 +/-0,501
1 (0-2)
1 (0-1)
2 (0-3)
1 (0-2)
1,58 +/-0,692
1,00 +/-0,333
1,47 +/-0,612
1,05 +/-0,229
2 (0-3)
1 (0-1)
1 (1-3)
1 (1-2)
Ortalama +/-St.Dv.
SBT
Ortanca (Min-Max)
SAK
Ortalama +/-St.Dv.
SAK
Ortanca (Min-Max)
Benign
Ortalama +/-St.Dv.
Benign
Ortanca (Min-Max)
Tablo 4.9: p38 boyanma skorları:
İstatistiksel olarak
Kruskal-Wallis çoklu
karşılaştırma testinde
nükleer
yaygınlıklar ve sitoplazmik yaygınlıklar arasında anlamlı fark gözlenmiş (p<0,05),
nükleer şiddet ve sitoplazmik boyanma şiddetleri arasında fark saptanmamıştır (p>0,05).
Nükleer yaygınlık farkları SBT ile SAK vakaları arasında ve benign grup ile SAK
vakaları arasındadır. SBT ve benign grup arasında fark izlenmemiştir ( Tablo 4.10)
Sitoplazmik yaygınlık farklılığı ise benign grup ile SBT ve SAK vakaları arasında
izlenmiştir (Tablo 4.10).
Fark SBT-SAK
Fark SAK-Diğer
Fark SBT-Benign
Nükleer yaygınlık
0,000 (p<0,05)
0,000 (p<0,05)
0,065
Sitoplazmik yaygınlık
0,667
0,001 (p<0,05)
0,026 (p<0,05)
Tablo 4.10 : Nükleer ve sitoplazmik yaygınlık Kruskal-Wallis çoklu karşılaştırması
a
b
Resim 1. TMA ve Makroarray blokları, H.E. ve İHK boyalı lamlar
a
b
c
Resim 2. Benign Kistadenofibrom H.E. boyalı kesitler
a
b
c
Resim 3. Seöz Borderline Tümör H.E. kesitler
a
b
c
d
Resim 4. Seröz Adenokarsinom H.E. kesitler
a
b
c
d
e
f
Resim 5. c-fos boyanmaları. a&b. Benign seröz kistadenofibrom. c&d. SBT. e&f. SAK
e
a
b
c
d
f
Resim 6. c-myc boyanmaları. a&b. Benign seröz kistadenofibrom. c&d. SBT. e&f. SAK
a
b
c
d
e
f
Resim 7. c-jun boyanmaları. a&b. Benign seröz kistadenofibrom. c&d. SBT. e&f. SAK
a
b
c
d
e
f
Resim 8. p38 boyanmaları. a&b. Benign seröz kistadenofibrom. c&d. SBT. e&f. SAK
5. TARTIŞMA
Seröz karsinomlar over kanserlerinin en sık görülen ve en ölümcül olan
formudur. Over karsinomu gelişimindeki moleküler yolakları belirlemek yeni tanısal
yaklaşım ve tedavi yaklaşımlarını oluşturabilmek için önemlidir. Birçok moleküler
model oluşturulmasına karşın hala seröz karsinomların patogenezi tam olarak
anlaşılamamıştır.
Mikrosatellit instabilitesi ve DNA kopya sayısındaki değişiklikler (kromozomal
instabilite) tümör hücrelerindeki genetik instabiliteyi göstermektedir. Yapılan bir
çalışmada 69 mikrosatellit belirleyicisi SBT’lerde çalışılmış (69), SBT’lerde yüksek
dereceli karsinomlardakine benzer mikrosatellit instabilitesi ender olarak izlenmiştir.
Karşılaştırmalı genomik hibridizasyon ile kromozomal imbalans, SBT ve düşük dereceli
seröz karsinomlarda, yüksek dereceli adenokarsinomlardan belirgin olarak az
bulunmuştur (70-71). Bir başka çalışmada dijital PCR analizi ile artmış allelik imbalans
indeksinin SBT’lerden invaziv düşük dereceli seröz karsinomlara progresyonla
paralellik gösterdiği saptanmıştır (5). MYCL1 ve NOERY/ARH1 gibi tümör supresör
genler komşuluğundaki kromozom 1p ‘deki allelik imbalans SBT’lerde sıklıkla
gözlenmiştir (5, 72) Bu değişiklikler aynı zamanda komşu invaziv düşük dereceli seröz
karsinomlarda da izlenmiştir (5, 72) Yüksek-dansite oligonükleotid mikroarray ile
SBT’ler ve seröz karsinomların gen ekspresyon profilleri araştırılmıştır (71). Hücre
siklus regülatörü olan p21/WAF1’in SBT’lerin ve low grade tümörlerin çoğunlunda
eksprese olurken yüksek gradelilerde olmadığı saptanmıştır. Gilks ve arkadaşları (73)
mucin 10 (subtip B), kallikrein 6, B7 protein ve keratin 17’de farklılık saptamıştır.
Konvansiyonel yüksek dereceli tümörlerden belirgin olarak farklılık olduğu anlaşılmıştır
(74).
KRAS mutasyonu SBT’ lerde ilk olarak Mok ve arkadaşları tarafından
tanımlanmıştır (75). Son çalışmalarda KRAS/BRAF mutasyonlarının SBT ve düşük
gradeli SAK’ larda önemli olduğu sonucuna varılmıştır (80-83). Chung-Liang Ho ve
arkadaşlarının yaptığı çalışmada ise (76) 8 SBT’ lü hastada SBT komponenti ve komşu
kistadenom komponenti epitelinde KRAS ve BRAF mutasyonuna bakılmış, 4 SBT
kodon 12 aktive KRAS mutasyonu, 3 vaka ise kodon 599’da BRAF mutasyonu
göstermiştir. 1 vakada ise wild-type KRAS ve BRAF mutasyonu gözlenmiştir. SBT
komşuluğundaki kistadenom epitelinde de 86% oranında benzer mutasyonlar
saptanmıştır.
SBT’lerden
farklı
olarak
sitolojik
atipi
kistadenom
epitelinde
izlenmemiştir. Bu çalışma ile KRAS ve BRAF’ın tümör ilerlemesinde henüz morfolojik
bulgular ortaya çıkmadan çok erken basamaklarda rol oynadığı anlaşılmaktadır. Buna
göre bazı kistadenomların SBT’lerin prekürsör lezyonu olduğu anlaşılmaktadır. SBT’ler
ile izlenen kistadenomlarda KRAS ve BRAF mutasyonu, SBT bulunmayanlardan
belirgin olarak daha fazla oranda izlenmektedir. SBT’lerden çok daha fazla oranda
izlenen seröz kistadenomların yalnızca bir kısmında neoplastik potansiyel bulunduğu ve
SBT’lere
progresyon
gösterdiği
RAS/RAF/MEK/MAPK
yolağındaki
düşünülebilir.
p38’in
nükleer
Bizim
çalışmamız
ekpspresyonunun
da
benign
lezyonlarda ve SBT’lerde SAK’lardan farklı olarak yüksek olduğu ortaya koymuştur.
Buna göre bazı benign seröz kistadenofibromların SBT’lerin prekürsör lezyonu
olabileceği
düşünülebilir.
Yine
p38
aktivasyonun
SBT’lerin
benign
kistadenofibromlardan gelişiminde henüz morfolojik bulgular ortaya çıkmadan yer
aldığı, seröz kistadenomların yalnızca bir ksımında neoplastik potansiyelin bulunduğu
ve bunların SBT’lere ilerlediği düşünülebilir.
Yüksek
dereceli
seröz
karsinomlarda
ise
KRAS/BRAF
mutasyonu
gözlenmemektedir. Bu nedenle yüksek gradeli karsinomlarda RAS/RAF/MEK/MAPK
sinyal yolağından farklı bir yolak söz konusudur. Yüksek dereceli karsinomların
50%’sinden fazlasında p53 mutasyonu izlenmektedir. SBT’lerde ise mutant p53 çok
ender olarak izlenmektedir (77-78).
KRAS/BRAF mutasyonları sonucu, KRAS/BRAF/MEK/MAPK (ekstrasellüler
sinyal regüle kinaz) sinyal yolağı aktive olmaktadır (84). Deneysel hücre kültürlerinde
bu gendeki mutasyonların onkojenik olduğu, birçok hedef molekül ile tümör gelişiminde
etkili olduğu düşünülmektedir. Konvansiyonel yüksek dereceli seröz karsinomlarda da
aktive MAPK veya ekstrasellüler sinyal regüle kinaz aktivasyonu gözlenebilir. Ancak
bu aktivasyon BRAF ve KRAS mutasyonlarından bağımsız epigenetik mekanizmalar ile
olabileceği savunulmaktadır. Çünkü yüksek dereceli seröz karsinomlarda BRAF ve
KRAS mutasyonları çok ender olarak izlenmiştir (84-85). Bu çalışma ile KRAS ve
BRAF mutasyonu gösteren SBT’lerde bu mutasyonlar sonucu aktive olan MAPK’lardan
p38 proteininin SBT’lerde SAK’lardan farklı olarak nükleer ekspresyon artışı gösterdiği
saptanmıştır. Bizim çalışmamızda SAK vakalarının SBT’lere oranla çok daha az p38
nükleer ekspresyon gösterdiği anlaşılmıştır. Buradan yola çıkarak SBT gelişiminde
KRAS ve BRAF mutasyonları ile aktive olan MAPK ailesinden p38 MAPK’ın aktive
olduğu düşünülebilir.
Seröz karsinomların bir varyantı olarak kabul edilen mikropapiller seröz
karsinomların (MPSC) kendine özgü histopatolojik ve klinik bulguları mevcuttur. Çoğu
MPSC’lar non-invazivdirler ve genellikle seröz borderline tümörler ile birliktelik
gösterirler. Bu tümörlerin benign proliferatif tümörden (SBT veya atipik proliferatif
seröz tümör) non-invaziv carsinom (non-invaziv MSC) ve dereceli invaziv karsinoma
(invaziv MPSC) ilerledikleri düşünülmektedir. MPSCların daha yavaş klinik gidiş
sergiledikleri
bildirilmektedir
(5).
MPSCların
genel
popülasyondaki
sıklığı
bilinmemekle birlikte, yapılan bir çalışmada (86) tüm seröz karsinomların 20-25 %’inin
oluşturduğu bildirilmektedir. İnvaziv MPSC’ lar yüksek dereceli konvansiyonel seröz
karsinomların aksine daha yavaş bir gelişim göstermektedirler. Gad Singer ve
arkadaşlarının yaptığı çalışmada, (5) 108 over karsinomlu hastada (24 SBT, 39 MPSC,
22 İnvaziv MPSC ve 23 konvansiyonel over karsinomu) kodon 12 veya 13’teki KRAS
mutasyonunu SBT lerde 50% (12/24), MPSClarda 36% (14/39) ve invaziv MPSClarda
ise 54% (12/22) olarak saptamışlar. Konvansiyonel over karsinomlarının hiçbirinde
KRAS mutasyonu izlenmemiştir. (0/23) Allelik imbalansları da araştırılmış, allelik
inbalans indeksinin SBT’ lerden non-invaziv ve invaziv MPSC’ lara doğru arttığı
saptanmış, Konvansiyonel seröz karsinomlarda ise erken yüksek dereceli (0,8 cmden
küçük tek overle sınırlı) tümörlerde bile yüksek allelik inbalans saptanmıştır. Buna göre
invaziv MPSC olarak adlandırılan düşük dereceli seröz karsinomlar ve bunun prekürsör
lezyonları (SBT ve non-invaziv MPSC) ile konvansiyonel yüksek dereceli seröz
karsinomlar
birbirinden
çok
farklı
ve
karakteristik
moleküler
değişiklikler
sergilemektedirler. Bu çalışmada KRAS mutasyonu invaziv MPSC’ ların neredeyse
yarısında saptanırken konvansiyonel karsinomlarda izlenmemiştir. KRAS sinyal
yolağının bu tümörlerde önemli bir rol oynadığı anlaşılmaktadır. Daha önce yapılan
değişik çalışmalarda (87) SBT tümörlerde KRAS mutasyonu saptanmış, karsinomlarda
izlenmediği için ilişkisiz olduğu savunulmaktadır (75). Kromozom 5q ve 1p deki
değişiklikler yalnızca MPSC’ larda değil, SBTlerde de gösterilmesi morfolojik
değişiklikler öncesi genetik değişikliklerin yer aldığını göstermektedir. Bilateral MPSC’
larda farklı KRAS mutasyon paterni veya allelik inbalans gösterilmesi, aynı erken
lezyondan farklı progresyonu ekarte ettirmemekle birlikte, bunların bağımsız geliştiğini
desteklemektedir(88). Konvansiyonel seröz karsinomlarda tümör boyutu ne olursa
olsun, morfolojik tanınabilir bir prekürsör lezyona rastlanmamaktadır. Bizim
çalışmamızda düşük dereceli seröz adenokarsinomlar yer almadığı için p38
aktivasyonunun bu tümörlerdeki yeri bilinmemektedir. Yalnızca düşük dereceli seröz
adenokarsinomların prekürsörü olarak kabul edilen SBT’lerde p38 aktivasyonu
gösterilmiştir. Düşük dereceli seröz karsinomlarda p38’in geniş vaka serilerinde
gösterilmesi sonucu
ancak
bu
tümörlerin
SBT’lerden geliştiği spekülasyonu
desteklenebilcektir.
Bilindiği gibi over seröz karsinomların gelişiminde iki farklı yolaktan
bahsedilmektedir. İlk yolakta, invaziv düşük dereceli seröz tümörlerin adenomakarsinoma sekansına benzer şekilde non-invaziv SBT’lerden geliştiği düşünülmektedir.
Prekürsör lezyonların da seçilebildiği savunulmaktadır. Detaylı histopatolojik analizler
sonucunda, SBT’lerin tümör progresyonunda farklı evrelerde iki non-invaziv tümörden
oluştuğunu göstermektedir. Bunlar atipik proliferatif seröz tümör ve in-situ düşük
dereceli seröz karsinoma olarak da tanımlanan non-invaziv mikropapiller seröz
karsinomlardır. Benign proliferatif lezyon olan atipik proliferatif seröz tümörden
intraepitelyal düşük dereceli seröz karsinoma ve bundan da düşük dereceli invaziv seröz
karsinom geliştiği düşünülmektedir. SBT’lerin yüksek dereceli seröz karsinomlar olarak
nüks ettiğini bildiren çalışmalar mevcuttur (89). Bunun yanında Ortiz ve arkadaşları
SBT ve seröz karsinom olarak nüks eden hastalarda p53 ve KRAS gen mutasyonlarını
araştırdığı çalışmada, aynı hastada SBT’ ler ve seröz karsinomların moleküler genetik
olarak farklı olduğunu göstermiştir (74).
Yukarıdaki çalışmalarda da belirtildiği gibi farklı iki yolaktan geliştiği moleküler
olarak ortaya konan SBT’ ler ve SAK’ larda bu çalışma ile RAS/RAF/MEK/MAPK
yolağı SBT’ ler ve SAK’ lar arasında farklı ekspresyon paterni ortaya koyduğu
immünhistokimyasal olarak gösterilmiştir.
Bu çalışma ile RAS/RAF/MEK/MAPK yolağı aktivasyonu ile aktive olan
transkripsiyon faktörlerinden c-fos’un; SBT’lerde nükleer boyanma şiddeti [şiddetortanca:1,00 (1-2)] ve yaygınlığı [yaygınlık-ortanca: 2,00 (1-3)] ile benign lezyonlardaki
boyanma şiddet [şiddet-ortanca: 1 (0-3)] ve yaygınlığının [yaygınlık-ortanca: 2 (0-4)];
SAK’lardaki nükleer boyanma şiddeti [şiddet-ortanca: 0 (0-1)] ve yaygınlığından
[yaygınlık-ortanca: 0 (0-2)] yüksek olduğu bulunmuştur. Nükleer boyanma ve şiddetleri
arasında SBT’ler ve benign lezyonlarda SAK’lara oranla istatistiksel olarak anlamlı fark
bulunmuştur (p<0,05). SBT’ler ve benign lezyonlar arasında ise nükleer boyanma
şiddeti ve yaygınlık açısından anlamlı bir fark bulunmamıştır (p>0,05). Sitoplazmik
boyanma şiddet ve aygınlıkları arasında ise her üç grup arasında istatistiksel bir fark
saptanmamıştır (p>0,05). Buna göre benign kistadenofibromlar ve SBT’lerin
gelişiminde nükleer transkripsiyon faktörü olan c-fos’un aktive olduğu düşünülebilir.
Yine seröz kistadenomlarda ve SBT’lerde benzer ekspresyon paterni göstermeleri daha
önce de belirtilen seröz kistadenomlardan SBT’lerin
gelişebildiği düşüncesini
destekleyebilecektir.
c-myc boyanmasına bakıldığında, benign lezyonlarda izlenen nükleer boyanma
şiddeti [şiddet-ortanca: 2 (0-2)] ve yaygınlığı [yaygınlık-ortanca: 1 (0-3)] yüksek
bulunmuş, SBT’lerdeki nükleer boyanma şiddeti [şiddet-ortanca: 0 (0-2)] yaygınlığı
benign lezyonlara oranla daha düşük bulunmuştur. SAK’ların hiçbirinde nükleer
boyanma izlenmemiştir. Buna göre her üç grup arasında istatistiksel olaak anlamlı bir
fark olduğu anlaşılmıştır (p<0,05). Sitoplazmik boyanma yaygınlıkları arasında her üç
grupta anlamlı bir fark izlenmemiştir. Sitoplazmik boyanma şiddetinin SAK’larda ve
SBT’lerde benign gruba oranla yüksek olduğu anlaşılmıştır.
Silverberg SG ve ark. yaptığı 44 vakalık bir çalışmada (Seröz ve müsinöz
kistadenomlar, borderline tümör ve invaziv
karsinomlar) c-myc ekspresyonu
immünhistokimyasal olarak incelenmiş, buna göre seröz ve müsinöz kistadenomlarda
yüksek nükleer ekspresyon saptanmış, invaziv tümörlerde ise sitoplazmik boyanma elde
edilmiş. Borderline tümörlerde ise intermediate paternde bir ekspresyon profili
saptanmıştır (90). Buna göre bizim çalışmamızda da c-myc’ in benign lezyonlardan
malign lezyonlara doğru gelişiminde nükleer ekspresyonun azaldığı ve sitoplazmik
ekspresyonun SBT’ ler ve SAK’ larda benign gruba oranla belirgin olarak daha fazla
gözlendiği ortaya konmuştur.
c-jun ile SBT’lerin 4’ünde, SAK vakalarının 7 tanesinde ve benign lezyonların
ise yalnızca 8 tanesinde nükleer boyanma saptanmıştır. İstatistiksel olaral her üç grupta
spesifik nükleer boyanma şiddeti ve yaygınlığı arasında anlamlı bir boyanma
bulunmamıştır. Sitoplazmik boyanma her üç gruptaki vakalarda da izlenmekle birlikte,
istatistiksel olarak SAK ve benign grup arasında sitoplazmik boyanma yaygınlığında
anlamlı bir fark elde edilmiş, SAK’larda ve SBT’lerde sitoplazmik boyanmalar arasında
da anlamlı bir fark gözlenmemiştir.
Wong AS ve ark. hücre kültürleri modelinde ovarian karsinogeneziste etkili
protein kinaz ekspresyon paternlerini Western blothing yöntemi ile araştırmıştır. Bu
çalışmada neoplastik over hücrelerinde normal over yüzey epiteline oranla p38 MAPK,
MEK-6, Casein kinase II, Cyclin dependent kinase ekspresyonunun artmış, c GMPdependent
kinase ekspresyonunun azalmış
ve ERK1/ERK2
düzeylerinin
ise
değişmediğini ortaya koymuşlardır (91). Bu çalışmada MEK6- p38 MAPK- CK II ve
PI3K yolaklarının over karsinogenezinde, tümör progresyonunda etkili olduğu
savunulmuştur.
Bizim çalışmamızda da p38 MAPK aktivasyonunun SBT’lerde SAK’lara oranla
yüksek olduğu ortaya çıkmıştır. SBT’lerde p38 nükleer yaygınlığı [yaygınlık-ortanca: 2
(1-3)] ile benign lezyonlardaki p38 boyanma yaygınlığı [yaygınlık-ortanca: 1 (1-3)] ;
SAK vaklarında izlenen nükleer boyanma yaygınlığından [yaygınlık-ortanca: 1 (0-2)]
yüksek bulunmuş, bu fark istatistiksel olarak da anlamlı çıkmıştır. Nükleer boyanma
şiddetleri arasıda ise üç grup arasında anlamlı bir fark elde edilmemiştir (p>0,05).
Sitoplazmik yaygınlık SBT’ler ve SAK’larda benign lezyonlara oranla daha fazla
saptanmış ve bu farkın istatistiksel olarak da anlamlı olduğu ortaya konmuştur.
Bizim çalışmamızda p38 nükleer ekspreyonunun benign seröz kistadenom
epitelinde SBT’lerdekine benzer şekilde artmış oranda saptanması, Chung-Liang Ho ve
ark. yaptığı çalışmada öne sürdükleri, bazı kistadenomların SBT’lerin prekürsör lezyonu
olduğu teorisini destekler nitelikte bulunmuştur (76).
Gingival fibroblastlar üzerinde yapılan bir çalışmada; trombin ile aktive edilen
fibroblastlarda RAS sinyal yolağının hızla aktive olduğu ve p38 ve CREB/ATF1
fosforilasyonunun gerçekleştiği ortaya konmuştur. Bundan sonra c-myc, c-fos, c-jun
ekspresyonları değişen sürelerde arttığını bildirilmektedir. Bu çalışmada inflamasyon
sürecinde p38 ve buna bağlı olarak transkripsiyon faktörleri olan c-myc, c-fos, c-jun
aktivasyonu tanımlanmıştır (92).
Buna göre bu çalışma ile SBT’lerde moleküler olarak mutasyonu gösterilen
RAS/RAF/MEK/MAPK yolağında p38 MAPK yolağı üzerinden fonksiyon gördüğü
savunulabilmektedir. Bildiğimiz gibi MAPK’lar p38 MAPK ailesi, ERK ailesi ve JNK
ailesi olmak üzere üç ana gruba ayrılmaktadır. Bu çalışmada JNK ailesinin nükleer
transkripsiyon faktörü olan c-jun ile gerek benign kisadenomlarda, gerek SBT’lerde ve
gerekse SAK’larda nükleer boyanma izlenmemiştir. Bu çalışmada ayrıca SBT’lerde p38
aktivasyonu ile c-myc ve c-fos’un ekspresyonunun arttığı savunulabilmektedir. c-myc
ve c-fos gibi bir çok uyarı sistemi ile aktive olan transkripsiyon faktörlerini direk p38
aktivasyonu ile ilişkilendirmek mümkün olamasa da benign seröz kistadenomlarda ve
SBT’lerde SAK’lardan farklı olarak belirgin nükleer ekspresyon artışı kanıtlanmıştır.
Bu çalışma son yıllardaki epitelyal over tümörlerini Tip I ve Tip II olmak üzere iki
ana kategoriye ayıran ve bunların farklı moleküler yolaktan geliştiğini savunan teoriyi
destekler nitelikte bulunmuştur. Bu teoride düşük dereceli seröz adenokarsinomların
SBT’lerden geliştiği savunulmakta ve konvansiyonel SAK’lardan farklı moleküler
değişiklikler göstererek bunlar ile ilişkisiz olduğu savunulmaktadır. Bizim çalışmamızda
da SBT’lerde p38 MAPK yolağının aktive olduğu saptanmıştır. SAK’larda ise belirgin
bir p38 nükleer ekspresyon artışı izlenmemiştir. Ancak SBT’lerde nükleer ekspresyon
artışı saptadığımız p38’in çalışmamıza dahil edemediğimiz düşük dereceli seröz
adenokarsinomlardaki ekspresyon paterni bilinmemektedir. Düşük dereceli seröz
adenokarsinomların da yer aldığı daha geniş vaka serilerini içeren çalışmalar ile bu
karsinogenez aşamalarının araştırılması gerekmektedir. Geniş vaka serilerinde
SAK’lardan farklı olarak, düşük dereceli seröz adenokarsinomlarda da benzer p38
nükleer ekspresyon artışı saptandığı takdirde bu teoriyi net olarak ortaya koymak
mümkün olabilecektir.
SBT’lerde p38, c-myc ve c-fos’un nükleer ekspresyon farklılığı göstermesi pratik
hayatta, bu tümörlerin SAK’lardan ayrılamadığı durumlarda kullanılabilir görünse de
belirtildiği gibi bu proteinlerin düşük dereceli seröz adenokarsinomlardaki boyanma
paterni bilinmemektedir. Bu nedenle ayrımda güçlük yaşanabilecek düşük dereceli seröz
adenokarsinomlar ile SBT’lerin benzer ekspresyon paterni gösterip göstermediğinin
geniş vaka serilerinde gösterilmesi gerekmektedir.
Bu çalışma moleküler olarak daha önce bir çok çalışma ile gösterilen ve
farklılıkları saptanan SBT’ler ve SAK’larda MAPK aktivasyonunu ve buna bağlı
olabilecek farklı transkripsiyon faktörlerini araştıran ilk immünhistokimyasal çalışma
olması nedeniyle de büyük önem taşımaktadır.
6. SONUÇLAR:
•
SBT vakalarının yaş ortalaması 44,17, SAK vakalarının yaş ortalaması 57,49
bulunmuştur.
•
Tümör lokalizasyonları arasında SBT, SAK ve Benign grup arasında anlamlı bir
fark saptanmamıştır.
•
Üçlü gradeleme sistemine göre; 41 Seröz Adenokarsinom vakasının 8’i grade II,
33 vaka ise grade III Seröz Adenokarsinom olduğu anlaşılmıştır.
•
p38’in nükleer boyanma yaygınlığı SBT vakaları ve SAK vakaları arasında
belirgin olarak yüksek bulunmuştur.
•
p38 SBT’ler ve benign lezyonlarda yüksek nükleer boyanma oranı gsterirken
SAK’larda bu düşük bulunmuştur.
•
c-fos’un nükleer boyanma yaygınlık ve şiddeti SBT’ler ve benign lezyonlarda
SAK’lara oranla daha fazladır.
•
c-fos’un nükleer boyanma yaygınlığı ve şiddeti SBT’ler ve SAK’lar arasında
istatistiksel olarak farklı bulunmuştur.
•
c-myc nükleer boyanma yaygınlığı ve şiddetinin her üç grupta farlılık gösterdiği
saptanmıştır.
•
c-myc nükleer ekspresyonunun benign lezyonlardan SAK vakalarına doğru
gelişiminde azaldığı saptanmıştır.
•
c-myc’in sitoplazmik ekspresyonunun SBT’ler ve SAK’larda benign gruba
oranla belirgin olarak daha fazla gözlendiği ortaya konmuştur.
•
p38, c-myc ve c-fos nükleer ekspresyon farklılıkları morfolojik olarak ayrım
güçlüğü yaşandığı durumlarda SBT’ ler ile SAK’ ların ayrımında rutin olarak
kullanılabileceği düşünülmekle birlikte bunun düşük dereceli seröz karsinomları da
içeren daha geniş vaka serisinde incelenerek araştırılması gerekmektedir.
7. ÖZET:
Overin
Seröz
Adenokarsinomları
ve
Seröz
Borderline
Tümörlerinde
RAS/RAF/MEK/MAPK Yolağındaki Moleküler Değişikliklerin İmmünhistokimyasal
Olarak Araştırılması
Giriş: SBT’ler ve SAK’ların etyopatogenezinde son yıllarda iki farklı yolaktan
bahsedilmektedir. SBT’ler ve bunlardan geliştiği düşünülen low grade SAK’larda
MAPKinaz yolağının aktive olduğu, konvansiyonel SAK’ların ise bunlardan farklı
genetik mekanizmalar ile yüzey epitelinden veya bir inklüzyon kistinden de-novo ortaya
çıktığı savunulmaktadır.
Bu çalışmada farklı moleküler değişiklikler gösterdiği bildirilen SBT’ler ve SAK’lar
arasında p38 MAPK yolağının ve c-myc, c-fos ve c-jun gibi transkripsiyon faktörlerinin
aktivasyon profilinin araştırılması amaçlanmıştır.
Materyal ve Metod: Bu çalışmada 2000-2007 yılları arasında, Ankara Üniversitesi
Tıp Fakültesi Patoloji Anabilim Dalı’nda raporlanmış ooferektomi materyalleri
incelenmiştir. 12 Borderline Seröz Tümör (BST), 41 Seröz Adenokarsinom (SAK) ve
Seröz Papiller Kistadenofibrom, Morgagni Kisti, Seröz Kistadenom ve Basit Seröz
Kistlerinden oluşan 19 vaka ile birlikte, toplam 72 vaka üzerinde çalışılmıştır.
‘Mikroarrayer’ ile tümörlü bloklardan 1,5 mm uzun çapında doku silindirleri çıkartılarak
ve her dokudan 3 kor alınarak 2 adet ‘TMA’ bloğu hazırlanmış, benign lezyonlar,
SBT’ler ve bazı SAK vakalarından ise 3 mm çaplı 2’şer kor alınarak 7 adet makroarray
bloğu hazırlanmıştır. Toplam 9 bloktan elde edilen kesitlere immünhistokimyasal olarak
p38, c-myc, c-fos ve c-jun antikorları uygulanmıştır.
Bulgular: c-fos’un SBT’ler ve benign grupta nükleer boyanma yaygınlığı ve
şiddetinin SAK vakalarına oranla yüksek olduğu izlenmiştir. c-myc ile SAK vakalarının
hiçbirinde spesifik nükleer boyanma gözlenmemiştir. Benign lezyonlar ve SBT’lerde
nükleer c-myc ekspresyonu izlenmiş, bunun da benign lezyonlardan SBT’lere doğru
azalan
oranlarda
bulunduğu
saptanmıştır.
c-myc
sitoplazmik
ekspresyonuna
bakıldığında, SBT ve SAK’larda benign gruba oranla sitoplazmik boyanma şiddetinin
yüksek olduğu anlaşılmıştır. c-jun ile bu tümörlerde spesifik nükleer boyanmaları
arasında anlamlı bir fark elde edilememiştir. p38 boyanma spesifik nükleer boyanmanın
SBT’ler ve benign grupta yüksek olduğu, SAK vakalarında ise nükleer boyanmanın
anlamlı olarak daha az izlendiği saptanmıştır.
Sonuç: p38, c-myc ve c-fos nükleer ekspresyonları SBT’ler ve SAK’larda
farklılık göstermektedir. Tanı güçlüğü yaşanan olgularda bu markerların nükleer
ekspresyon farklılıklarından faydalanılması mümkündür. SBT’ler ve SAK’ların farklı
moleküler yolaklardan geliştiği anlaşılmaktadır. Ancak bu yolakta rol oynayan
moleküleri immünhistokimyasal olarak araştıran ilk çalışma olması nedeniyle bu
verilerin özellikle düşük dereceli seröz adenokarsinomların da yer aldığı daha geniş
vaka serilerinde de gösterilmesi gerekmektedir.
Anahtar sözcükler: Seröz borderline tümör, Seröz adenokarsinom, MAPK sinyal
yolağı, immünhistokimya.
8. SUMMARY:
İmmunohistochemical Detection of RAS/RAF/MEK/MAPK Pathway
on Serous Adenocarcinoma and Serous Borderline Tumors of Ovary.
İntroduction: Recent years, the authors propose a dualistic model for ovarian
serous carcinogenesis. In this model, one pathway involves a stepwise progression
from SBT to low grade serous carcinoma by molecular changes in MAPKinase
molecular pathway, and the other pathway is characterized by rapid progression
from the ovarian surface epithelium or inclusion cysts to a conventional (high-grade)
serous carcinoma.
In this study we aimed that, to determine the difference in p38 MAPK
pathway, and the transcription factors, c-myc, c-fos, c-jun between SBTs and SACs.
Materials and Methods: In this study, we examined, 12 SBT, 41 SAC and 19
cases of benign group that composed of serous papillary cystadenofibroma, serous
cystadenoma, Morgagni cysts that were diagnosed at Ankara University Pathology
Department in years between 2000-2007. 2 new tissue microarray blocks were
obtained by taking tissue cylinders 1,5 mm in diameter with a microarrayer. And
each case was represented with 3 tissue cylinders.
7 macroarray blocks were
obtained by tissue taking cylinders 3 mm in diameter and each case was represented
with 2 tissue cylinders. All cases were shown in 9 blocks. These blocks were stained
with p38, c-myc, c-fos ve c-jun.
Results: The intensity and diffusiveness of the nuclear staining of c-fos in SBT
and benign group was hidher than SACs. By c-myc, there were no nuclear staining
in SACs. In benign group and SBTs there were nuclear staining with c-myc and
intensity of nuclear staining was stronger in benign group than SBTs. Cytoplasmic
staining of c-myc in SBTs and SACs was stronger than benign group. By c-jun there
were no different staining between 3 groups. In SBTs and benign group, nuclear p38
staining was higher than SACs.
Conclusion: The nuclear stainin of p38, c-myc and c-fos is different between
SBTs and SACs. This may be helpful in the cases, that we have problems in the
differentiation of SACs and SBTs. However this is the first immunohistochemical
study that aimed to detemine the difference of MAPK pathway in SBTs and SACs.
So there must be more studies in large series, including low grade serous carcinoma.
Key Words: Serous Borderline Tumor, Serous Adenocarcinoma, MAPK
pathway, İmmunohistochemistry.
9. KAYNAKLAR:
1.
Parkin DM, Bray F, Ferlay J, Pisani P: Global cancer statistics, 2002. CA Cancer J
Clin 2005, 55:74-108
2.
Greenlee RT, Hill-Harmon MB, Cancer statistics, CA Cancer J Clin 2001; 51: 15-36
3.
D.Hanahan and R.A.Weinberg, The hallmarks of cancer. Cell 2000, 100: 57-70
4.
T.P.Garrington and G.L. Johnson, Organization and regulation of mitogen-activated
protein kinase signaling pathways. Curr Opin Cell Biol 1999; 11: 211-218)
5.
Singer G. Kurman RJ., Diverse tumorigenic pathways in ovarian serous carcinoma,
Am. J Pathol 2002, 160: 1223-1228
6.
Gudrun P et al. Inactivation of the Mitogen-Activated Protein Kinase pathway as a
potential target-based therapy in ovarian serous tumors with KRAS or BRAF mutation.
Cancer Res 2005; 65(5):1994-2000
7.
Ho- C-L, Kurman RJ, Mutation of the BRAF and KRAS precede the development of
ovarian serous borderline tumors. Cancer Res 2004; 64: 6915-6918
8.
Hsu C-Y, Characterization of active mitogen activated protein kinase in ovarian serous
carcinomas. Clin Cancer Res 2004; 10: 6432-6436
9.
Singer G, Patterns of p53 mutations separate ovarian serous borderline tumors, low
and high grade carcinomas and provide support for a new model of ovarian
carcinogenesis. Am J Surg Pathol. 2005
10. Pettersson F 1991 Annual report on the results of treatment in gynecologic cancer.
Twenty-first volume. Statements of results obtained in patients treated in 1982 to 1986,
inclusive 3 and 5-year survival up to 1990. Int J Gynaecol Obstet 36:238–277
11. Şengelen M, Türkiye'de Kanser İstatistikleri. Hacettepe Üniversitesi Sağlık Bilimleri
Enstitüsü, Kanser Epidemiyolojisi Yüksek Lisans Tezi, Ankara, 2002
12. Rosen EM, Fan S, Pestell RG, et al: BRCA1 gene in breast cancer. J Cell Physiol
196:19-41, 2003
13. Aarnio M, Sankila R, Pukkala E, et al: Cancer risk in mutation carriers of DNAmismatch-repair genes. Int J Cancer 81:214-218, 1999
14. Whittemore AS, Harris R, Itnyre J: Characteristics relating to ovarian cancer risk:
Collaborative analysis of 12 US case-control studies. Am J Epidemiol 1992; 136: 1184–
1203
15. Brinton LA, Lamb EJ, Moghissi KS, et al: Ovarian cancer risk after the use of
ovulationstimulating drugs. Obstet Gynecol 103:1194-1203, 2004
16. Choi KC, Kang SK, Tai CJ, et al: Follicle stimulating hormone activates mitogenactivated protein kinase in preneoplastic and neoplastic ovarian surface epithelial cells. J
Clin Endocrinol Metab 87:2245-2253, 2002
17. Altinoz MA, Korkmaz R: NF-kappaB, macrophage migration inhibitory factor and
cyclooxygenaseinhibitions as likely mechanisms behind the acetaminophen- and
NSAID-prevention of the ovarian cancer. Neoplasma 51:239-247, 2004
18. Ness RB, Cottreau C: Possible role of ovarian epithelial inflammation in ovarian
cancer. J Natl Cancer Inst 91:1459-1467, 1999
19. DiSaia PJ, Creasman WT, eds: Epithelial ovarian cancer. Clinical gynecologic
oncology. St. Louis: Mosby Year Book; 1997:282-350
20. Cheng EJ., Kurman RJ. Molecular genetic analysis of ovarian serous cystadenomas.
2004 Lab Invest 84: 778-784.
21. Silverberg SG, Bell DA, Kurman RJ, Borderline ovarian tumors; key points and
workshop summary. 2004 Hum Pathol 35: 910-917
22. Seidman JD, Vang R. Borderline ovarian tumors: contamporary viewpoints on
terminology and diagnostic criteria with illustrative images. Human Pathol 35: 918-933
23. Pickel H, Tamussino K. History of gynecological pathology. XIV. Hermann Joannes
Pfannenstiel. Int J Gynecol Pathol 2003;22:310–314
24. Abel C, Bandler SW. Gynecological Pathology. A Manual of Microscopic Technique
and Diagnosis in Gynecological Practice For Students and Physicians. William Wood &
Company: New York, 1901
25. Taylor HC. Malignant and semimalignant tumors of the ovary. Surg Gynecol Obstet
1929;48:204–30
26. Munnell EW, Taylor HC. Ovarian
carcinoma: a review of 200 primary and 51
secondary cases. Am J Obstet Gynecol 1949;58:943–95
27. Serov SF, Scully RE, Sobin LH. International Histologic Classification of Tumours.
No. 9. Histological Typing of Ovarian Tumours. World Health Organization: Geneva,
1973
28. Tavassoli FA, Devilee P (eds). World Health Organization Classification of Tumours.
Pathology and Genetics. Tumours of the Breast and Female Genital Organs. IARC
Press: Lyon, 2003
29. Longacre TA, Mc Kenney JK. Ovarian serous tumors of low malignant potential
(borderlien tumors) outcome-based study of 276 patients with long term (≥5 year)
follow up. 2005 Am J. Surg Pathol 29: 707-723
30. Tavassoli FA, Serous tumors of low malignant potential with early stromal invasion
(serous LMP with microinvasion) Mod Pathol 1988 1:407-414
31. Mooney J, Silva E, Tornos C, et al. Unusual features of serous neoplasms of low
malignant potential during pregnancy. Gynecol Oncol 1997;65:30–35
32. Bell DA. Scully RE: Ovarian serous borderline tumors with stromal microinvasion:
report of 21 cases. 1990; Hum Pathol 21: 394-403
33. Kennedy AW, Hart WR. Ovarian papillary serous tumors of low malignant potential
(serous borderline tumors): a long term follow-up study, including patients with
microinvasion, lymph node metastasis, and transformation to invasive serous carcinoma.
Cancer 1996;78:278–286
34. Segal GH, Hart WR. Ovarian serous tumors of low malignant potential (serous
borderline tumors): the relationship of exophytic surface tumor to peritoneal ‘implants’.
Am J Surg Pathol 1992;16: 577–583
35. Hart WR. Borderline epithelial tumors of the ovary. Mod Pathol 2005;18 Suppl 2: 3350
36. Seidman JD, Kurman RJ. Ovarian serous borderline tumors: a critical review of the
literature with emphasis on prognostic indicators. Hum Pathol 2000;31: 539^57
37. Bell DA, Weinstock MA, Scully RE. Peritoneal implants of ovarian serous borderline
tumors: histologic features and prognosis. Cancer 1988; 62: 2212–2222
38. Sieben NL, Roemen GMJM. Clonal analysis favours a monoclonal origin for serous
borderline tumours with peritoneal implants. J of Pathol 2006; 210: 405-411
39. Diebold J., Amann G., Seemüller F., Mayr D. Diagnostic and molecular genetic
pathology of serous borderline tumours of the ovary J. Diebold Current Diagnostic
Pathology (2004) 10, 318–325
40. Moore WF, Bentley RC, Berchuck A, Robboy SJ. Some Mullerian inclusion cysts in
lymph nodes may sometimes be metastasis from serous borderline tumors of the ovary.
Am J Surg Pathol 2000;24:710–8
41. Tan LK, Flynn SD, Carcangiu ML. Ovarian serous borderline tumors with lymph node
involvement. Am J Surg Pathol 1994;18:904–912
42. Shiraki M, Otis CN, Donovan JT, et al. Ovarian serous borderline epithelial tumors
with multiple retroperitoneal nodal involvement: metastasis or malignant transformation
of epithelial glandular inclusions? Gynecol Oncol 1992;46:255–258. 63
43. Leake JF, Rader JS, Woodruff JD, et al. Retroperitoneal lymphatic involvement with
epithelial ovarian tumors of low malignant potential. Gynecol Oncol 1991; 42:124–130
44. Rice LW, Berkowitz RS, Mark SD, et al. Epithelial ovarian tumors of borderline
malignancy. Gynecol Oncol 1990;39:195–198
45. Rota SM, Zanetta G, Ieda N, et al. Clinical relevance of retroperitoneal involvement
from epithelial ovarian tumors of borderline malignancy. Int J Gynecol Cancer
1999;9:477–480
46. Clevent PB, Young RH, Hyperplastic mesothelial cella within abdominal lymph
nodes: mimic of metastatic ovarian carcinoma and serous borderline tumor; a report of
two cases associated with ovarian neoplasms. Mod Pathol, 1996 ,9: 879-886
47. Prat J, de Nictolis M. Serous borderline tumors of the ovary: a long-term follow-up
study of 137 cases, including 18 with a micropapillary pattern and 20 with
microinvasion. Am J Surg Pathol 2002;26: 1111–1128
48. Deavers MT, Gershenson DM, Tortolero-Luna G, et al. Micropapillary and cribriform
patterns in ovarian serous tumors of low malignant potential: a study of 99 advanced
stage cases. Am J Surg Pathol 2002; 26:1129–1141
49. Mulhollan TJ, Silva EG. 1994; Ovarian involvement by serous surface papillary
carcinoma. Int J Gynecol Pathol; 13: 120-126
50. Silverberg SG, Histopathologic grading of ovarian carcinoma: a review and proposal.
Int J Gynecol Pathol; 2000, 19: 7-15
51. Kolch W. Meaningful relationships: The regulation of the Ras/Raf/MEK/ERK
pathway by protein interactions. Biochem J 2000; 351:289-305
52. Lee JT, McCubrey JA. The Raf/MEK/ERK signal transduction cascade as a target for
chemotherapeutic intervention in leukemia. Leukemia 2002; 16:486-507
53. Blalock WL, Navolanic PM, Steelman LS, et al. Requirement for the PI3K/Akt
pathway in MEK1-mediated growth and prevention of apoptosis: Identification of an
Achilles heel in leukemia. Leukemia 2003; 17:1058-67
54. Davies H. Et al. Mutations of the BRAF gene in human cancer. Nature 2002; 417:949454
55. Liem AA, Chamberlain MP, Wolf CR, Thompson AM. The role of signal transduction
in cancer treatment and drug resistance. EJSO 2002; 28:679-84
56. Platanias LC. Map kinase signaling pathways and hematologic malignancies. Blood
2003; 101: 4667-79
57. Ip YT and Davis RJ Signal transduction by the c-Jun N-terminal kinase (JNK)-from
inflammation to development, 1998, Curr Opin Cell Biol. 1998 Apr;10(2):205–219
58. Greenberg ME, Ziff EB. Stimulation of 3T3 cells induces transcription of the c-FOS
proto-oncogene. Nature 1984; 43-438
59. Zhu YS, Brodsky M, Franklin SO, Metrazole induces the sequential activation of cFOS, proencephalin and tyrosine hydroxylase gene expression in the rat adrenal gland:
modulation by glucocorticoid and adrenocorticotropic hormone. Mol Pharmacol 1993;
44: 328-335
60. Susini S, Roche E, Glucose and glucoincretin peptides synergize induce c-FOS, cJUN, junB, zif-268 and nur-77 gene expression in pancreatic β(INS-1) cells. The
FASEB Journal. 1998; 12: 1173-1182)
61. Stachowiak MK, Sar M. Stimulation of adrenal medullary cells in vivo and in vitro
induces expression of c-FOS protooncogene. Oncogene 1990; 5: 69-73
62. Iwata K, Takahashi O, FOS protein induction in the medullary dorsal horn and first
segment of the spinal cord by tooth-pulp stimulation in cats. Pain 1998; 75: 27-36
63. Glover JNM, Crystal structure of the Heterodimeric Bzıp Transcription Factor cFOS/c-JUN bound to DNA. Nature 1995; 373: 257-261
64. Foletta VC, Transcription factor AP-1 and the role of Fra-2. Immunol Cell Biol 1996;
74: 121-133
65. De Dousa SO, Immunolocalization of c-FOS and c-JUN in human oral mucosa and in
oral squamous cell carcinoma. J Oral Pathol Med 2002; 31: 78-81
66. Lee CS, Immunohistochemical localisation of the c-FOS oncoprotein in pancreatic
cancer. Zentrabl Pathol 1994; 140: 271-275
67. Franchi A, Immunohistochemical detection of c-FOS nad c-JUN expression and
cartilaginous tumours of the skelaton. Virchows Arch 1998; 432: 515-519
68. Cavigelli M, Dolfi F. Induction of c-FOS expression through JNK-mediated TCF/Elk1 phosphorylation. EMBO J 1995; 14: 5957-5964
69. Shih YC, Kerr J, Hurst TG, et al. No evidence for microsatellite instabilityf rom
allelotype analysis of benign and low malignant potential ovarian neoplasms. Gynecol
Oncol1998;69:210^ 3
70. Staebler A, Heselmeyer-Haddad K, Bell K, et al. Micropapillarys erous carcinoma of
the ovary has distinct patterns of chromosomal imbalances byc omparative genomic
hybridization compared with atypical proliferative serous tumors and serous carcinomas.
Hum Pathol 2002;33:47 ^ 59.
71. Meinhold-Heerlein I, Bauerschlag D, Hilpert F, et al. Molecular and prognostic
distinction between serous ovarian carcinomas of varying grade and malignant potential.
Oncogene 2005;24:1053 65
72. Krishnamurti U, Sasatomi E, SwalskyP
A, Jones MW, Finkelstein SD.
Microdissection-based mutational genotyping of serous borderline tumors of the ovary.
IntJGynecol Pathol 2005;24:56^61
73. Gilks CB,Vanderhyden BC, Zhu S, van de Rijn M, LongacreTA. Distinction between
serous tumors of low malignant potential and serous carcinomas based on global mRNA
expression profiling. Gynecol Oncol 2005;96:684^94
74. Ortiz BH, AilawadiM, Colitti C, et al. Second primary or recurrence? Comparative
patterns of p53 and K-ras mutations suggest that serous borderline ovarian tumors and
subsequent serous carcinomas are unrelated tumors. Cancer Res 2001;61:7264^7
75. Mok SC, Bell DA, Knapp RC, et al. Mutation of K-ras protooncogene in human
ovarian epithelial tumors of borderline malignancy. Cancer Res 1993; 53:1489-92
76. Chung-Liang Ho, Mutations of BRAF and KRAS Precede the Development of
Ovarian Serous Borderline Tumors CANCER RESEARCH 64, 6915–6918, October 1,
2004; 64:6915^ 8
77. Milner BJ, Allan LA, Eccles DM, et al. p53 mutation is a common genetic event in
ovarian carcinoma. Cancer Res1993;53:2128^ 32
78. Singer G, Stohr R, Cope L, et al. Patterns of p53 mutations separate ovarian serous
borderline tumors and low- and high-grade carcinomas and provide support for a new
model of ovarian carcinogenesis:
a mutational analysis with immunohistochemical
correlation. AmJ Surg Pathol 2005;29:218^24
79. Singer G, OldtRIII, CohenY, et al.Mutations inBRAF and KRAS characterize the
development of low-grade ovarian serous carcinoma. JNatl Cancer Inst 2003;95: 484^6
80. Varras MN, Sourvinos G, Diakomanolis E, et al. Detection and clinical correlations of
ras gene mutations in human ovarian tumors. Oncology 1999;56:89–96
81. Mandai M, Konishi I, Kuroda H, et al. Heterogeneous distribution of K-ras-mutated
epithelia in mucinous ovarian tumors with special reference to histopathology. Hum
Pathol 1998;29:34–40
82. Cuatrecasas M, Erill N, Musulen E, et al. K-ras mutations in nonmucinous ovarian
epithelial tumors: a molecular analysis and clinicopathologic study of 144 patients.
Cancer 1998;82:1088–95
83. Ichikawa Y, Nishida M, Suzuki H, et al. Mutation of K-ras protooncogene is
associated with histological subtypes in human mucinous ovarian tumors. Cancer Res
1994;54: 33–5
84. Hsu C-Y, Bristow R, Cha M, et al. Characterization of active mitogen-activated
protein kinase in ovarian serous carcinomas. Clin Cancer Res 2004; 10:6432^6
85. Davidson B,
Givant-Horwitz V, Lazarovici P, et al. Matrix metalloproteinases
(MMP), EMMPRIN
extracellular matrix metalloproteinase inducer) and mitogen-
activated protein kinases (MAPK): coexpression in metastatic serous ovarian
carcinoma.Clin ExpMetastasis 2003;20:621^31
86. Slomovitz BM, Caputo TA, Economos K, Gretz H: Non-invasive ovarian
proliferations with micropapillary architecture are part of the spectrum of serous
borderline tumor. Mod Pathol 2001, 14:146A
87. Caduff RF, Svoboda-Newman SM, Ferguson AW, Johnston CM,Frank TS:
Comparison of mutations of Ki-RAS and p53 immunoreactivity in borderline and
malignant epithelial ovarian tumors. Am J SurgPathol 1999, 23:323–328
88. Shih IM, Yan H, Speyrer D, Shmookler BM, Sugarbaker PH, Ronnett BM: Molecular
genetic analysis of appendiceal mucinous adenomas in identical twins, including one
with pseudomyxoma peritonei. Am J Surg Pathol 2001, 25:1095–1099
89. Parker RL, Clement PB, Chercover DJ, SornarajahT, Gilks CB. Earlyrec urrence of
ovarian serous borderline tumor as high-grade carcinoma: a report of two cases.
IntJGynecol Pathol 2004;23:265^72
90. Silverberg SG, Sasano H, Immunolocalization of c-myc oncoprotein in mucinous anda
serous adenocarcinomas of the ovary; Hum Pathol. 1992 May; 23 (5): 491-5
91. Wong AS. Profiling of protein kinases in the neoplastik transformation of human
ovarian surface epithelium. Gynecol Oncol, 2001, Aug, 82 (2):305-311
92. Chan CP, Trombin activates Ras-CREB/ATF-1 signaling and stimulates c-fos, c-jun,
and c-myc expression in human gingival fibroblasts J Periodontol. 2008;79(7):1248-54