DG-FIB
Ürünü kullanmadan önce dikkatle okuyun. Sadece laboratuvar tanısında kullanılır.
KULLANIM AMACI
DG-FIB fibrinojenin kantitatif tayini için tasarlanmıştır.
GİRİŞ
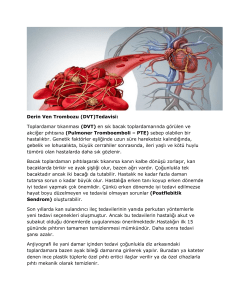
Trombin enzimi pıhtılaşma sırasında sondan bir önceki proteindir, çözünür fibrinojen üzerinde rol alır ve onu
çözünmez fibrine dönüştürür. Normal plazma fibrinojen düzeyi 200-400 mg/dl aralığında olmasına rağmen sonradan
kazanılmış veya doğuştan olan hipofibrinojenemi durumunda 10-20 mg/dl kadar düşük düzeyler ortaya çıkabilir.
Plazma fibrinojen düzeyinin belirlenmesinin, plazma fibrinojen içeriğiyle ilgili kanama bozukluklarının tanısında yararlı
bir test olduğu kanıtlanmıştır. Bu bozukluklar hiperfibrinojenemi, hipofibrinojenemi, disfibrinojenemi ve
afibrinojenemi’yi kapsamaktadır.
TESTİN PRENSİBİ
DG-FIB plazma fibrinojen düzeyini belirlemek için, dilüe plazmanın pıhtılaştırılması için sığıra ait trombinin kullanıldığı,
Clauss pıhtılaşma zamanı metodunu kullanmaktadır. İlk olarak, fibrinojen içeriği bilinen referans plazmanın (DG-Ref,
213825) 1/5, 1/10, 1/20 ve 1/40’lık dilüsyonları kullanılarak standart eğri hazırlanır. Trombin eklendiğinde, pıhtılaşma
zamanı fibrinojen içeriğiyle ters orantılı olarak elde edilir. Sonra, 1/10’luk dilüsyonda hasta plazması trombin ile
pıhtılaşır ve meydana gelen pıhtılaşma zamanı standart eğriden fibrinojen düzeyinin interpolasyonu için kullanılır.
BİLEŞİM
Her bir DG-FIB'in içeriği:
- DG-FIB
5 ml’lik 1 şişe. Herbir şişe dondurularak kurutulmuş sığır trombini içerir (100 NIH units/ml).
Reaktiflerin hazırlanması
- DG-FIB
Şişeyi su ile 5 ml’ye tamamlayarak kullanıma hazırlayın. Kullanımdan önce ara sıra döndürerek oda sıcaklığında 1520 dakika bekletin. Tüm partiküllerin iyice çözündüğünden emin olun.
KARARLILIK
2-8 ºC'de saklayın. Kullanıma hazırlandıktan sonra, 2-8 ºC’de 5 gün veya dondurularak saklandığında 30 güne kadar
kararlılığını korur. Tekrar kullanımdan önce oda sıcaklığına ısıtın. Uzun süre ısıtmadan kaçının.
ÖRNEK
1. Temiz venöz ponksiyon iğnesi ile venöz kan alınır.
2. Dokuz hacim kan bir hacim antikoagülant (sodyum sitrat, %3.2) ile hemen karıştırılır, tüp tersyüz edilerek iyice
karışması sağlanır.
3. Örnek 1500 g’de 15 dakikadan az olmayacak şekilde santrifüjlenir.
4. Plazma 60 dakika içinde plastik pipet kullanılarak tüpten alınır ve plastik tüpte saklanır.
5. Plazma örneği 4 saat içinde test edilir; aksi halde -20 °C’de dondurularak iki haftaya kadar saklanır veya -70 °C’de
altı aya kadar saklanır ve sadece kullanımdan önce eritilir.
(See NCCLS Standard H21-A3 Vol. 18 No. 20)
GEREKLİ MATERYAL (TEMİN EDİLMEMİŞTİR)
• Dilüsyon için reaktif düzeyinde su (deiyonize veya distile)
• Havuzlanmış normal plazma veya ticari referans plazma (DG-Ref 213825)
• Owren tamponu (DG-Owren 213837)
• Pıhtının belirlenmesi için manuel, mekanik veya foto-optik koagülometre.
• Plastik test tüpleri, 12 x 75 mm
• Serolojik pipetler, 1 ve 5 ml
• Hassas pipetleyiciler, 0.1ml ve 0.2 ml
• Uygun zamanlayıcı
TEST METODU
1. Sırasıyla 0.4, 0.9, 1.9, ve 3.9 ml DG-Owren kullarak 0.1 ml DG-Ref’in 1/5, 1/10, 1/20 ve 1/40’lık dilüsyonlarını
hazırlayın.
2. Fibrinojen tayini için cihaz üreticisinin talimatlarını takip ederek, test örneği gibi herbir dilüsyonun 0.2 ml’sine 37
ºC’de 2 dakika ön ısıtma yapın.
3. Test örneğine oda sıcaklığında DG-FIB’in 0.1 ml’sini ekleyin (37 ºC).
4. İkili çalışmaların pıhtı oluşum zamanlarını (koagülasyon zamanı) not edin.
5. DG-Ref’in tüm dilüsyonları için tekrar yapın.
6. Pıhtı oluşumu sürelerinin ortalamasını, fibrinojen konsantrasyonunu log-log kağıda çizerek standart eğriyi
oluşturun.
Örneğin, eğer kalibre edilen DG-Ref 240 mg/dl fibrinojen (dilüe edilmemiş) içeriyorsa 1/5, 1/10, 1/20 ve 1/40’lık
dilüsyonları, sırasıyla 48, 24, 12 ve 6 mg/dl olur.
7. Hasta plazmasının 1/10’luk dilüsyonunu DG-Owren kullanarak oluşturun. İki kopya olarak pıhtı oluşum zamanın
belirlemek için yukarıda gösterildiği gibi dilüsyonun 0.2 ml’sini DG-FIB’in 0.1 ml’si ile kullanın.
8. Hasta için pıhtı oluşum süresinin ortalamasını kullanın, standart eğriden fibrinojen değerini interpole edin.
9. Hastanın fibrinojen değerini elde etmek için eğrideki fibrinojen değerini dilüsyon faktörü ile çarpın (örneğin, x10).
NOT: Düşük fibrinojen konsantrasyonlarında pıhtı tayini yapamayacakları için bazı foto-optik cihazlarda 1/5, 1/10 veya
1/15’lik dilüsyonlar tercih edilebilir.
KALİTE KONTROL
1. Tüm tayinleri ikili kopya olarak gerçekleştirin.
2. Standart eğrilerin, doğru performans vermesi için aylık olarak hazırlanması tavsiye edilir.
3. Standart eğrisi hazırlanmış olan testin kalite kontrolü için her zaman DG-C1 ve DG-C2 kullanın. Kontrol değeri
hedeflenen değerin ± %15’inde olmalıdır.
REFERANS ARALIK
Mekanik ve foto-optik cihaz kullanılarak, tipik pıhtı oluşum süreleri aşağıda gösterilmiştir. Bu değerler sadece ana
hatlarıyla dikkate alınmalıdır, çünkü laboratuvarda kullanılan farklı cihaz ve teknikler farklı sonuçlar oluşturur.
SINIRLAMALAR
Görünüşte önemsiz faktörlerden ortaya çıkabilecek değişimleri minimize etmek için çok dikkat edilmelidir.
A. Numune Toplanması. KAÇININ:
1. Cam kullanılması. Sadece plastik kullanın.
2. Antikoagülant ile kan karışımının gecikmesi.
3. Hemolizli veya lipemik örnekler.
4. Doku tromboplastini ile kontaminasyon.
5. Yanlış oranda antikoagülant/kan.
B.Laboratuvar Teknikleri:
1. Testi 37 °C’de gerçekleştirin.
2. Sadece yüksek saflıkta su kullanın.
3. Optimum pH 7.0-7.5.
C. Etkileyici Maddeler:
1. FDP: Yükselmiş fibrin yıkım ürünleri (>30 μg/ml) uzamış pıhtılaşma zamanı ile sonuçlanabilir. Test plazmasının
daha fazla dilüsyonu (örneğin 1/20) FDP girişimini azaltacaktır.
2. HEPARİN: Dilüe edilmemiş hasta örneğine yaklaşık olarak 5 U/ml eklendiğinde, heparin yüzünden trombinin
inhibisyonu sonucunda uzamış pıhtılaşma zamanı elde edilir.
UYARILAR VE ÖNLEMLER
Tüm atıklar biyolojik materyal içerdiğinden uygun bir şekilde etiketlendirilmeli ve diğer atıklardan ayrı olarak
depolanmalıdır.
Tüm atık materyaller uluslararası, ulusal ve yerel yönetmeliklerde yazıldığı gibi imha edilmelidir.
Test klinik gözlemler ve diğer laboratuvar testlerinin sonuçları ile birlikte kullanılmalıdır.
KAYNAKÇA
1. Cohn, E.J. et al. J. Am. Chem. Soc. 7:465 (1950).
2. Menachi, D. Throm. Diath. Haemorrh. 29:525 (1963).
3. Bang, N.U. et al. Thrombosis and Bleeding Disorders: Theory and Methods. Academic Press. New York (1971).
4. McKay, D.G., Disseminated Intravascular Coagulation. Harper and Row, New York (1965).
5. Clauss, A., Acta Haemat. 17:237 (1957).
6. National Committee for Clinical Laboratory Standards: Guidelines for the Standardized Collection, Transport, and
Preparation of Blood Specimens for Coagulation Testing and Performances of Coagulation Assays. Document H21A3, vol. 18, No. 20, 1998.
7. Stevens, D. and Sanfelippo, M., Am. J. Clin. Path. 50:183 (1973).
SUNUM
213831 DG-FIB (1x5ml)
Revizyon tarihi: eylül, 2003
Bu döküman birkaç dilde mevcuttur. Çeviriler ingilizce olan ana dökümandan yapılmıştır. Şüpheler veya farklılıklar
olması durumunda ingilizce olan ana dökümandaki anlatıma öncelik verilmelidir.
Diagnostic Grifols, S.A. Passeig Fluvial, 24 - 08150 Parets del Vallès, ESPAÑA (SPAIN)