BEYNĐN ENERJĐ METABOLĐZMASININ DAMAR-SĐNĐR BĐRLEŞĐMĐ ĐLE
MODELLENMESĐ
Neurovascular Coupling Model of Brain Energy Metabolism
Sefer Burak KACAR*, Ömer ŞAYLĐ*, Kutlu ÜLGEN**, Ata AKIN*
*Boğaziçi Üniversitesi, Biyo-Medikal Müh. Enstitüsü, 34342 Bebek-Đstanbul. e-posta: burak_ka@hotmail.com
** Boğaziçi Üniversitesi, Kimya Mühendisliği Bölümü, 34342 Bebek-Đstanbul.
Özetçe - Bu makalede, insan beyninin ön lobunda
gerçekleşen biokimyasal olayların, Matlab (ver 6.0 Rel 12)
ortamında matematiksel modelinin geliştirilmesi ve
incelenmesi ele alınmıştır ve bunların hiperamonyak
hastalarının damar-sinir birleşimi üzerine etkilerinin
incelenmesi ele alınmıştır. Geliştirilen yazılım hem
doğrusal hem de doğrusal olmayan denklemleri Matlab
ortamndaki ‘ode15s solver’ aracılığıyla çözmekte, daha
sonra ise kullanıcı dostu arayüz ile sistemdeki
parametreleri değiştirmek ve biokimyasal sistemdeki
değişikliği gözlemlemek mümkündür. Damar sinir birleşim
modelinden elde edilen sonuçlar Aubert’in sonuçları ile
uyumlu bulunmuş ve hiperamonyak hastalığının
incelenmesi için kullanılmıştır.
Anahtar Sözcükler: damar-sinir birleşimi, hiperamonyak
Abstract - In this paper, a software package modeling
neurovascular coupling
is developed. The main algorithm
calculating the biochemical responses is based on the ode15s
solver in Matlab environment according to the neorovascular
coupling model in Aubert’s paper in literature. The software
package is developed under Windows XP in Matlab 6.0
environment and thus enables the user to work under an userfriendly graphical user interface. The algrithm which was
deveolped could solve both linear and non-linear equations via
‘ode15s solver’ in Matlab environment and so, it can give an
opportunity to the user to change the paremeters in biochemical
system and investigate the changes. The responses which was
obtained from neurovascular coupling model have been found in
good aggrement with the results which was obtained by Mrs.
Aubert and hyperammonemia has been investigated by using our
software package. Results have been discussed and biochemical
pathways behind hyperammonemia have been clarified.
Keywords: neurovascular coupling model, hyperammonemia
I. GIRIŞ
Matematiksel modelleme fizikte, kimyada ve
mühendislikte doğal olayların ve deneysel sonuçların
gerek yorumlanmasında gerekse tahmin edilmesinde
güçlü bir araçtır. Bir matematiksel model her zaman
gerçek olayın sadeleştirilmiş bir şeklidir ve bundan
dolayı aynı olay için amaçlarımıza ve eldeki verilerimize
uygun farklı matematiksel modeller kurmak mümkündür.
Metabolizmanın
matemetiksel
modellenmesi,
metobolizmanın önemli kısımlarının kantitatif olarak
ifade edilmesi bakımından anlayışımızı da oldukça
geliştirecektir.
Sinir
hücrelerinin
biokimyasal
etkinliklerinin modellenmesi, damar-sinir birleşiminin
sağlıkta ve hastalıkta nasıl etkileneceğinin anlaşılması
ihtiyacı bakımından da fonksiyonel görüntüleme
gruplarının özel ilgisini çekmektedir. Fonksiyonel beyin
görüntülemedeki dikkat çekici gelişmelere rağmen,
günümüzde hala hücresel ve moleküler bazda elde
edilen işaretlerin anlamlandırılmaları büyük çapta
bilinmemektedir. Fonksiyonel görüntülemenin temel
fizyolojik prensibi, sinirsel aktivite ve buna eşlik eden
kan akış hızındaki ve enerji metabolizmasındaki yerel
artışlardaki sıkı ilişkinin ifade edilmesidir[1].
Uyarıdan kaynaklanan sinirsel aktivasyona, yerel kan
akış hızının veya hacminin artışına neden olan metabolik
ve oksijen tüketen mekanizmalar eşlik etmektedir.
Ancak, milisaniyeler içinde gerçekleşen sinirsel
süreçlerin aksine damarsal cevaplar olgunlaşmaları için
daha fazla zamana ihtiyaç duyarlar, bu süre genelde
birkaç saniye civarındadır. Damar-sinir birleşiminin
veya hemodinamik cevabın modellenmesi için çeşitli
önerilerde bulunulmuştur.
Metabolik olayları geliştirmek ve analiz etmek için
şuan kullanıcı dostu yazılım programları mevcuttur.
GEPASI, biokimyasal sistemlerin analizi için özel olarak
hazırlanmış bir yazılımdır. Bu yazılım paketi,
biokimyasal sistemlerin kontrol değişkenlerini ve
elastisiyetlerini hesaplamada kullanılmaktadır. Bu
programa eşdeğer sayılabilecek programlar SCAMP ve
DBSolve’dır. Bu yazılım programları, ilk bakışta
oldukça faydalı görünmesine rağmen, karmaşık
biokimyasal olayların modellenmesinde yetersiz
kalmaktadır. Bu yüzden, biolojik modelimizi çözmek
için herhangi bir kısıt olmaksızın uygun yazılım
programını seçmeliyiz[6].
Makalenin amacı, Aubert’in yaratmış olduğu
biokimyasal modeli, Matlab(Ver. 6.0 R12) ortamında
tekrar yaratıp, buna bir arayüz ekleyerek, modelin
hastalıklı durumlardaki değişimlerini incelemektir. Bu
model sayesinde, sürekli beyinsel aktivite durumunda
performanstaki bozulmaların sebepleri de açıklanmaya
çalışılacaktır.
II. SĐNĐR-DAMAR BĐRLEŞĐM MODELĐ
Modelin amacı, beynin sınırlı bir bölgesi için sinir ve
kan damarlarının metabolik ve iyon denge denklemlerini
tanzim edip, Matlab ortamında yeniden yaratmaktır.
Dikkate alınan konsantrasyonlar, kılcal damar içi ya da
hücre içi konsantrasyonlardır. Modelin temel varsayımı
elektriksel aktivite ve metabolizma arasındaki birleşimin
sodyum pompasının ATP tüketimi sonucu olduğudur.
Bu varsayım H1 hipotezi olarak adlandırılacaktır. Bu
yüzden sinaps öncesi ve sonrası elektriksel aktiviteye
Na+ iyonlarının hücre içine girmesi ve bunun Na/K
ATPase pompasını tetikleyerek hücre iyon derişiminin
yeniden kurmak için aktif taşımaya başlaması neden
olmaktadır.
Sinir hücrelererindeki ATP derişiminin denge düzeyi
farklı mekanizmalar tarafından düzenlenmektedir.
Bunlar: (i) ATP’nin tampon rol oynayan fosfokeratinden
elde edilmesi. (ii) glikoliz ve (iii) oksijenli
fosforlanmadır. Uyarının olmadığı durağan durumda,
glikozun tamamen CO2 ve H2O’ya okside olduğu
varsayılır. Öte yandan, beynin belli bölgesine uyarı
verildiğinde, gerekli olan serbest enerjinin büyük çapta
oksijensiz glikoliz yolu ile elde edildiği ve bunun laktat
üretimine neden olduğu bilinmektedir. Laktat sentezi
geçici bir durumdur ve bunun oksijenli fosforulasyonun
yeterli seviyeye ulaşmasından önce gerçekleştiği
bilinmektedir. Son olarak ise, kan akışı hücrelere glikoz
ve oksijen sağlamakta, fazla laktat ise hücrelerden
alınmaktadır. Elektriksel aktivite ve metabolizma uyarısı
arasındaki ilişkinin hücre içi sodyum derişimi dışında
ikinci hücre içi mesaj taşıyıcı tarafından izah edildiği
mekanizmalar da göz önünde bulundurulacaktır. (H2
hipotezi ). Aşağıdaki şekilde modelin temel
sembolleri onların derişimlerini göstermektedir. Đkinci
olarak, tüm hacim, alan ve kan akış değerleri birim doku
hacmi olarak ifade edilmiştir. Örneğin, toplardamar
hacmi olarak Vv ‘ yi yazdığımızda, bu birimsiz
toplardamar hacim oranını temsi etmekte, benzer şekilde
kılcal damar akışı Fin(t) s-1 biriminden ifade edilmektedir.
Üçüncü olarak ise derişimlerin altındaki ‘’0’’ değeri
temel ya da dinlenme durumundaki derişim değerlerini
vermektedir. Son olarak ise, reaksiyon hızları
milimol/(saniye*hücre içi hacim) biriminden ifade
edilmiştir.
Modelin Yapısı
Modelimiz, 15 durum değişkeninden oluşan, bir girişdurum-çıkış modelidir. Fin(t) (beyin kan akış hızı) ve
vstim(t) (uyarı) olmak üzere iki tane giriş fonksiyonu
mevcuttur. Modelin çıkışları ise, (i) BOLD işareti ,yt ve
(ii) P MRS tarafından ölçülen metabolik derişimleridir.
Modelimizi, aşağıdaki şekilde görüldüğü üzere iki ana
bölüm halinde incelememiz mümkündür.
Şekil 2. Modelimizin giriş-durum-çıkış organizasyonu
(Kaynak 3’den alınmıştır.)
varsayımlarını
bulunmaktadır.
göz
önünde
bulunduran
model
Şekil 1. Modelin temel fizyolojik hipotezlerini göz önüne alan
diagram
(Kaynak 3’den alınmıştır.)
Ön Kabüller
Modeli tarif etmeden önce bazı ön kabüller yapmamız
gerekmektedir. Đlk olarak iyonların ya da moleküllerin
Kütle ve yük denklemleri zamana bağlı sabit durumlu
diferansiyel denklemlerden oluşmaktadır. Damar sinir
birleşim modelimizde Na+, GLC, GAP, PEP, PYR, LAC,
NADH, ATP, PCr, O2i, O2c, GLCC, LACC, VV, dHb
oluşan durağan durum değişkenleri mevcuttur.
Değişkenlerin
altındaki
‘c’
altsimgesi
kılcal
damarlardaki derişimleri, ‘i’ altsimgesi ise hücre içi
derişimleri göstermektedir. Bu durum değişkenleri ile
sodyum dinamiği, hücre içi enerji metabolizması, ve
glikoz, laktat, ve oksijen kan-beyin bariyeri
metabolizmaları tanımlanmıştır. Yukarıdaki şekilde
görüleceği üzere, birinci bloğun girişleri Fin(t) ve
vstim(t)’dir. Çıkışlardan biri O2c-(t) dir. Fin(t) ve O2c-(t)
fonksiyonları Buxton ve arkadaşlarının Balloon
Modeli’ndeki Bold işaretini hesaplamaya yarayan ikinci
bloğun girişleridir.
Modelin detayları şöyle gösterilmiştir: (i) beyin kan akışı
(ii) hücre içi sodyum (Na+) (iii) glikoliz (GLC, GAP,
PEP, PYR, LAC, NADH) (iv) ATP, PCr ve mitokondri
solunumu (ATP, PCr, O2i) (v) kan-beyin bariyeri
değişimleri (O2c, GLCC, LACC) (vi) Balloon Modeli (VV,
dHb) [8]
III. HĐPERAMONYAK VE
METABOLĐZMAYA ETKĐLERĐ
Makelenin bu kısmında hiperamonyak hastalığını
tanımlayacağız ve bu hastalığın uyarlanmış damar sinir
birleşim sistemi modelinde değişen parametreleri
uygulayarak, hiperamonyak ve sağlıklı durum arasındaki
farkları yorumlayacağız. Bu kısımda, Aubert’in beyin
tümörlerini inceleyen çalışmasıyla benzer metadoloji
izlenmiştir. Öncelikle, her değişen parametrenin etkisi
teker teker ele alınacak, daha sonra ise bunların birleşik
etkisini incelenecektir.
Amonyak, yüksek derişimlerde merkezi sinir
sisteminde işlevsel rahatsızlıklara yol açan, protein ve
diğer birleşiklerin parçalanması sonucu ortaya çıkan
zararlı bir birleşiktir. Amonyağın zehirli etkisi
karaciğerde üre döngüsü vasıtasıyla
giderilir.
Hiperamonyak terimi ise, amonyağın karaciğerde zehirli
etkisinin giderilmesi yerine, kan dolaşımına katılması
anlamını taşımaktadır. Hiperamonyak ve buna bağlı
rahatsızlıklar, genel olarak kalıtımsal üre döngüsündeki
bozulmalardan, sirozdan, virüs enfeksiyonları ve
toksinlerin (etanol gibi) yutulması sonucu ortaya çıkar.
Hiperamonyak, ağır karaciğer hastalıklarında başta gelen
ölüm nedenleri arasındadır. Genel belirtiler arasında,
beyin ödemi ve komaya neden olan merkezi sinir sistemi
bozuklukları vardır. Đki tip hiperamonyak vardır:
1.
2.
Edinilmiş Hiperamonyak
Zehirli maddelerin yutulmasından, virüs enfeksiyonları
ve bağışıklık sistemi hastalıklarından kaynaklanan
karaciğer bozuklukları kan ve beyinde amonyak
derişimin artmasına neden olur. Karaciğer fonksiyonları
bozuldukça, HE (Hepatic Encephalopathy) denilen ağır
nöropsikiyatrik durum ortaya çıkar. [9]
Hiperamonyağın Fizyolojik Mekanizması:
Bilindiği üzere, sinir aktivitesi astrositler tarafından
kontrol edilen beyin homostasisine yakından bağlıdır.
Amonyağın ortadan kaldırılmasında önemli fonksiyonlar
üstlenen genel olarak astrositlerdir. Aşağıdaki şekilde
astrositlerin, amonyağın ortadan kaldırılmasındaki
fonksiyonları verilmiştir.
Kalıtımsal Hiperamonyak:
Üre döngüsünde enzimatik reaksiyonlarda doğuştan
kaynaklanan bozukluklar, bu hastalarda sık karşılaşılan
bir durumdur. Ancak, en sık karşılaşılan durum birincil
kalıtımsal üre döngüsü bozukluğu olan OTC (ornithine
carbomyl transferase) enzimidir. OTC, vücutta azotun
parçalanması ve ortadan kaldırılmasında rol oynayan 6
enzimden bir tanesidir. OTC bozukluğu insanlarda aşırı
dozda X-ışınlarına maruz kalma sonucunda kalıtımsal
olarak iletilir. Aşağıdaki şekilde üre döngüsünün yapısı
görülmektedir.
Şekil 5 Üre döngüsü (Kaynak 7’den alınmıştır)
Şekil 6 Nöron-astrosit modeli (Kaynak 7’den alınmıştır)
Bu yüzden, hiperamonyak hastalığında nöropatolojik
değişimler nöronlar yerine astrositlerde meydana
gelmektedir. Şekil 6’da görüldüğü gibi, sinir boşluğuna
salgılanan glutamat EAAT-1 ve EAAT-2 taşıyıcıları
tarafından astrositlere iletilir. Genel olarak astrositlerde
bulunan GS enzimi ise, glutamat ve amonyağı glutamin
parçalayan önemli bir enzimdir. GS enziminin aktivitesi
hormonlar vasıtasıyla düzenlenmektedir (insulin, tiroid
vs.). PCA sıçanları üzerinde yapılan çalışmalarda,
amonyak fazlalığının glutamat yoğun bölgelerde
bulunan astrositlerde GS artışına neden olduğu
gözlenmiştir. PCA sıçanları, cerrahi bir operasyondan
sonra gönüllü etanol tüketimlerini arttırırlar, yani
edinilmiş hiperamonyak rahatsızlığına sahiptirler. Bunun
aksine, glutamat yoksun bölgelerdeki GS enzimlerindeki
düşüş amonyak ve glutamat arışına neden olur. Bu
bölgelerde bulunan astrositlerin GS üretiminden yoksun
olmaları ve hücre dışı glutamat derişiminin artışı sinirsel
zehirlenmeye neden olabilir.
Hücre dışı glutamat’in artışı NMDA resöptörlerinin de
aşırı derecede uyarılmasına ve bunun sonucu olarak da
Ca2+ ve Na+ iyonlarının da hücre içine girip Na+/K+
pompasının fazla çalışmasına neden olur. Hücre dışı
glutamate derişiminin artışı aynı zamanda NOS
enziminin uyarılmasına ve nitrikoksit (NO) sentezininin
artışına neden olur. NO önemli bir haberleşme
molekülüdür ve fazla sentezi de nöronların
zehirlenmesine neden olur. Aşırı nitrikoksit reaktif
oksijen maddeleri uyararak mitokondriye de zarar verir.
NO aynı zamanda astositlerdeki GS enziminin
aktivitesini engelleyerek aşırı amonyağın ortadan
kaldırılmasını engeller.
Hiperamonyak Đçin Önerilen Olası Adımlar
Aşağıdaki şekilde hiperamonyak için önerilen olası
mekanizma verilmiştir.
Kan amonyağında artış
Beyin amonyağında artış
Kan amonyağında artış
α-KGDH’in engellenmesi
Kan amonyağında artış
Beyin laktatında
artış
Beyin enerji
Astrosit glutamat nakil
düşüşü
Beyin enerji
Hücre dışı beyin
glutamatında düşüş
Hücre şişmesi
Beyin ödemi
Damar içi
Basınçta Artış
Beyin fıtığı
Ölüm
Şekil 7 Hiperamonyağın olası fizyolojik mekanizması (Kaynak
5’den alınmıştır.)
Yukarıdaki şekilde görüldüğü gibi amonyaktaki artış,
Kreps döngüsünün önemli enzimlerinden olan αKGDH’i engellemektedir. Bunun sonucu olarak da,
glikozun oksitlenmesinde azalma ve laktik asit
derişiminde artış meydana gelmektedir. Glutamat ve
laktik asit miktarlarında artış, hücrelerde şişmeye ve
beyin fıtığına neden olmaktadır. Beyinde meydana gelen
ödemler, damar içi basıncı artması ve bunun sonucu
olarak da beyin fıtıklarının ve ölümün meydana
gelmesiyle yakından ilintilidir.
Şimdi hiperamonyak rahatsızlığının çeşitli metabolizma
birleşenleri üzerine etkilerini ele alacağız. Bunlar:
Hiperamonyakta Yüksek Glikoz Tüketimine Bağlı
Metabolik Değişimler Üzerine Etkisi
Hiperamonyak rahatsızlığını incelemek maksadıyla
hayvan modelleri üzerine yapılan çalışmalarda birbiriyle
çelişen sonuçlar elde edilmesine karşın, insanlar üzerine
yapılan çalışmalarda beyin metabolik glikoz kullanım
oranında düşüş gözlenmiştir. Hawking ve Jessy
tarafından yapılan çalışmalarda PCA sıçanlarında beyin
metabolic glikoz kullanım oranında (CMRGLC) % 25 ila
% 60 arsında azalış gözlenmiştir.
Hiperamonyakta Kan Akışındaki Azalmanın Metabolik
Değişimler Üzerine Etkisi
Hiperamonyak rahatsızlığının beyin kan akışı üzerine
önemli etkileri bulunmuştur. Etkiler hastalığın ağırlığına
ve süresine göre değişmekte ve bölgesel seçicilik
taşımaktadır. Son araştırmalar, beyin kan akışında genel
bir düşüşten ziyade bölgesel değişimler olduğu
doğrultusundadır. Son araştırmalar aynı zamanda beynin
üst kısımlarında kan akışında azalma, alt tabakalarda ise
artma olduğunu göstermektedir. Uyarlanmış damar sinir
birleşim modelimizde ise kan akışında azalma olduğunu
varsayacağız. Bunun sebebi, kullandığımız damar sinir
sistemi birleşim modelinin de beynin üst tabakasındaki
ölçümlere dayanmasıdır.
Hiperamonyakta
Na+/K+
ATPase
Metabolik Değişimler Üzerine Etkisi
Aktivitesinin
Akut hiperamonyakta beyin enerji metabolizmasındaki
açığı açıklamak üzere iki mekanizma önerilmiştir.
Bunlar:
1) toplam sitrik asit döngüsündeki α-KGDH
enziminin aktivitesinin engellenmesi
2) NMDA resöptörlerinin aktivasyonu
Birinci mekanizma için, α-KGDH’ nın deaktivasyonu
püruvat oksidasyonunun azalmasına ve laktik asit ve
alaninin beyinde birikmesine neden olmaktadır.
NMDA resöptörlerinin aktivasyonu ise Na+/K+
pompasının
fazla
çalışmasına
ve
kalsiyum
homostasisinin bozularak mitokondride ATP sentezinin
azalmasına yol açmaktadır. NMDA resöptörlerinin
aktivitesi Ca2+ ve Na+ iyonlarının postsinapslardan daha
fazla içeri girmesine sebep olur, çünkü Ca2+ ve Na+
iyonlarının geçirgenliği artmıştır. Na+/K+ pompasının
aktivitesi de bu yüzden hem Na+ hem de Ca2+
homostasisini sağlamak için artmıştır. [10]
Hiperamonyakta
Mitokondri
Solunumuna
Metabolik Değişimler Üzerine Etkisi:
Bağlı
Hiperamonyağın önemli etkilerinden bir tanesi de
mitokondri
solunumuyla
ilgilidir.
Doğuştan
hiperamonyak hastalığına sahip spf sıçanları üzerinde
yapılan çalışmalarda, elektron nakil zincirinde (ETC)
cytochrome
C
oxidase
aktivitesinin
durması
gözlemlenmiştir. Spf sıçanları, X-ışınları ile OTC
enziminin aktivitesi engellenmiş, yani kalıtımsal
hiperamonyağa sahiptirler. Uyarlanmış damar sinir
birleşim modelimizde vmito mitokondri solunumunun
yerini tutmaktadır ve mitokondri solunum hızını
düşürmek için modelde Vmax,mito parametresini düşürmek
gereklidir. Vmax,mito, ikincil habercilerin olmadığı
durumlarda azami solunum miktarını temsil etmektedir.
[9]
edilen maksimum ya da minimum noktalardaki değişim
yüzde değişim cinsinden ifade edilmiştir.
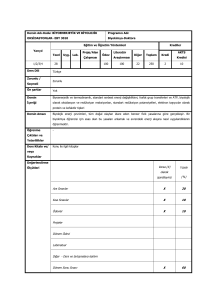
Tablo 1’den de göreleceği üzere, beynin kan akışında
bir azalma olduğunda, ATP derişimi minimum
noktasında % 2 azalmakta, BOLD işareti de minimum
noktasında % 40 azalma göstermektedir. Laktik asit
derişimi maksimım noktada % 21 artış göstermekte, PCr
ve rCMRO2’de ise fazla bir değişiklik gözükmemektedir.
Hiperamonyağın Beyin Metabolizması Üzerine Birleşik
Etkisi:
Hiperamonyak rahatsızlığının metabolizma üzerine
etkisini tek tek parametreler vasıtasıyla inceledikten
sonra, birleşik etkiyi bulmak için tüm değişen
parametreleri
benzetim
paket
programımıza
uygulamamız mümkündür.
IV. BENZETĐM PAKETĐMĐZLE
HĐPERAMONYAĞIN ĐNCELENMESĐ
Bu kısımda, benzetim paketimiz vasıtasıyla, literatürden
edindiğimiz katsayıları modelimizde uygulayacağız ve
sonuçları tablo halinde sunacağız. Beyin glikoz kullanım
oranını değiştirmek için kHK-PFK parametresini
değiştirmemiz gereklidir. portacaval shunted rats (PCA
sıçanları) üzerinde yapılan çalışmalarda beyin glikoz
kullanım oranında %25 oranında azalma saptanmıştır.
Beyin glikoz kullanım oranı mekanizmasını %25
azaltmak için diferansiyel denklemlerimizdeki kHK-PFK
parametresini de % 25 azaltmak gereklidir. Beyin kan
akışı, diferansiyel denklem sistemimizde Fin (t) = (1+αF)
F0 denklemi ile ifade edilmiştir. Burada F0, temel
durumdaki
kan
akışının
yerini
tutmaktadır.
Literatürdeki çalışmalarda kan akışının % 25 oranında
düşeceği bilinmektedir. Kan akış hızını %25 oranında
düşürmek için F0 parametresini de % 25 oranında
azaltmak gereklidir. Hiperamonyak rahatsızlığın diğer
etkisi, Na+/K+ ATPase enzimi üzerinedir. Literatürde
yapılan çalışmalarda, Na+/K+ ATPase enziminin % 57
oranında artmış olduğu saptanmıştır. Bu enzimin
aktivitesini % 57 oranında arttırmak için, diferansiyel
denklem sistemimizde kpump parametresini de % 57
oranında arttırmak gereklidir. Hiperamonyağın bir diğer
etkisi de mitokondri solunumu ile ilgilidir. Literatürdeki
çalışmalarda
mitokondri
solunumunun
azaldığı
bilinmektedir. Mitokondri solunumun % 20 oranında
azaltmak için, Vmax,mito parametresini de % 20 oranında
azaltmak gereklidir. Son olarak ise bahsettiğimiz tüm bu
değişikliklerin birleşik etkisini görmek üzere tüm
değişen parametreleri aynı anda uygulayacağız. Bir
sonraki bölümde hiperamonyak hastalığının yol açtığı
değişikliklerin durum değişkenleri ve fizyolojik
mekanizmalar üzerine etkileri ele alınacaktır.
Benzetim Sonuçları:
Tablo 1’de, hiperamonyak hastalığının benzetim
programımız vasıtasıyla incelenmesi sonucunda elde
Beynin glikoz tüketiminde % 25’lik bir azalma
meydana geldiğinde; ATP ve PCr minimum noktalarında
sırasıyla % 8 ve % 2 ‘lik bir azalma göstermekte, laktat
derişimi ise maksimum noktasında % 67 azalma
göstermektedir. Bunun nedeni beynin daha az glikoz
tüketimine bağlı olarak laktat sentezinin de azalmasıdır.
Na+/K+ ATPase aktivitesinde % 57’lik artış sonucu
ATP, PCr ve BOLD işaretinin minimum noktalarında
sırasıyla % 7, % 1 ve % 12 azalma meydana gelmektedir.
Laktat ve rCMRO2 de ise maksimum noktalarda
sırasıyla % 70 ve % 2.5 artış meydana gelmektedir.
Mitokondri solunumunda % 20 artış meydana
geldiğinde ATP, PCr ve BOLD parametrelerinin
minimum noktalarında sırasıyla % 73, % 87 ve % 66.7
azalma meydana gelmektedir. En büyük değişim oranı
ise laktat derişimde meydana gelmektedir. Durağan
durumda (2000. saniye) 1 mM olan laktat derişimi, 10
mM’a kadar çıkmaktadır. rCMRO2 oranında ise
maksimum noktada % 14.6 artış olmaktadır.
Birleşik etkiye baktığımızda, ATP, PCr ve BOLD’un
minimum noktalarında sırasıyla % 88.5, % 89.5 ve % 20
azalma meydana gelmekte,
rCMRO2 oranında ise
maksimum noktada % 13 artış olmaktadır. Laktat
derişime baktığımızda, 2000. saniyede durağan durumda
amonyak derişimi 1 mM’dan 12.5 mM’a çıkmıştır ve
artmaya devam etmektedir.
V. TARTıŞMA VE SONUÇ
Bu makalenin esas amacı, beynin fonksiyonlarını
görüntülemeye yarayan metodları yorumlamak amacıyla
beyinde gerçekleşen çeşitli hemodinamik, metabolik ve
elektrofizyolojik olayları incelemektir. Bu model, aynı
zamanda bir metabolik hastalık olan hiperamonyak
rahatsızlığının beyin hemodinamiğinde nasıl cevaplar
vereceğine dair de bizlere fikir verecektir. Ancak
bilindiği kadarıyla beyindeki tüm metabolik olayları
kapsayan bir model literatürde mevcut değildir, sadece
özel durumlar için modeller bulumaktadır. Bunlar: (i)
beyin hemodinamiği ve oksijen değişimi (ii) alyuvar
glikolizi ve oksidatif fosforilasyon (iii) beyin
elektrofizyolojisi.
Modelimizde kullanılan diferansiyel denklemler şu an
için beyin metabolizması hakkındaki bilgi düzeyimizi
yansıtmaktadır. Bu değerleri değiştirerek metabolik
hiperamonyak
hastalığında
değişen
durum
parametrelerini ve metabolik değişimleri gözlemlemek
mümkündür.
SÖZLÜK
Türkçe
Atardamar
Bariyer
Benzetim
Durum
En küçük
Dizge (sistem)
Hiperamonyak
Kılcal damar
Konsantrasyon
Sav
Sınır küme
Toplardamar
Uyarı
Uyarlanmış
Đngilizce
Artery
Barrier
Simulation
State
Minimum
System
hyperammonemia
Capillary
Concentration
Theorem
Limit
Veneous
Stimulation
implemented
KAYNAKLAR
[1] Andreas Karoly Gombert and Jens Nielsen ‘’Mathematical
modeling of metabolism ’’, Current Opinion of Biotechnology, cilt 11,
sayfa 180-186
[2] Agnes Aubert, Robert Costalat and Romain Valabregue ‘’
Modelling of the Coupling between brain electrical activity and
metabolism ’’, Acta Biotheoretica, cilt 49, sayfa 301-326
[3] Agnes Aubert, Robert Costalat ‘’ A Model of the Coupling between
Brain Electrical Activity, Metabolism, and Hemodynamics:
Application to the Interpretation of Functional Neuroimaging’’,
Neuroimage, cilt 17, sayfa 1162-1181
[4] Agnes Aubert, Robert Costalat, Hugues Duffau ve Habib Benali, ‘’
Modelling of Pathophysiological Coupling between Brain Electrical
Activation, Energy Metabolism and Hemodynamics: Insight for the
Interpretation of Intracerebral Tumor Imagin’’, Acta Biotheoretica, cilt
50, sayfa 281-295, 2002.
[5] Charauret N., Rose C., and Butterworth RF., ‘’Mild Hypothermia
in the Prevention of Brain Edema in Acute Liver Failure: Mechanisms
and Clinical Prospects,’’ Metabolic Brian Disease., cilt 17, sayfa 448450, 2002.
[6] Christoph Giersch ‘’ Mathematical modelling of metabolism ‘’
Current Opinion in Plant Biology ‘’, cilt 3, sayfa 249-253
[7] Felipo V., Butterworth R.F., ‘’Neurobiology of ammonia,’’
Progress in Neurobiology, cilt. 67, sayfa. 259-279, 2002.
[8] Kacar S.B., Sayli Ö., Ülgen K., Akın A., ‘’Beynin Enerji
Metabolizmasının Damar-Sinir Birleşimi Đle Modellenmesi, ’’
Biyoumut 2003 sayfa 58-63.
[9] Rama Rao K. V., and Norenberg M.D., ‘’Cerebral energy
metabolism in hepatic encephalopathy and hyperammonemia,’’
Metabolic Brain Disease, cilt. 16, sayfa. 67-78, 2001.
[10] Ratnakumari L., Audet R., Qureshi I.A., and Butterworth R.F.,
‘’Na+-K+-ATPase activities are increased in both congenital and
acquired hyperammonemic syndromes,’’ Neuroscience Letters, cilt
197, sayfa 89-90, 1995.
[11] The Student Edition of Simulink, ‘’ Dynamic System Simulation
For Mat lab’’ Prentice Hall 1998, Version2
[12] http:// www.busim.ee.boun.edu.tr
[13] http:// www.mathworks.com
TABLO 1
HIPERAMONYAK HASTALıĞıNıN BENZETIM SONUÇLARı
ATP
%2 azalma
(min. noktada)
PCr
-
Lac
% 21 artış (mak.
noktada)
rCMRO2
-
%8 azalma
(min. noktada)
%1-2 azalma(min
noktada)
%67 azalma
(mak. noktada)
-
%7 azalma
(min. noktada)
% 0.5-1 azalma (min.
noktada)
% 70 artış (mak.
noktada)
% 2.5 artış
(mak.
noktada)
Vmax,mito
(%20
artış)
%73 azalma
(min noktada)
% 87 azalma (min
noktada)
2000 nci saniye:
1mM (normal
durum)
10.5 mM
(hiperamonyak)
%14.6
artış
(mak.
Noktada)
Birleşik
etki
%88. 5 azalma
(min noktada)
%89.5 azalma (min.
noktada)
2000 nci saniye:
1mM (normal
durum)
12.5 mM
(hiperamonyak)
%13 artış
(mak.
Noktada)
F0 (%25
azalma)
kHK-PFK
(%25
azalma)
kpump
(%57
artış)
BOLD
% 40 min
noktada
azalma
%12
azalma
(min
noktada)
% 66.7
azalma
(min
noktada)
%20
azalma
(min
noktada)