5. Hafta
advertisement

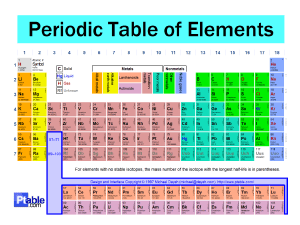
9. SINIF KİMYA 10-14 MART 3. Ünite Kimyasal Türler Arası Etkileşimler Konu Başlıkları 1. Kimyasal Türler ve Etkileşimleri a) Kimyasal Bağ Nedir? b) Bağların Sınıflandırılması - Bağ Enerjisinin Büyüklüğüne Göre (Güçlü ve Zayıf Etkileşimler) - Bağın Oluşum Mekanizmasına Göre (İyonik, Kovalent, Metalik Bağlar) 2. Güçlü Etkileşimler Bu ünitede kavrayacaklarınız Kimyasal tür Elektrostatik çekim Bağ enerjisi İyonik bağ Orbital örtüşmesi Kovalent bağ Koordinasyon bağı Polarlık Dipol moment Metalik bağ Van der Walls bağı Dipol-dipol bağı İndüklenmiş dipol Hidrojen bağı Konu Başlıkları 1. Kimyasal Türler 2. Kimyasal Türler Arasındaki Etkileşimler 3. Kimyasal Bağların Oluşum Mekanizması 4. Güçlü ve Zayıf Bağların Oluşması ve Kopması ATOM : Atom : Elementlerin özelliğini taşıyan en küçük birimine atom denir. Veya, fiziksel ve kimyasal yöntemlerle daha basit birimlerine ayrıştırılamayan, maddenin en küçük birimine atom denir. Gözle görülmesi imkânsız, çok küçük bir parçacıktır ve sadece taramalı tünel mikroskobu (atomik kuvvet mikroskobu) ile incelenebilir. Ortalama çapları 10 -8 cm civarındadır. MOLEKÜL : Genel olarak molekül, Saf kimyasal maddenin (Element ya da bileşik) kendi başına bütün kimyasal bileşimini ve özelliklerini taşıyan, en küçük parçasıdır. Atomik Moleküller; O2, N2, F2 , Cl2 , P4, S8 … gibi. Bileşik Moleküller: CO2, NO2, SO2...gibi. Not: NaCl, AlCl3, NaNO3 gibi iyonik bileşikler gerçekte molekül değil iyonik kristaller olarak bilinirler. İYON : Bir atom, elektron verdiğinde verdiği elektron sayısı kadar + yükle yüklenir. Elektron aldığında, aldığı elektron sayısı kadar -yükle yüklenir. İşte bu + ve - yüklü atomlara İYON denir. + yüklü iyonlara KATYON, - yüklü iyonlara da ANYON denir. ANYON - : Nitrat SO3 = : Sülfit SO4 = : Sülfat = : Karbonat NO3 CO3 CrO4 = : Kromat KATYON H+ : Proton Na+ : Sodyum Mg+2 : Magnezyum Ca+2 : Kalsiyum Al+ 3 : Alüminyum