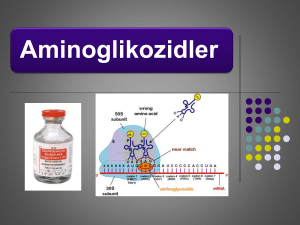
Antibiyotiklere
Direncin Araştırılması
Antibakteriyel etki mekanizmaları
RNA polimeraz
DNA topoizomeraz
rifampicin
Hücre
duvarı
quinolones,
novobiocin
b-lactams
vancomycin
bacitracin
DNA
mRNA
Hücre zarı
polymyxins
THF
DHF
50S
50S
50S
30S
30S
30S
ribosomes
folate sentezi
sulphonamides
trimethoprim
pABA
protein sentezi (30S)
protein sentezi (50S)
tetracyclines
aminoglycosides
fusidic acid ve diğerleri
macrolides
lincosamides
chloramphenicol
oxazolidinones
Antibiyotikler
• Hücre zarına etkililer: Polimiksin, kolistin
• Hücre duvarı sentez inhibisyonu :Beta
laktamlar, glikopeptidler,
sikloserin,basitrasin, ristocetin
• Protein sentezi inhibisyonu yapanlar:
Kloramfenikol, tetrasiklinler,
makrolidler,klindamisin, aminoglikozidler
• Nükleik asit sentezini bozanlar:
Nalidiksik asit, kinolonlar
• Antimetabolitler: Ko-trimoksazol
• Diğerleri: fusidik asit, metronidazol,...
Antibiyotik direnci
• Doğal direnç : Yapısal özellikleri ile
- İlacın uygun hedef bölgesi yoktur
- Hedefe ulaşmayı engelleyen yapı
- Hücre içine giriş mekanizması
yoktur
Sporlar, L- formları, dormant M.
tbc,... antibiyotiklerden etkilenmez
Antibiyotik direnci
• Kazanılmış direnç :
- İlacın hedefinde değişiklik olması
- İlacın inaktivasyonu
- Farklı metabolik yol
- Hücre içinde ilacın azalması
Kazanılmış direnç
• Kromozomal mutasyonlar
Kolay oluşurlar, antibiyotik çekilince
kaybolur
***Yeni genetik elemanlarla (plazmid,
transpozon,...)
Zor oluşur, adaptasyon sağlanırsa kalıcı
olabilir
Direnç (genetik temeller)
• Kromozomal mutasyonlar
• Plazmid
• Transpozon /IS
“Gen Kasetleri”
Günümüzde önemli
dirençler
• Beta laktamazlar.....
• Penisiline dirençli pnömokok
(PBP dönüşümü)
• Metisiline dirençli stafilokok
(PBP dönüşümü)
• Vankomisine dirençli enterokok
(D-alanin değişimi)
Direncin araştırılması
• Disk difüzyon testleri
• Dilüsyon testleri
• E-test
• Otomatize sistemler (vitek, ATB,...)
• Biyokimyasal testler (beta laktamaz)
• Genotipik metodlar
(PCR, sekans, DNA probları,...)
Disk difüzyon
Disk difüzyon
Disk difüzyon
Disk difüzyon
Disk difüzyon
Mikrobisidal etkinlik ölçümü (Dr.M.Yılmaz)
Minimal inhibitör konsantrasyon (MIC): in vitro antimikrobiyal ajanın
organizmanın üremesini inhibe ettiği en düşük konsantrasyonu
Antibiyotik
dilüsyonlarını
ekle
İnokülasyon
Buyyon
&
ekle
inkübasyon
0.05 0.1
antibiyotiksiz
kontrol
0.2
0.4 0.8
MIC
1.6
3.2
6.3 12.5 25
50
µg/ml
Minimal inhibitör konsantrasyon (MIC): in vitro antimikrobiyal ajanın
organizmanın üremesini inhibe ettiği en düşük konsantrasyonu
0.05 0.1
0.2
0.4 0.8
1.6
3.2
6.3 12.5 25
50
Petrilere
ekim yap
Petrileri
inkübe et
Minimum bakterisidal konsantrasyon (MBC):
in vitro antimikrobiyal ajanın organizmayı öldürdüğü en düşük
konsantrasyon
Dilüsyon (MİK)
(Mikrodilüsyon)
Agar tarama
• Agar dilüsyon
tarama
• 6 mg/L oksasilin
MRSA/ORSA
tarama
E-test
OTOMATİZE
SİSTEMLER
Biyokimyasal testler
• Beta laktamaz araştırılması (Nitrosefin)
* H.influenzae
* Moraxella catarrhalis
* Gonokok
* Anaeroplar
*Enterokoklar
* S.aureus
Moleküler metodlar
Günümüzde
Antibiyotik Araştırmaları
• Günümüzde direnç “dinamik”
• Antibiyotiklerin
farmakokinetik/farmakodinamik
etkileşimi
• Her antibiyotik için farklı uygulamalar
FK/FD
“Antibiyotiklerin iki önemli etkisi vardır:
Tedavi amaçlı, enfeksiyöz organizmayı
öldürür, ancak hastalık yapmayan diğer
organizmalara da zarar vererek
ekosistemin çeşitliliğine, bütünlüğüne ve
duyarlı - dirençli organizma dengesine
zarar verir..…
Levy, 1997
Antibiyotik direnç genlerinin moleküler yayılımı
Donör organizmanın 3 antibiyotik direnç geni var:
1.
Kromozomda PBP’ olarak gösterilen düşük afiniteli
2.
Küçük nonkonjugatif plazmidde Beta laktamaz
3.
Konjugatif plazmide bağlı transpozonda Tet R
Transformasyon: ölen bakteriden çıplak DNA transferi
Kromozom üstünde homolog gen tranferiyle
Transdüksiyon: direnç genlerinin (küçük
plazmid) bakteriyofajlarca taşınması
Konjugasyon: Donör ve alıcı arasında fiziksel
temas gerektirir, konjugatif plazmidler
geçerken nonkonjugatiflerin de geçtiği
gösterilmiştir
Transpozon: kendi rekombinasyon enzimlerini
taşıyan özel DNA dizileri (transposase), bir
yerden bir yere sıçrar (nonhomolog
bölgelere)
Antibiyotik direnci
• Hastanelerde ve toplumda
dirençli bakterilerle oluşan
infeksiyonlar artmaktadır!
• Yakın gelecekte mucize
antibiyotikler
beklenmemektedir
Antibiyotik direnci
• “The pandemic of antibiotic
resistance”
Anderson RM. Nature Med 1999
• “...post-antibiotic era”
Cohen ML Science 1992
Direncin Seleksiyonu
IMS 2000 Verileri Türkiye
25
20
15
10
5
0
333.4 Trilyon
AB
AR
ULSER
RA
PSK
VIT
AGRI
AG
Çevreye sürekli olarak antibiyotik
yayılıyor...
90 – 180 milyon kg/yıl antibiyotik
(25 MİLYAR tam tedavi kürü ~ 4 kişi
başı/yıl)
Tarım alanında insanlardan 10 X fazla
(hayvanlarda insanlardan 30 X daha
fazla)
VRE
Antibiyotiklerin floraya
etkisi
Overuse of high stability antibiotics and its consequences in
public and environmental health.
Acta Microbiol Pol. 2003;52(1):5-13.
Zdziarski P, Simon K, Majda J.
In this paper the ecological aspects of widespread antibiotic consumption are
described. Many practitioners, veterinarians, breeders, farmers and analysts
work on the assumption that a antibiotics undergo spontaneous degradation. It is
well documented that the indiscriminate use of antibiotics has led to the water
contamination, selection and dissemination of antibiotic-resistant organisms,
alteration of fragile ecology of the microbial ecosystems. The damages caused
by the overuse of antibiotics include hospital, waterborne and foodborne
infections by resistant bacteria, enteropathy (irritable bowel syndrome, antibioticassociated diarrhea etc.), drug hypersensitivity, biosphere alteration, human and
animal growth promotion, destruction of fragile interspecific competition in
microbial ecosystems etc. The consequences of heavy antibiotic use for public
and environmental health are difficult to assess: utilization of antibiotics from the
environment and reduction of irrational use is the highest priority issue. This
purpose may be accomplished by bioremediation, use of probenecid for
antibiotic dosage reduction and by adoption of hospital infections methodology
for control resistance in natural ecosystems.
Kinolon dirençli E.coli
CDC NNIS - VRE
insidensi
30
23,9
25
25,6
21,8
20
15,4
15
11,5
ICU
Non-ICU
12,812
10
5,3
2,9
5
0
4,8
0,40,3
89
91
93
95
97
99
Gelecek...
İlk VRSA olgusu
• 40 y, DM, PVH,KBY,hemodiyalizli
hasta
• MRSA bakteremisi nedeniyle 2 ay
vankomisin tedavisi
• Kateter ucunda VRSA,diyabetik ayak
doku kültürü VRSA,VRE
Antibiyotik çağının sonu mu?
M.Ö. 2000
Al, bu kökü ye.
M.S. 1000
O kök kötü. Gel, bu duayı oku.
M.S. 1850
O dua batıl inanç. Al, bu iksiri iç.
M.S. 1920
O iksir yanlış. Al, bu hapı yut.
M.S. 1940
O hap etkisiz, bu antibiyotiği al
M.S. 1980
O antibiyotik de etkisiz,
diğer antibiyotiği al
M.S. 2000
Antibiyotikler artık işe yaramıyor(?)
"Al, bu kökü ye..."
Akılcı antibiyotik
kullanımı
“ÖNCE ZARAR VERME”
DÜŞÜN !!!!!!
SOR ???
İYİ YILLAR, İYİ BAYRAMLAR !!!