1
TERMODİNAMİK
Enerji değişimini/akışını/hareketini inceler.
a- Sistem ile çevre arasında madde ve her türlü enerji alış-verişi olmayan sistemlere
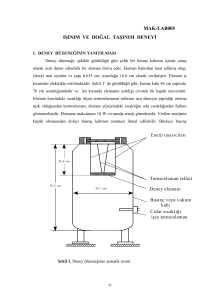
“yalıtılmış (izole) sistem“ denir. (Adyabatik sistem: Örnek termos)
b-Sistem ile çevre arasında hem madde hem de enerji alış-verişi olabilen sistemlere “açık
sistem” adı verilir.
c- Sistem ile ortam arasında madde alış-verişi olmayıp, enerji alış-verişi bulunan sistemlere
“kapalı sistem” denir.
Termodinamiğin Birinci Kanunu
Enerjinin korunumu kanunudur. E = Q + W
Enerji yok edilemez ancak bir biçimden diğerine dönüşür.
Evrenin enerjisi sabittir.
E = Q - W
E = Q + W
2
BİR SİSTEMİN İŞİ
W=F.l
F
Pdış =
veya
A
F = Pdış A
W = Pdış A l
W = Pdış V
Tersinmez (Irreversible) İş
W = Pdış V
Tersinir (Reversible) İş
dW = Pdış dV
Pdış = Piç + dP
2
V2
1
V1
dW
V2
Pdış dV = (Piç dP) dV
V1
V2
W Piç dV
V1
Wmax
V2
V1
V
2
nRT
dV
dV n R T
V
V
V1
Wmax n R T
V2
V1
dV
V
Wmax 2,303 n R T log
V2
V1
=> Wmax 2,303 n R T log
P1
P2
3
Örnek: 25 0C’de basıncı 6 atm olan ve ideal kabul edilen 2 litre hacmindeki bir kapta bulunan
gaz, 1 atmosfer dış basınca karşı izoterm olarak genişletilmektedir. Son hacmi 10 litre olan bu
gazın yaptığı işi
a) Tersinmez olarak,
b) Tersinir olarak hesaplayınız
Çözüm:
a) W = Pdış V = Pdış (V2 - V1)
W = 1 (10 - 2) = 8 L atm
Wmax
b) PV=nRT
6.2=n.0,082.298 => n= 12/24.436= 0,491 mol
10
2,303 n R T log
= 2,303(0,491)(0,082)(298)log 5= 19,31 L. atm
2
ENTALPİ
QP = H = Sabit basınçta alınan veya verilen ısı entalpi olarak isimlendirilir.
H = E + P V
4
Örnek: 1 mol buz 0 oC ve 1 atmosfer basınç altında eridiği zaman 1440 cal ısı
almaktadır. Buzun ve suyun molar hacimleri sırasıyla 0,0196 ve 0,018 litredir. Aynı şartlarda
54 gram buzun erimesi halinde H ve E değerlerini hesaplayınız.
Çözüm:
H = QP =
54
1440 4320 cal
18
E = QP - P V = 4320 - 1 (0,018 - 0,0196) (1,987/0,082)
E = 4320 - (-0,0388)
E = (4320 + 0,0388) cal
TERMOKİMYA
C(grafit) + O2 (g)
ΔH o298 = - 94,05 kcal
CO2 (g)
ΔH o25 = ΔH o (ürünler) - ΔH o (girenler)
Örnek
C2H5OH (s) + 3 O2 (g)
2 CO2 (g) + 3 H2O (s)
reaksiyonun standart reaksiyon ısısını hesaplayınız. Standart oluşum entalpileri etil alkol,
karbondioksit ve su için sırasıyla - 66360 cal/mol, - 94050 cal/mol ve - 68320 cal/mol olarak
verilmiştir.
Çözüm:
Ho = 2 ΔH o(CO 2 ) 3 ΔH o(H2O) - ΔH o(C2H5OH)
Ho = 2 (-94050) + 3 (-68320) - (-66360)
Ho = -326700 cal
Hess Kanunu
5
C(k) + ½ O2 (g)
CO(g) + 1/2 O2 (g)
C(k) + O2 (g)
CO (g)
CO2 (g)
H = - 26416 cal
H = - 67636 cal
H = - 94052 cal
CO2 (g)
Molar Isılar
Bir maddenin bir gramının sıcaklığının 1 oC yükseltmek için verilmesi gereken ısı miktarına
“özgül ısı” ya da “ısı kapasitesi”
Bir maddenin 1 molünün sıcaklığını 1oC değiştirmek için verilecek ya da alınacak ısı
miktarına “molar ısı” veya “molar ısı kapasitesi” adı verilmektedir.
Q P ΔH
ΔT ΔT
Q
ΔE
CV = V
ΔT ΔT
CP =
sbt P
sbt V
H = n CP (T2 - T1) = n CP T
E = n CV (T2 - T1) = n CV T
Qp=mCT
Örnek: 2,8 gram azot (N2) gazı sabit basınç altında 0 oC den 1000 oC ye kadar
ısıtılıyor. Söz konusu sıcaklık aralığında azotun molar ısısı sabit olup, CP = 6,76 cal/mol dür.
Buna göre entalpi değişimini hesaplayınız.
Çözüm:
H = n CP T
H = (2,8/28) (6,76) (1273 - 273)
= 676 cal.
6
TERMODİNAMİĞİN İKİNCİ KANUNU
Kelvin-Planck
Termodiamik bir çevrim gerçekleştirerek çalışan bir makinenin sadece bir kaynaktan ısı alıp,
net iş üretmesi olanaksızdır.
Clausius İfadesi
Termodinamik bir çevrim gerçekleştirerek çalışan bir makinenin, başka hiçbir enerji
etkileşiminde bulunmadan, düşük sıcaklıktaki bir cisimden ısı alıp yüksek sıcaklıktaki bir
cisme ısı vermesi olanaksızdır.
Joule
İş kolaylıkla diğer enerji biçimlerine dönüştürülebilir fakat diğer enerji biçimlerini işe
dönüştürmek o kadar kolay değildir. İş daima % 100 verimle ısıya dönüştürülebilir.
Birinci yasa, bir hal değişimi sırasında enerjinin korunumunu gerektirir.
İkinci yasa, hal değişimlerinin hangi yönde gerçekleşebileceklerini belirler. Olayların
kendiliğinden olup olamayacağını inceler.
TERMODİNAMİĞİN ÜÇÜNCÜ KANUNU
Bütün katı tam kristal maddelerin entropileri mutlak sıfır sıcaklığında sıfırdır.
Entropi: Düzensizliğin ölçüsüdür.
Q
ΔS rev
T
ΔS
298
Te
CP (k)
O
ΔS
Te
C
P (k)
O
ΔS
ΔH e
Te
0
CP dT
T
T
T
dT ΔH e b
dT ΔH b
dT
CP (s)
CP (g)
T
Te
T
Tb
T
Te
Tb
dT
T
Sıcaklık değişimi
Hal değişimi
Örnek : Asetik asidin donma noktasında erime ısısı 43,2 cal/g ve kaynama noktasında
buharlaşma ısısı 96,8 cal/g dır. Sıvı asetik asidin ortalama özgül ısısı 0,46 cal/g olduğuna göre,
bir mol asetik asid donma noktasında katı halden 1 atmosfer basınç altında kaynama
noktasında buhar haline geçtiğindeki entropi değişmesini hesaplayınız. Asetik asit için Te =
16,6 oC, Tb = 118,3 oC ve molekül ağırlığı 60 dır.
7
Çözüm:
Te
S S C P (k)
0
T
0
0
O
T
T
dT ΔH e b
dT ΔH b
dT
C P (s)
C P (s)
T
Te
T
Tb
T
Te
Tb
T
He b
dT H b
ΔS
C P (s)
Te Te
T
Tb
ΔS
He
T H
C p ln 2 b
Te
T1 Tb
ΔS
43,2 . 60
391,3 96,8 . 60
0,46 . 60 ln
391,3
289,6
289,6
S = 8,95 + 164,76 - 156,45 + 14,841 = 32,10 cal/mol derece
Standart mutlak entropileri veren tablolardan faydalanarak bir kimyasal reaksiyonun standart
entropi değişimi hesaplanabilir.
aA+bB
cC+dD
reaksiyonunun standart reaksiyon entropisi, reaksiyona giren ve çıkan maddelerin standart
mutlak entropilerinden faydalanarak,
ΔS 0298 (c S0C d S0D ) - (a S0A b S0B )
Örnek : 25 oC de standart mutlak entropi katı Ca için 9,95 cal/mol derece, oksijen
gazı için 49,0 cal/mol derece ve CaO(k) için 9,5 cal/mol derece olarak verildiğine göre,
aşağıdaki reaksiyonun reaksiyon entropisini hesaplayınız.
Ca (k) + ½ O2 (g)
CaO (k)
Çözüm:
S 0298 S 0CaO - (S 0Ca ½ S0O2 )
S 0298 9,5 - (9,95 + 49/2)
S 0298 - 24,95 cal/mol derece
8
PROBLEMLER
Problem (1): Bir sisteme 150 kJ değerinde ısı veriliyor. Sistem buna karşılık 78000 J
değerinde bir iş yaptığına göre, sistemin iç enerji değişimini hesaplayınız.
Çözüm:
E = Q - W = 150 - 78 = 72 kJ
Problem (2): 25 oC sıcaklıkta ve 760 mm Hg cıva basıncında bulunan 100 g azot gazı
0,1 atmosferlik bir dış basınca karşı genişletilmektedir. Bu sırada gazın yaptığı işi
hesaplayınız.
Çözüm:
V1 =
n R T (100 / 28) (0,082) (298)
=
= 87,4 L
P1
1
V2 =
n R T (100 / 28) (0,082) (298)
=
= 872,7 L
P2
(76 / 760)
W = Pdış V = (0,1) (872,7 - 87,4) = 78,53 L atm
Wmax 2,303 n R T log
V2
V1
Problem (3): 2,00 atmosfer basınç altında 22,4 litre hacim kaplayan bir gaz, sabit
basınç altında ısıtılarak hacmi 44,8 litreye çıkarılıyor. Bu hal değişmesinde sisteme verilen ısı
3800 cal olduğuna göre, bu hal değişimine ait iç enerji değişmesini hesaplayınız.
Çözüm: Sistemdeki değişiklik sabit basınçta meydana getirildiği için, sisteme verilen
ısı QP olmaktadır. 1 L atm = 24,2 cal/L atm
E = QP - P V
E = 3800 - 2 (44,8 - 22.4) (24,2)
E = 2715,8 cal
9
Problem (4): Aşağıda verilen reaksiyonun 25 oC deki entalpi değişimini hesaplayınız.
Standart oluşum ısıları sırasıyla Na2CO3 (k) için - 271000 cal/mol, HCl için - 22063 cal/mol,
NaCl (k) için - 98232 cal/mol, CO2 için - 94052 cal/mol ve H2O (s) için - 68317 cal/mol olarak
verilmiştir.
Na2CO3 (k) + 2 HCl (g)
2 NaCl (k) + CO2 (g) + H2O (s)
Çözüm: Reaksiyonda yer alan her bir bileşiğin oluşum ısıları verildiğine göre,
reaksiyonun standart entalpisi (9.29) eşitliği yardımı ile hesaplanabilir.
Ho = (2H o(NaCl) ΔH o(CO2 ) ΔH o(H2O) ) - (H o(Na 2CO3 ) 2H o(HCl) )
Ho = [2 (- 98232) + (- 94052) + (- 68317)] - [(- 271000) +
2 (- 22063)]
Ho = - 43707 cal/mol
Problem (7): 2 mol argon gazı sabit basınç altında 25 oC den 225 oC ye kadar
ısıtılmaktadır. Argon için CP = 4,987 cal/mol K olduğuna göre bu ısıtma işlemi esnasındaki
entropi değişimini hesaplayınız.
Çözüm:
Entropi değişiminin hesaplanması için n mol gaz için göz önüne alınmalıdır.
ΔS n
T2
T1
498
C P dT
dT
2 4,987
T
T
298
10
S = (2) (4,987) ln
498
298
S = 5,12 cal/K
Problem (9-8): Sıvı suyun ve su buharının sabit basınçtaki molar ısı kapasiteleri
sırasıyla 17,97 cal/K, 8,58 cal/K ve suyun 100 oC ve 1 atm basınçtaki buharlaşma ısısı 9710,6
cal/mol olduğuna göre, bir mol suyun 1 atm basınçta 25 oC den 250 oC ye kadar ısıtılması
sırasındaki entropi değişimini hesaplayınız.
Çözüm: Toplam entropi değişimi, her bir basamakta meydana gelen entropi
değişmelerinin toplamı olacağından,
Tb
ΔS C P (s)
T1
T
2
dT ΔH b
dT
C P (g)
T
Tb
T
Tb
S = C P (s) ln
Tb ΔH b
T
C P (g) ln b
T1
Tb
T2
S = 17,97 ln
373 9710,6
523
8,58 ln
298
373
373
S = 4,034 + 26,033 + 2,900
S = 32,967 cal/mol K
SORULAR
1: 25 oC ve 4 atmosfer basınç altında bulunan bir ideal gazın hacmi 3 litredir. Bu gaz 1 atm
dış basınca karşı 12 litreye kadar genişletiliyor.
a) Olayı irreversibil kabul ederek sistemin yaptığı işi,
b) Reversibil kabul ederek sistemin yaptığı işi hesaplayınız.
11
2: 1,20 gram karbon dioksitin 10 oC den 0 oC ye kadar soğutulması sırasındaki entropi
değişmesini hesaplayınız. Söz konusu sıcaklık aralığında CO2 için molar ısı CP = 9,31 cal/mol
K olarak verilmiştir.
3: Sıcaklığı - 5 oC olan 100 gram buz ısıtılarak 100 oC de su buharı haline getiriliyor. Buz için
CP = 0,5 cal/g K, su için CP = 1 cal/g K, He = 80 cal/g ve Hb = 540 cal/g olarak verilmiştir.
Buna göre, sistemde meydana gelen toplam entropi değişimini hesaplayınız.