ÇUKUROVA ÜNİVERSİTESİ
FEN BİLİMLERİ ENSTİTÜSÜ
YÜKSEK LİSANS TEZİ
Belkız AKKUŞ
NÜKLEOBAZ İÇEREN KARIŞIK LİGANDLI METAL FOSFİN
KOMPLEKSLERİ SENTEZİ
KİMYA ANABİLİM DALI
ADANA, 2009
ÇUKUROVA ÜNİVERSİTESİ
FEN BİLİMLERİ ENSTİTÜSÜ
NÜKLEOBAZ İÇEREN KARIŞIK LİGANDLI METAL FOSFİN
KOMPLEKSLERİ SENTEZİ
Belkız AKKUŞ
YÜKSEK LİSANS TEZİ
KİMYA ANABİLİM DALI
Bu tez 14/01/2009 Tarihinde Aşağıdaki Juri Üyeleri Tarafından Oybirliği/
Oyçokluğu İle Kabul Edilmiştir.
İmza.....................................
İmza...................................
İmza..................................
Prof.Dr.Osman SERİNDAĞ Prof.Dr. Bilgehan GÜZEL
Prof.Dr. Burhan ARIKAN
DANIŞMAN
ÜYE
ÜYE
Bu tez Enstitümüz Kimya Anabilim Dalında hazırlanmıştır.
Kod No:
Prof.Dr. Aziz ERTUNÇ
Enstitü Müdürü
Bu Çalışma Çukurova Üniversitesi Araştırma Projeleri Tarafından Desteklenmiştir.
Proje No: FEF2008YL11
Not: Bu tezde kullanılan özgün ve başka kaynaktan yapılan bildirişlerin, çizelge, şekil ve fotoğrafların
kaynak gösterilmeden kullanımı, 5846 sayılı Fikir ve Sanat Eserleri Kanunundaki hükümlere tabidir.
ÖZ
YÜKSEK LİSANS TEZİ
KARIŞIK LİGANDLI GEÇİŞ METAL KOMPLEKSLERİNİN SENTEZİ
VE KARAKTERİZASYONU
ÇUKUROVA ÜNİVERSİTESİ
FEN BİLİMLERİ ENSTİTÜSÜ
KİMYA ANABİLİM DALI
Danışman : Prof. Dr. Osman SERİNDAĞ
Yıl : 2009, Sayfa : 70
Jüri : Prof. Dr. Osman SERİNDAĞ
Prof. Dr. Bilgehan GÜZEL
Prof. Dr. Burhan ARIKAN
N,N-bis(difenilfosfinometil)aminoter-bütil, [(Ph2PCH2)2NC(CH3)3)] ve N,Nbis(difenilfosfinometil)aminometil, [(Ph2PCH2)2NC(CH3))] ligandları Pt(II) ve Pd(II)
metal kompleksleri inert azot atmosferinde Schlenk metoduna göre sentezlenmiştir.
Sentezlenen bis-aminometil komplekslerinin nükleobazlarla (timin,urasil,teofilin)
reaksiyonu ile de farklı ligand içeren geçiş metali kompleksleri sentezlenmiştir.
Sentezlenen komplekslerin karakterizasyonu için ( FT-IR, 1H-NMR,
13
C ve
31
P-
NMR) teknikleri kullanılmıştır
Anahtar Sözcükler: Difenil fosfin, aminometilfosfin, karışık ligand, nükleobaz,
metal kompleksleri
I
ABSTRACT
MSc THESIS
SYNTHESIS OF TRANSITION METAL COMPLEXES WITH MIXED
LIGANDS AND CHARACTERIZATION
DEPARTMENT OF CHEMISTRY
INSTITUE OF NATURAL AND APPLIED SCIENCES
UNIVERSITY OF ÇUKUROVA
Adviser : Prof. Dr. Osman SERİNDAĞ
Year : 2009, Pages : 70
Jury : Prof. Dr. Osman SERİNDAĞ
Prof.Dr. Bilgehan GÜZEL
Prof. Dr. Burhan ARIKAN
N,N-bis(diphenylphosphinomethyl)aminoter-buthyle,
dppatbu
ve
N,N-
bis(diphenylphosphinomethyl)aminomethyl, [(Ph2 PCH2)2NC(CH3))] ligands were
prepared and its Pd (II), Pt (II) complexes were synthesized by Schlenk Technique
under nitrogen atmosphere. The synthesis of transition metal complexes with mixed
ligands were prepared by the interaction of palladium and platinum complexes with
nucleobases. The products were characterized by using FT-IR, 1H,
13
C and
NMR Spectrometers.
Keywords: Diphenylphosphines, Aminomethylphosphines, Mixed ligand,
nucleobase, Metal complexes.
II
31
P-
TEŞEKKÜR
Çalışmalarım boyunca yardımlarını esirgemeyen ve beni yönlendiren danışmanım
Sayın Prof. Dr. Osman SERİNDAĞ’a sonsuz teşekkürü bir borç bilirim. Deneysel
çalışmalarım boyunca desteğini gördüğüm Dr. Mustafa Keleş’e, ve diğer laboratuar
arkadaşlarıma teşekkür ederim. Ayrıca kimya bölümü öğretim üyeleri ve bölümümüz
çalışanlarından Uzman Serkan KARACA ve Teknisyen Kemal Can’a maddi ve
manevi desteklerinden dolayı teşekkür ederim.
Yüksek lisans çalışmalarım süresince beni motive eden, her türlü yardımlarını
benden esirgemeyen Tuğba Keleş’e, aileme ve eşim Mehmet Akkuş’a sonsuz
şükranlarımı sunarım.
III
İÇİNDEKİLER
SAYFA NO
ÖZ…………………………………………………………………………………...
I
ABSTRACT………………………………………………………………………...
II
TEŞEKKÜR………………………………………………………………………..
III
İÇİNDEKİLER ………...…………………………………………………………...
IV
ÇİZELGELER DİZİNİ……………………………………………………………
VI
ŞEKİLLER DİZİNİ………………………………………………………………..
VII
EKLER DİZİNİ………………………………………………………………........
IX
SİMGE VE KISALTMALAR……………………………………………………..
X
1.Giriş ……………………………………………………………………………....
1
1.1. Fosfinler ……………………………........................................................
4
1.1.2. Aminometilfosfinler………………………………………...
4
1.2.
Fosfin
Ligandları
ve
Karışık
Ligand
İçeren
Metal
Kompleksleri....................................................................................
8
1.2.1 DNA Bazları Hakkında Genel Bilgi………………………….
10
1.2.2. Nükleobazların Biyolojik Önemi……………………………
13
1.3. Pürin ve Pirimidinin Yapısı ve Reaksiyonları………………………….
15
1.3.1. Diazinlerin Yapısı………………………………………..
16
1.3.2.Diazinlerin Reaksiyonları ..................................................
16
1.3.3.Purin Türevlerinin Reaksiyonları………………………...
17
2. ÖNCEKİ ÇALIŞMALAR……………………………………………………....
19
3. MATERYAL VE METOD……………………………………………………...
30
3.1.Materyal…………………………………………………………………...
30
3.1.1. Sentezler ve Karakterizasyonlarında Kullanılan
Materyaller………………...................………..........................
30
3.1.2. Kullanılan Araç ve Gereçler........................................................
31
3.2. Metod……………………………………………………………………..
31
3.2.1. Ligand ve Komplekslerin Sentezi...............................................
31
IV
3.2.1.1. [Ph2P(CH2OH)2]Cl Sentezi (1)......................................
t
32
3.2.1.2 ( Ph2PCH2)2NBu , (dppa bu) Sentezi (2)........................
32
3.2.1.3 [ PtCl2(Ph2PCH2)2NBu ] Kompleksinin Sentezi (3)……
33
3.2.1.4 [(Ph2PCH2)2NCH3] (dppam) Sentezi (4)………………
34
3.2.1.5 [PdCl2(Ph2PCH2)2NCH3] Kompleksinin Sentezi (5)….
34
3.2.2. Karışık Ligandlı Metal Komplekslerinin Sentezi……………..
34
3.2.2.1 [Pt (dppatbu) (tym)2] Kompleksinin Sentezi (6)……….
34
3.2.2.2. [Pt(dppatbu) (urasil)2] Kompleksinin Sentezi (7)………...
36
3.2.2.3. [Pt (dppatbu ) (teofilin)2] Kompleksinin Sentezi (8)……..
37
3.2.2.4. [Pd(dppam ) (timin)2] Kompleksinin Sentezi (9)……..
39
4. BULGULAR VE TARTIŞMA…………………………………………….........
41
4.1. Infrared Spektrumlarının Değerlendirilmesi...............................................
43
4.2. 1H NMR Spektrumlarının Değerlendirilmes ………………..............……. 45
4.3 13C NMR Spektrumlarının Değerlendirilmesi…………….............……….
4.4 31P NMR Spektrumlarının Değerlendirilmesi …………..............………...
5. SONUÇLAR VE ÖNERİLER………………………………….……………..…
46
47
49
Kaynaklar…………………………………………………………………………....
50
Özgeçmiş…………………………………………………………………………….
54
Ekler………………………………………………………………………................
55
V
ÇİZELGELER DİZİNİ
Çizelge 1.1.
SAYFA NO
Pt nükleobaz komplekslerinin
tümörlü
hücredeki büyüme
miktarları…………………………....……………………………. 10
Çizelge 4.1.
Sentezlenen Komplekslerin FT-IR Spektrumları (cm-1)..............
Çizelge 4.2.
Sentezlenen
Metal
Komplekslerinin
1
H-NMR
Spektrum
Değerleri.........................................................................................
Çizelge 4.3
Sentezlenen
Metal
Komplekslerinin
13
C-NMR
45
46
Spektrum
Değerleri.......................................................................................... 47
Çizelge 4.4
Sentezlenen
Metal
Komplekslerinin
31
P-NMR
Spektrum
Değerleri.........................................................................................
VI
48
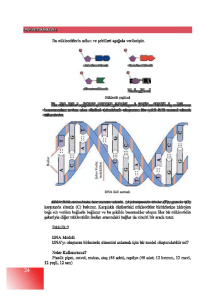
ŞEKİLLER DİZİNİ
SAYFA NO
Şekil 1.1
DNA bazlarındaki güçlü nükleofilik atomlar……………………………
1
Şekil 1.2
cis-platinin DNA’ya bağlanması………………………………………...
2
Şekil 1.3
Metalin DNA’ ya koordine olabildiği bazlardaki güçlü
nükleofilik atomlar………………………………………………………
3
Şekil 1.4
Bazı Fosfin Ligandlarının Yapıları……………………………………...
5
Şekil 1.5
Aminometilfosfinin sentezlenme tepkimeleri…………………………..
5
Şekil 1.6
Tris(anilinometil)fosfin
ve
1,
3,
5-
diazafosforinan’nın
yapısı........................................................................................................
6
Şekil 1.7
Antitümöral Özellik Gösteren Ajanlar………………………………….
7
Şekil 1.8
Antimikrobiyal Özellik Gösteren Kompleksler………………………...
8
Şekil 1.9
DNA bazlarının metal kompleksler.........................................................
8
Şekil 1.10
(a) pBr322 (b) pBr-cisplatin (c,d,e,f) pBr – nükleobaz kompleksleri…
9
Şekil 1.11
Pürin
ve
pirimidinlerin
genel
moleküler
yapıları
ve
numaralandırılmaları……………………………………………………
11
Şekil 1.12
Başlıca pürin ve pirimidin molekülleri ve onların organik isimleri…….
11
Şekil 1.13
Bakteri ve bakteriyofaj DNA’sında yer alan bazı minör bazlar………..
12
Şekil 1.14
Ökaryot DNA ‘sında yer alan bazı minör bazlar……………………….
12
Şekil 1.15
Pürin metabolizması esnasında ortaya çıkan bazı pürin molekülleri…...
12
Şekil 1.16
Çeşitli bitkilerde bulunan metilenmiş pürin bileşikleri…………………
13
Şekil 1.17
Pürin ve pirimidinlerde görülen keto-enol tautomerizasyonu………….
13
Şekil 1.18
Sentetik pirimidin ve pürin analogları………………………………….
14
Şekil1.19
6-azoüridin ve 8-azoguanin açık yapısı………………………………...
15
Şekil 1.20
Pürin analogları…………………………………………………………
15
Şekil 1.21
Pirimidinin rezonansları………………………………………………...
16
Şekil1.22
Purinin türevleri......................................................................................
17
Şekil 2.1
Antitümör Özellik Gösteren Kompleksler………………………….......
19
Şekil 2.2
Pd(II) teofilin kompleksi………………………………………………..
20
Şekil 2.3
Altın (I) kompleksi……………………………………………………...
21
Şekil 2.4
9-metil adenin bazının deprotonlanması ile siklik trimer yapı oluşumu..
21
VII
Şekil 2.5
9-metil adenin bazının Pt kompleksiyle oluşturabileceği tüm yapılar….
22
Şekil 2.6
Rutenyum nükleobaz kompleksleri…………………………………….
22
Şekil 2.7
[RuIIICl4(DMSO)(H-Hypoxanthine)] kristal yapısı……………………
23
Şekil 2.8
[RuIIICl4(DMSO)[H-(N6-butyladenine)]] kristal yapısı……………….
23
Şekil 2.9
Pd(II) Nükleozid kompleksleri………………………………………...
23
Şekil 2.10
Pd(II) kompleksinin rezonans yapıları…………………………………
24
Şekil 2.11
Pirimidin bazlarının türevlendirilmiş yapıları…………………………..
24
Şekil 2.12
Pd(II) ile pirimidin bazlarının oluşturduğu kompleksler……………….
25
Şekil 2.13
a) PtII(hmp)XCl b) PtII(hmp)X2 yapısı (X= adenin,9-etilguanin,7metilguanin,sitozin,1-metilsitozin veya sitodin………………………...
Şekil 2.14
Pt –nükleobaz
26
kompleksinin oluşma basamakları (X= adenin,9-
etilguanin,7-metilguanin,sitozin,1-metilsitozin veya sitodin…………...
26
Şekil 2.15
PtII(hmp)(9-etilguanin)2](NO3)2 yapısı…………………………………
27
Şekil 2.16
Adenin bazı ile oluşturulan Pt(II) kompleksi…………………………...
27
Şekil 2.17
Pt(II) ve Pt(IV) ile gunanin ligandının oluşturduğu kompleks.(N9
tarafından bağlanma oluşmuştur………………………………………..
Şekil 2.18
28
Pt(IV) ile guanozin ligandıyla oluşturduğu kompleks (N7 üzerinden
bağlanması)……………………………………………………………... 28
Şekil 2.19
Pürin anologlarının Pt (II) ile oluşturduğu kompleksler………………... 29
Şekil 3.1
Fosfonyum Tuzu Eldesi............................................................................ 32
Şekil 3.2
Ligand Sentezi (dppatbu).......................................................................... 33
Şekil 3.3
Pd (II) Metal Kompleksi Sentezi.............................................................. 33
Şekil 3.4
Pt (II)Metal Kompleksi Sentezi................................................................ 34
Şekil 3.5
[Ptl(dppatbu) (tym)2] Kompleksinin Açık Yapısı.................................... 35
Şekil 3.6
[Pt (dppatbu) (urasil)2].. Kompleksinin Açık Yapısı…………………...
37
Şekil 3.7
[Ptl(dppatbu) (teofilin)2] Kompleksinin Açık Yapısı…………………..
38
Şekil 3.8
[Pd(dppam) (timin)2] Kompleksinin Açık Yapısı……………………… 40
Şekil 4.1
Metal fosfin kompleksleri......................................................................... 41
Şekil 4.2
[ Pt (dppatbu ) (timin)2] Kompleksinin Açık Yapısı……………………. 42
VIII
Şekil 4.3
[ Pt (dppatbu ) (urasil)2] Kompleksinin Açık Yapısı……………………
42
t
Şekil 4.4
[ Pt (dppa bu ) (teofilin)2 ] Kompleksinin Açık Yapısı………………… 42
Şekil 4.5
[ Pd (dppam) (timin)2 ] Kompleksinin Açık Yapısı……………………
IX
43
EKLER DİZİNİ
SAYFA NO
Ek. 1.1.
[Pt(dppatbu) (timin)2 ] Kompleksinin 1H-NMR Spektrumu………………
55
Ek. 1.2.
[Pt(dppatbu) (urasil 2] Kompleksinin 1H-NMR Spektrumu ………………
56
Ek. 1.3.
[Pt (dppatbu) (teofilin)2] Kompleksinin 1H -NMR Spektrumu …...…........
57
Ek. 1.4.
[Pd (dppam) (timin)2] Kompleksinin 1H-NMR Spektrumu Spektrumu ….
58
Ek. 1.5.
[ Pt(dppatbu) (timin)2 ] Kompleksinin 13C-NMR Spektrumu……...……...
59
t
13
Ek. 1.6.
[Pt(dppa bu) ) (urasil 2] Kompleksinin C-NMR Spektrumu……....….…
60
Ek. 1.7.
[Pt (dppatbu) (teofilin)2] Kompleksinin 13C -NMR Spektrumu …….....…
61
Ek. 1.8.
[Pd (dppam) (timin)2] Kompleksinin
Ek. 1.9.
[Pt(dppatbu) (timin)2 ] Kompleksinin 31P-NMR Spektrumu.....................
63
Ek. 1.10.
[Pt(dppatbu) ) (urasil 2] Kompleksinin 31P -NMR Spektrumu…………….
64
Ek. 1.11.
[Pt (dppatbu) (teofilin)2]Kompleksinin
P-NMR Spektrumu ……….......
65
Ek. 1.12.
31
[Pd (dppam) (timin)2] Kompleksinin P-NMR Spektrumu ……………...
66
Ek. 2.1
[Pt(dppatbu) (timin)2 ] Kompleksinin FT-IR Spektrumu………………...
67
Ek. 2.2
[Pt(dppatbu) (urasil 2] Kompleksinin FT-IR Spektrumu………………….
68
Ek. 2.3
[Pt (dppatbu) (teofilin)2] Kompleksinin FT-IR Spektrumu………………
69
Ek. 2.4
[Pd (dppam) (timin)2] Kompleksinin FT-IR Spektrumu…………………
70
X
13
C-NMR Spektrumu …..…...…....
31
62
SİMGELER VE KISALTMALAR
dppatbu
: N, N-bis(difenilfosfinometil) aminoter-butil
Ar
: Aril
[PtCl2COD] : Diklor (1, 5-sikloktadien) platin(II)
[PdCl2COD] : Diklor (1, 5-sikloktadien) paladyum(II)
DMSO
: Dimetilsülfoksit
DMSO-d6
: Dötero-dimetilsülfoksit
CDCl3
:
FT-IR
: Fourier Dönüşümlü Infrared Spektroskopisi
1
: Proton nükleer magnetik rezonans spektroskopisi
H-NMR
31
P-NMR
Kloroform
: Fosfor-31 nükleer magnetik rezonans spğektroskopisi
g
: Gram
L
: Litre
ml
: Mililitre
°C
: Santigrat derece
δ
: Kimyasal kayma
ppm
: Milyonda bir birim
MA
: Mol ağırlığı
d
: Dublet (ikili)
s
: Singlet (tekli)
z
: Zayıf
o
: Orta
ş
: Şiddetli
XI
1. GİRİŞ
Belkız AKKUŞ
1. GİRİŞ
Kanser hastalığı günümüzde her ülkede, her yaşta görülebilen, coğrafi sınır
tanımayan, sosyal statü ve gelir durumu ayrımı yapmayan evrensel bir sorun
niteliğindedir. Dünya Sağlık Örgütü (WHO) verilerine göre, her yıl dünyada 6
milyondan fazla insan kansere yakalanmaktadır. Kanser, en basit ve en anlaşılır
şekilde; kontrolden çıkan anormal hücrelerin düzensiz çoğaldığı hastalıklar grubu
olarak tanımlanabilir. Kanser hücresi normal hücrelerden farklı olarak, kontrolsüz ve
sınırsız çoğalma, kan ve lenf yolu ile uzak organlara giderek üreme, orada yerleşerek
koloni yapma yeteneğine sahiptir. Dahası canlının doğal bağışıklık sisteminden
kaçabilmekte ve ölüme sebep olabilmektedir. Bu denli ölümcül bir hastalığın tedavi
edilebilmesi oldukça önemlidir ve günümüzde bu amaçla çeşitli yöntemler
kullanılmaktadır. Bu yöntemler arasında kimyasal tedavinin (kemoterapi) yeri
oldukça önemlidir. Bu amaçla birçok organik molekülün yanı sıra geçiş metali
komplekslerinin de kullanıldığı bilinmektedir (Yang, 1999).
Cis-platin olarak da bilinen diamindikloroplatin(II) kompleksi, kemoterapide en
fazla kullanılan geçiş metali komplekslerindendir. Ancak cis-platinin yan etkileri
bilim adamlarını yeni metal kompleksleri araştırmaya ve özellikle çeşitli amin
türevlerini kullanarak cis -platine benzer yapılar üzerinde çalışmaya itmiştir. Cisplatinin antikanser etkisi hakkındaki genel kanaat; molekülün DNA’ ya bağlanması
sonucunda DNA replikasyonunun engellendiği yönündedir. Bahsedilen DNA
inhibisyonu memeli hücrelerinde kanıtlanmıştır (Takahara, 1996).
Pirimidinler
Pürinler
3
4
3
5
N
2
O
1
N
H
5
O
NH2
3
HN
2
6
Sitozin, C
O
4
1
N
H
CH3
5
3
2
6
Timin, T
HN
O
NH2
O
O
4
5
1
6
1
HN
6
5
N
3N
4
N
H
Urasil, U
H2 N
1
N
7
5
N
4
N
H
8
8
2
N
H
6
7
2
N3
9
Guanin, G
9
Adenin, A
Şekil 1.1. DNA bazlarındaki güçlü nükleofilik atomlar
Cis-platin sulu ortamda hidroliz olur ve kloro gruplarının ikisi de metalden
ayrılır. Böylelikle molekülün hücre duvarından geçebilmesini sağlayan katyonik cis-
1
1. GİRİŞ
Belkız AKKUŞ
platin meydana gelir. (Yongwon, 2007) cis-platin DNA’nın en zengin elektron
yoğunluğuna sahip bazlarından guanin (G)’in N7 donörüne bağlanır, diğer bir
bağlanma yeri ise adenin (A) N7 donörüdür(Takahara, 1996). cis-platinin yanı sıra
diğer anti kanser ajanları da tercihen guanin bazına bağlanır (Yang, 1999). cis-platin
DNA’ ya üç şekilde bağlanabilir.
1) İplikler arası; platin köprüleri DNA’ nın karşıt zincirleri arasında oluşabilir.
2) İplik içi; tek bir zincirde iki bitişik DNA bazıyla (guanozin) köprü oluşabilir.
3) tek bir bazın bifonksiyonel atağı ile; guaninin O-6 ve N-7 atomları cis-platin ile
şelat oluşturabilir.
H3N
G
Pt
H3N
G
Protein
G Pt
G
H3N
Pt
A
G
G
NH3
NH3
NH3
NH3
Pt
NH3
NH3
G
Pt
G
NH3
Şekil 1.2. cis-platinin DNA’ya bağlanması.
Cis-platinin DNA ile yaptığı bağlanmalar Şekil 1.2’ de gösterilmiştir. Hidroliz
olan cis-platin daha sonra DNA’daki guanin bazına bağlanır ve sonunda komşu
guanin ile de bağlanarak halka kapanır ve bir GG makro şelatı oluşur. GG
makroşelatında iki guanozin ligandı dihedral konformasyonda ve aralarında 26o açı
ile koordine olurlar. GG platinasyonu DNA’ nın 35-40o bükülmesine sebep olur.
Bükülmüş DNA’ ya yüksek hareketli grup proteinleri sıkıca bağlanırlar ve normal
transkripsiyonu engellerler. Daha sonra DNA, endonükleaz enzimleriyle kesme ve
programlanmış hücre ölümü gerçekleşir (apoptosis) (Takahara, 1999). Cis-platinin
2
1. GİRİŞ
Belkız AKKUŞ
normal hücrelere zarar vermemesinin sebebi muhtemelen normal hücrelerdeki
onarım enzimlerinin hücreyi zarardan korumasıdır.
Cis-platinin oldukça toksik olması (nefrotoksisite ototoksisite), daha geniş
spektrumlu bir antikanser ilacı sentezleme amacı ve kanser hücrelerinin cis-platine
karşı tekrarlanan tedavi sırasında direnç göstermesi, ikinci nesil platin bileşikleri
olarak da adlandırılan karboplatin ve nedaplatin gibi biyolojik olarak aktif çeşitli
Pt(II) kompleksleri bulunmasına sebep olmuştur (Mckeage, 2000).
Ağırlıklı
görüşlere
göre,
DDP’nin
DNA’
ya
bağlanması
DNA’
nın
replikasyonunu engellediği önerilmiştir. Bu DNA inhibisyonu memeli hücrelerinde
kanıtlanmıştır. Bu olay RNA sentezinden önce meydana gelir ve istenilen protein
sentezlenemez. E.coli filamentasyonu üzerine yapılan çalışmalarda direkt ve endirekt
olarak DDP’ nin bakterinin DNA’ sına bağlandığına dair kanıtlar vardır. (Sadler
2003)
Pirimidinler
Pürinler
3
4
3
5
N
2
O
1
N
H
Sitozin, C
5
O
NH2
3
HN
2
6
O
4
1
N
H
Timin, T
CH3
5
3
HN
2
6
4
5
1
HN
5
6
N
Urasil, U
6
H2N
6
7
1
5
N
7
N
8
8
2
1
N
H
O
NH2
O
O
3N
4
N
H
2
N3
4
N
H
9
9
Guanin, G
Adenin, A
Şekil 1.3. Metalin DNA’ ya koordine olabildiği bazlardaki güçlü nükleofilik atomlar
Cis-DDP DNA’ ya bağlanırken kloro gruplarının ikiside metalden ayrılır. Cisizomerinde DNA ile bağ uzunluğu 3,3 Ǻ iken trans- platinde 5,0 Ǻ dur. Cis-DPP,
DNA’ nın en zengin elektron yoğunluğuna sahip guanozin (G), N7 donörüne
bağlanır, diğer bir bağlanma yeri ise adenozin (A) bazının N7 donörüdür. Cis-DDP
ve diğer anti kanser ajanlarıda tercihli olarak guanozin bazına bağlanır. Cis-DDP’ nin
NA’ ya bağlanması üç yolla gerçekleşir (Şekil 1.9 ) interstrand, platin köprüleri
DNA’ nın karşıt zincirleriyle oluşur; intrastrand, tek bir zincirde iki bitişik DNA
bazıyla (muhtemelen guanozin bazlarıyla) köprü oluşur; ve tek bir bazın
bifonksiyonel atağı ile oluşur. Deneysel sonuçlara göre, her dörtyüz cis-DDP ile
3
1. GİRİŞ
Belkız AKKUŞ
DNA bağlanmasının yalnızca birinde interstrand çapraz-bağları oluşur. Tek bir bazın
bifonksiyonel atağında ise guanozinin O-6 ve N-7 fonsiyonları DDP ile şelat
oluşturabilir
1.1. Fosfinler
Yapılan çalışmalar sonucunda, cis-platin türevlerinin yanı sıra tersiyer fosfin
ligandlarını (PR3) içeren metal komplekslerinin de kanser tedavisinde kullanılabilme
potansiyellerinin oldukça yüksek olduğu tespit edilmiştir (McKeage, 2002).
Fosfinlerin genel formülleri PR3 olup R = alkil, aril ve hidrojendir. PH3, (fosfin),
PMe3 (trimetilfosfin), PPh3 (trifenilfosfin)), fosfitlerin genel formülleri ise P(OR)3
olup her iki yapıda olduğu gibi fosfor üzerindeki bir çift ortaklanmamış elektron
(dönor elektronlar) ile metale koordine olmaktadır. Şekil 1.1.’de görüldüğü gibi
farklı yapıda çok sayıda fosfor içeren çok dişli ligandlarda örnek verilebilir (A. M.
LaPointe 1999). Fosfin içeren metal kompleksleri arasında aminometilfosfin (R2PCH2-N) komplekslerinin antikanser özeliklerinin incelenmesine yönelik çalışmaların
sayısı yok denecek kadar azdır.
Bir geçiş metaline bir fosfin ligandının bağlanabilme yeteneği genellikle onun
sterik ve elektronik özelliklerine bağlıdır. Sterik ve elektronik özellikleri
değiştirilerek bir fosfin ligandının geçiş metalleri ile oluşturacağı komplekslerinin,
katalitik reaksiyonlardaki aktivitesi ve seçiciliği arttırılabilir. Bu kompleksler tek
dişli ligandlara göre daha kararlı kompleksler olup belirli bir ürünün katalizlenmesi
açısından stereogenik ve stereospesifik katalizörlerdir.
1. 1. 2 Aminometilfosfinler
Coates & Hoye (1960) tarafından uygulanan Mannich reaksiyonu ile
aminometilfosfin ligandları ile metal komplekslerinin sentezinde yeni bir kapı
açmıştır. P-C-N bağı içeren bu aminometilfosfinler, formaldehitin sekonder fosfin ile
(RR’PH) reaksiyonundan elde edilmektedir (Şekil 1.4.).
4
1. GİRİŞ
Belkız AKKUŞ
H
N
R2P
H2
C
(CH2)n
R2P
PR2
Aminofosfin
PR2
RHN
Alkilfosfin
PR2
Aminometilfosfin
(R)2P
P(R)2
N
N
P(R)2
(R)2P
1,1,2,2-tetrakis((dialkilfosfino)metil)hidrazin
R=-CH3, -Ph
Şekil 1.4. Bazı Fosfin Ligandlarının Yapıları
Alkil veya aril eklentili fosfinlerin, R3P, (R = alkil, aril) sentezlenmesi için PH3
veya Ph2PH’deki H ile yerdeğiştirme veya PCl3 ve Ph2PCl gibi klorlu fosfinlerin
stokiyometrik miktarda LiR ile tepkimesi sonucu elde edilebilir. Böylelikle -mono, di ve -trifosfinler sentezlenebilir.
P-CH2-P bağı ya da aminometilfosfin P-C-N bağı içeren fosfinler hakkında
günümüzde oldukça fazla sentez yapılmıştır. Aminometilfosfin, yaygın olarak
diklormetan, tetrahidrofuran veya toluen çözücüleri kullanılarak Ph2PH, amin ve
formaldehitin aşırısı ile tepkimeye sokularak elde edilir (Şekil 1.5).
RR’PH + RR’NH + HCHO
RR’PCH2NRR’ + H2O
Ph2P
Ph2PH
+ HCHO + H2NR
N
R
Ph2P
RnP(CH2OCOMe)3-n
1.KOH, MeOH/H2O
2.R2NH
,RnP(CH2NR2)3-n
Şekil 1.5 . Aminometilfosfinin sentezlenme tepkimeleri.
5
1. GİRİŞ
Belkız AKKUŞ
Elde edilen aminometilfosfin anilin, etanol veya asetonlu ortamda hidroksil ile yer
değiştirerek tetrakis(anilinometil)fosfonyum klorür (THPC) oluşturmaktadır (1.3).
Asetonlu ortamda trietilamin ile 1, 3, 5- diazafosforinan ve elde edilen ligand
amonyak ile tris(anilinometil)fosfin oluşmaktadır.
P(CH2NHPh)3
P(CH2OH)3 + PhNH2
(1.2)
NH3
THPC + PhNH2
P(CH2NHPh)4 CI
(1.3)
NEt3
Ph
N
P-CH2NPh
(1.4)
N
Ph
Şekil 1.6. Tris(anilinometil)fosfin ve 1, 3, 5- diazafosforinan’nın yapısı.
İleri amino asit türevlerinin sentezi (metanol veya asetonitril) optiksel olarak aktif
hidroksimetil fosfinleri kullanılarak denenmiştir. Aminoasit sübstitüe edilmiş
ligandların siklohekzil türevleri kendi fosfin oksitleriyle birlikte hazırlanmıştır.
Aminometil fosfinlerin hidrojenasyon, hidroformülasyon gibi reaksiyonlara katalitik
etkisi bulunduktan sonra çalışmalar oldukça hız kazanmıştır. Aminometil fosfinlerin
Metal kompleksleri özellikle geçiş metal komplekslerinin sentezi arttırılmıştır. Pt(II)
ve Rh(I) komplekslerinin bazıları hidroformülasyon ve hidrojenasyon katalizörleri
olarak incelenmiştir.
Fosfin ligandlarının ve komplekslerinin antitümör ve antibakteriyel etki gösterdiğinin
deneysel olarak saptanması bu tür bileşiklerin sentezine ve farmakolojik
özelliklerinin incelenmesine var olan ilgiyi daha da artırmıştır. Bu çerçevede yapılan
araştırmalarda altın(I) fosfin türevlerinin canlı ortamında murine tümör modellerine
karşı önemli aktivite gösterdiği tespit edilmiştir ( Mc Keage 2002).
İlk olarak trietilfosfinaltın(I)tetraasetatotiyoglikoz (Auranofin) ve trifenilfosfin
altın(I) klorür kompleksleri üzerinde yoğunlaşılmıştır. Auranofin kompleksi, P388
6
1. GİRİŞ
Belkız AKKUŞ
lösemili fare hücresinin DNA polimeraz enzimini inhibe ederek farenin yaşama
süresini uzatmıştır (Mirabelli 1985-Simon 1981). Ancak daha sonra tetrahedral
altın(I)
kompleksleri
([Au(dppe)2]Cl)
ve
olan
bis[1,2-bis(difenilfosfino)etan]altın(I)
klorür
bis[1,2-bis(di-n-piridilfosfino)etan]altın(I)
klorür
([Au(dpype)2]Cl) komplekslerinin murine tümor modellerine karşı daha geniş bir
spektrumda daha yüksek aktiflik gösterdiği tespit edilmiştir (Berner-Price 19881999).
Bis[1,2-(difenilfosfino)etan]altın(I)
klorür
([Au(dppe)2]Cl),
in
vitro,
mitokondri DNA’sına bağlanarak, DNA-protein çapraz bağlanmasını engellemekte
ve böylece P388 lösemi hücreleri üzerine antimitokondriyal etkide bulunmaktadır
(Dong 1997) (Şekil 1.5).
+
+
Ph2P
PPh2
Au
Ph2P
R2P
Cl
PPh2
R2
P
PR2
Au
R2P
Cl
PR2
R2
P
Au
P
R2
R= m- veya p-piridil
[Au(dppe)2]Cl
R2
P
R2
P
2Cl-
Au
P
R2
P
R2
+2
P
R2
R=o-Piridil
Şekil.1.7. Antitümöral Özellik Gösteren Ajanlar
Potansiyel olarak antitümör etki göstermesi beklenen metal komplekslerinin,
fosfolipid yapısındaki hücre zarından geçebilmesi için belirli bir yağ severliğe
(lipofiliklik) sahip olması gerekmekte ve bu amacı gerçekleştirebilmek için
genellikle katyonik kompleksler kullanılmaktadır (McKeage 2002). Auronofinde
olduğu gibi yağ sever (lipofilik) özellikteki (glikoz gibi) moleküller yardımıyla da
yağ severlik (lipofiliklik) sağlanabilmektedir. (Reedijk 1999) Sitotoksik platin
komplekslerinin hedefi olarak çoğunlukla DNA görülür.
Ayrıca [(Ph2PCH2)2NCH3] (dppam) ligandının Au(I), Cu(I), Ag(I) ve Co(II)
kompleksleri sentezlenmiş antimikrobiyal etkileri incelenmiş ve 1200 mg/disk
derişimde bütün komplekslerin antimikrobiyal aktivite gösterdiği tespit edilmiştir
(Şekil 1.7.) (Uruş 2005).
7
1. GİRİŞ
Belkız AKKUŞ
Ph2
P
N
Me
Ph2
P
Me
M
Ph 2
P
Ph2
P
N
X
N
P
Ph 2
Ph2
P
Cl
Co
Cl
Me
M: Ag, X: NO 3 (1)
M: Au, X: Cl (2)
M: Cu, X: Cl (3)
[CoCl2dppam] (4)
Şekil 1. 8. Antimikrobiyal Özellik Gösteren Kompleksler
1.2. Fosfin Ligandları ve Karışık Ligand İçeren Metal Kompleksleri
Metal komplekslerinin biyolojik yönünün incelenmeye başlanmasıyla bazı
komplekslerin bilinmeyen biyolojik tepkimelerde kullanılacağı tespit edilmiştir.
Şekil 1.9. DNA bazlarının metal kompleksleri.
Aminofosfin Pt(II) komplekslerinin DNA bazları olan guanin ve timine
halka-açılma (ring-opening) reaksiyonlarıyla bağlanabildiği ve kanserli hücrelere
karşı sitotoksik etki gösterebildiği bilinmektedir. DNA ve RNA yı oluşturan pürin ve
pirimidin bazları ve bunların türevleri olan bazları içeren kompleksler sentezlenmiş
ve bunların anti tümör etki gösterdiği saptanmıştır. Özellikle metal-fosfin
komplekslerine pürin ve pirimidin bazları takılarak elde edilen karışık ligandlı
kompleksler üzerine birçok çalışma yapılmış.
Kansere karşı nükleik asitlerin çeşitli modifikasyonları yapılmaktadır. Modifiye
bazlar ve DNA anologları arasında geri bağlamalarla yeni yapılar ve oligonükleotid
de yeni fonksiyonel gruplar oluşturulmuştur.
Biyolojik aktivitesi güçlü olan bazı geçiş metal kompleksleri Pt, Pd, Zn, Au terapatik
amaçla kullanılmaktadır. Cis Pt-Cl2 antikanser terapati de çok iyi bilinmektedir ve
8
1. GİRİŞ
Belkız AKKUŞ
kanser hücrelerinin büyümesini engeller. Örneğin Zn kompleksleri DNA’da ki
guanin-sitozin (GC) bloğunu tanımakta seçicidir ve hedef DNA yı bağlayıp inhibe
eder (Romanelli,2005). Ayrıca fosfin ligantları Ag(I), Au(I), Sn(IV) anti kanser, anti
HIV ve antimitokondriyal ajanlardır. Nükleobazların (timin, sitozin, urasil) Pt(II) ve
Pd(II) ile oluşturduğu karışık ligandlı komplekslerin DNA ile etkileşimi ve antitümör
özellikleri Atomik force microscopy de incelendiğinde Pt komplekslerinin DNA
Pbr322 tümörlü hücresini modifikasyona uğratır. Yeni Pt komplekslerinin HL 60
karşı etki gösterdiği gözlenmiştir. (Ruiz,2006).
Şekil 1.10. (a) pBr322 tümörlü hücre (b) pBr-cisplatin (c,d,e,f) pBr – nükleobaz
kompleksleri
9
1. GİRİŞ
Belkız AKKUŞ
Çizelge1.1. Pt- nükleobaz komplekslerinin tümörlü hücredeki büyüme miktarları
Kompleks
24 saat
72 saat
Cisplatin
15.610
2.150
[Pt(dmba)(1-
0.729
0.692
0.643
0.674
1.614
0.935
Methy)(L)
[Pt(dmba)(1Meura)(L)]
[Pt(dmba)(1Methy)(L)
Çizelge 1.1.’ de gösterilen sonuçlarla kıyaslandığında 24 saat ve 72 saat sonunda
platinin nükleobazla olan kompleksinde,
cisplatin kompleksine göre tümörlü
hücrelerin daha az büyüdüğü gözlenmiştir. Nükleobazlarla elde edilen sonuçların
cisplatinden daha iyi çıkması bu tür komplekslere olan ilgiyi arttırmıştır (Ruiz,2006).
1.2.1. DNA Bazları Hakkında Genel Bilgi
Pürin ve Pirimidinler:
DNA ve RNA’lar oluşturan nükleotidler, aromatik heterosiklik bileşikler olan
pürin ve pirimidinlerin birer türevidirler. Konsantrasyon bakımından hücrede daha
yoğun bulunmasından dolayı birçok kitapta bunlar
nükleobaz olarak da
adlandırılmaktadır.
Pürin ve pirimidinler planar konfigürasyonda bulunan moleküllerdir. Azot
içeren bu heterosiklik moleküllerin numaralandırılması oldukça önemli olup
pürinlerde saat yönünün tersi ve pirimidinlerde saat yönüne doğru yapılır. Pürin ve
pirimidin bazları hidrofobik ve nötral pH’da suda çözünemeyen bir karaktere
sahiptirler. Alkali pH’da pürin ve pirimidinler yüklü hale geçmekte ve sudaki
çözünürlüğü artmaktadır. Hidrofobik karakterlerinden dolayı bunların düzlemsel
yapılarının üst üste yığılması (para yığını gibi) van der Waals ve dipol-dipol
etkileşimleri sonucu meydan gelir. Baz yığılmaları ile ortaya çıkan etkileşimler su ile
10
1. GİRİŞ
Belkız AKKUŞ
teması azaltmaktadır ve bu nükleik asitlerin 3- boyutlu yapısının stabilizasyonunda
oldukça önemlidir Sahip oldukları heterosiklik yapılarından dolayı pürin ve pirimidin
bazları
260
nm’deki
ışığı
absorblama
özelliği
de
gösterirler.
Şekil 1.11. Pürin ve pirimidinlerin genel moleküler yapıları ve numaralandırılmaları
Nükleik asitler 5 majör heterosiklik bazdan meydana gelirler. Buradaki majör ve
minör kavramları bazların fizyolojik önemlerine göre değil hücre içerisindeki
kullanışlarına bağlıdır. RNA ve DNA polinükleotidleri için kullanılan majör
heterosiklik bazlar pürinlerinden adenin ve guanin, pirimidinlerden ise sitozin, timin,
urasil’dir.
Şekil 1.12. Başlıca pürin ve pirimidin molekülleri ve onların organik isimleri
11
1. GİRİŞ
Belkız AKKUŞ
Prokaryot ve ökaryotlarda bir de minör bazlar bulunur. 5-metilsitozin hem bakteriyel
hem
de
insan
DNA’sında
bulunur.
Bakteriyofaj
DNA’sında
yer
alan
hidroksimetilsitozin aynı zamanda bazı bakteri ve virüslerde bulunmaktadır.
Şekil 1.13. Bakteri ve bakteriyofaj DNA’sında yer alan bazı minör bazlar
Bundan başka memeli RNA’sında bulunabilen minör bazlar içerisinde, mesajcı RNA
da yer alan N6, N6 –dimetiladenin ve N7-metilguanin(Şekil.1.14) ile taşıyıcı RNA da
bulunabilen daha farklı türevler vardır.
Şekil. 1 14. Ökaryot DNA ‘sında yer alan bazı minör bazlar.
Ayrıca hücrede serbest olarak bulunan hipoksantin ve ksantin (Şekil.1.15), adenin ve
guanin metobolizmasında ortaya çıkmaktadır. Ürik asit ise pürin katabolizması
sırasında ortaya çıkan okside son ürün olup insanlarda idrar yolu ile atılmaktadır.
12
1. GİRİŞ
Belkız AKKUŞ
Şekil 1.15. Pürin metabolizması esnasında ortaya çıkan bazı pürin molekülleri
Bitkilerde farmakolojik özelliklere sahip başka heterosiklik bazlar bulunmaktadır.
Metilenmiş ksantin bunlar için iyi bir örnektir: kafein(1, 3, 7-trimetilksantin)
kahvede, teofilin(1,3-dimetil ksantin) çayda, teobromin (3, 7-dimetil ksantin) kakao
da bulunur. (Şekil.1.15.)
Şekil. 1 16. Çeşitli bitkilerde bulunan metilenmiş pürin bileşikleri
Keto-Enol Tautomerizasyonu: Heterosiklik bileşiklerin aromatik karakterleri
nedeniyle pürin, pirimidin ve onların türevlerinin amino ve okso grupları, tautomerik
bir
denge
içerisindedirler.
Tautomerleri
amino/imino
ve
keto/enol(laktam/laktim)çiftleri şeklinde olup yapılarındaki farklılıklar Şekil.1.16’da
gösterilmektedir. Bu tautomerik çiftler ortamın pH’sına göre değişir. Fizyolojik
şartlarda denge amino ve laktam formu yönündedir.
Şekil. 1 17. Pürin ve pirimidinlerde görülen keto-enol tautomerizasyonu
13
1. GİRİŞ
Belkız AKKUŞ
1.2.2. Nükleobazların Biyolojik Önemi
Pürin ve pirimidin bazları antitümör ajanlarıdır. (Lakomska, 2008) Özellikle pürin ve
pirimidin anologları kullanılmaktadır. Kimyasal olarak sentezlenen pürin ve
pirimidin anologları, klinik ve tıbbi araştırmalarda oldukça önemlidir. Heterosiklik
halkada veya şeker kısmında değişiklik yapılıp canlılara uygulandığında hücrenin
spesifik bir yerine yerleşmesi halinde toksik etki göstermektedir. Böyle bir etki iki
şekilde ortaya çıkar:
1) Özellikle nükleik asit sentezinde yer alan spesifik enzimlerin sentetik pürin veya
pirimidin analogları tarafından inhibisyonu veya,
2) Sentetik pürin veya pirimidin analoglarının, metobolitlerin nükleik asitlerinin içine
yerleşmesi ve burada baz çiftini bozarak genetik bilgi aktarımını etkilemesi.
Bu tür analoglar özellikle onkologların ilgilerini çekmektedir. Bunlar içerisinde 5floro veya 5-iyodo bileşiklerin urasil veya deoksiüridin türevleri, timin veya timidin
anologları olarak çalışırlar.
O
I
HN
S
SH
O
O
HOH2C
OH
H
N
N
H
5-iodo-2'-deoksiüridin
H
N
F
N
N
HN
NH
O
N
N
H
O
H2N
5-fluorouracil
6-Mercaptopurin
N
N
6-Thioguanine
Şekil.1.18. Sentetik pirimidin ve pürin analogları
Hem 6-tiyoguanin hem de merkaptopürin’de tiyol grubu 6. pozisyonda bulunan
hidroksil grubu ile yer değiştirmiştir ve klinikte geniş kapsamlı kullanılmaktadır. 5veya 6-azaüridin, 5- veya 6-azasitidin ve 8-azoguanin(Şekil1.18) analoglarındaki
nitrojen atomu, heterosiklik yapıda bir karbon atomu ile yer değiştirmiştir ve klinikte
kullanılmaktadır.
14
1. GİRİŞ
Belkız AKKUŞ
Şekil.1 19. 6-azoüridin ve 8-azoguanin açık yapısı.
Pürin
anologlarından
4-hidroksipirazolopirimidin
(allopurinol)
gut
tedavisinde
kullanılmakta olup pürin biyosentezini ve ksantin oksidaz aktivitesini inhibe eder.
Azotiyoprin, 6-merkaptopürine katabolize olmakta ve immünolojik rejeksiyonu
baskılaması için organ transplantasyonlarında kullanılmaktadır. Bir başka pürin analoğu
olan teofilinin anti-kanser etkinliğinde değişik mekanizmaların rol alması mümkündür.
Teofilin kanser tedavisi dışında astım bronşit kronik akciğer hastalıkları ve kalp
yetmezliği tedavisinde tıpta önemli bir yere sahiptir.(Romerosa,2000)
Şekil 1.20. Pürin anologları
1.3 Pürin ve Pirimidinin Yapısı ve Reaksiyonları
15
1. GİRİŞ
Belkız AKKUŞ
Pürin ve pirimidinler diazinler denilen, altılı halkada ikişer tane azot atomu içeren
bileşiklerdir ve birbiri ile izomer üç tane diazin vardır, piridazin(1,2-Diazin)
Pirimidin(1,3-diazin) ve Pirazin(1,4-diazin) dir.
1.3.1. Diazinlerin Yapısı: Diazinlerde hem karbon atomları hem de azot atomları sp2
hibridize haldedir. Düzlemsel olan halkaların aromatik karakterleri, karbon ve azot
atomlarının birer elektron taşıyan ve halka düzlemine dik durumdaki p orbitallerinin
,halka düzleminin üstünden ve altından girişim yapmaları ile oluşan ve topluca 6π
elektronuna (ya da 3π bağına)karşın olan elektron bulutundan ileri gelir. Herbir azot
atomunun bağ oluşmu için kullanılmayan ve iki elektron taşıyan sp2hibrit orbitalleri
,bu azot atomlarının ortaklanmamış elektron çiftlerini oluşturur ve diazinlerin
bazikliğinden bu elektron çiftleri sorumludur.
N
N
N
N
N
N
N
N
Şekil 1. 21. Pirimidinin rezonansları
1. 3. 2 Diazinlerin Reaksiyonları
a)Diazinlerin asitle reaksiyonu:Piridazin asitli ortamda piridazinyum katyonuna
dönüşür.
+H+
N
N
N
N
H
b)Alkil halojenürlerle:Diazinler alkil halojenürler ile monokuaterner tuzlar
oluşturmak üzere reaksiyon verirler.örneğin;
16
1. GİRİŞ
Belkız AKKUŞ
+CH3I
N
N
N
N
Pirimidin
I
H3C
1-metilpirimidinyum iyodür
c) Nükleofil reaktiflerle:Pirazin,sıvı NH3 içinde NaNH2 ile oda sıcaklığında 2aminopirazin oluşturur.
N
N
NH3
NaNH2
N
N
NH2
2-aminopirazin
Pirazin
1. 3. 3. Pürin türevlerinin reaksiyonları: Birleşmiş pirimidin-imidazol halka
sistemi “Pürin” adı ile bilinir. Pürin türevi olan “Urik Asid” birçok hayvanlarda
metobolizmada oluşan bir üründür.Önemli bir urik asid türevi “Ksantin” dir.
Şekil 1. 22. Pürinin türevleri
Kafein, teobramin ve teofilin birer ksantin türevi olup çay kahve ve kakao’da
bulunan önemli alkaloidlerdir.
Aromatik karakterdeki pirazol ve imidazol’de halka karbon atomları elektrofil
substitusyona karşı pirrol’den daha düşük reaktivite gösterirler. Bu durum pirrol’deki
bir =CH- yerine bir azometin girmesiyle oluştuğu düşünülen diazoller ile, benzendeki
17
N
2
N
H2
Oks
1. GİRİŞ
Belkız AKKUŞ
bir=CH- yerine bir =N- girmesiyle oluşan piridin’in karşılaştırması ile anlaşılabilir.
Bir elektrofil reaktif halka azotlarından sadece azometin azotuna bağlanabilir.
İmidazol ve pirazol’lerde kuvvetli bazlar etkisiyle deprotonasyon olasıdır. Pirrol
halkasında bir =CH- yerine bir çifte bağlı azot =N- girmesi bazikliği arttırır.
İmidazol,pirrol’den ve hatta piridinden daha kuvvetli bazdır. İki heteroatomun
birbirine doğrudan doğruya bağlanması baziklikte zayıflamaya neden olmaktadır
(İkizler Aykut 1985).
18
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
2. ÖNCEKİ ÇALIŞMALAR
Ji-Cheng Shi, ve arkadaşları ( 1997), Şeker-fosfin ligandlı altın(I) kompleksleri
[Au(n-MBPA)L] [n-MBPA= metil 4,6-O-benziliden-n-deoksi-n-(difenilfosfino)-aD-altropiranozit, HL= 1H-pirimidin-2-tion (2-pymSH), 3,5-dimetil-1H-pirimidin-2tion (2-pymmSH). 1, n= 2, L=2-pymS; 2, n= 3, L= 2-pymS; 3, n= 2, L= 2-pymmS;
4, n= 3, L= 2-pymmS] sentezlendi ve 1H,
13
C ve
31
P-NMR ve moleküler titreşim
spektrumuyla karakterize edildi. Au kompleksinin X-Ray difraksiyonuyla geometrisi
belirlenmiştir. Au-P bağ uzunluğu 2,256 Ao, Au-S ise 2,306 Ao ve P-Au-S bağ açısı
178,5o ‘ dir. Oniki altın(I)-kiral fosfin komplekside P388 löseminin büyümesini
inhibe etmiştir. En yüksek aktiviteyi 9 numaralı kompleks 10-7 mol.dm-3 derişimde
bile göstermiştir.
HO
O
6
6
O
O
O
O PPh
2
4
OMe
O
3
2
1
HPh2
P
O OH
4
5
5
3
2
Au
1
O
OH
2-MBPA
OMe
PPh2
OMe
3-MBPA
N
S
N
O
[Au(3-MBPA)Cl]
Şekil 2.1. Antitümör Özellik Gösteren Kompleksler
Antonio Romerosa ve Arkadaşları(2000)
Paladyum(II) metalinin tiyo-pürin türevleriyle (8-tiyo teofilin (8-TTH2) ,8- benzil
tiyo teofilin (8-BzTTH), 8-(metil-tiyo teofilin) (8-MTTH) ve tri-fenil fosfinle yaptığı
karışık ligand komlekleslerini sentezlemişler. 31P, 1H , 13C ve X ışınlarını kullanarak
yapıları karakterize etmişler. Sentezlenen bu maddelerin anti tümör etki gösterdiği
19
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
saptanmıştır. Ayrıca astım ve bronşit tedavisinde kullanılan teofilinin bu yöndeki
etkisinin artığı görülmüştür
Şekil 2.2. Pd(II) teofilin kompleksi
F. Novelli, M. Recine, F. Sparatore, C. Juliano (1999), Yedi altın kompleksi
hazırlanmıştır
ve Gram-pozitif ve Gram-negatif bakteriler (Escheria coli,
Pseudomanas aeruginosa, Staphylococcus aureus, Staphylococcus epidermidis),
mantarlar (Candida albicans ve Aspergillus niger) ve protozoa (Trichomonas
vaginalis) karşı (protozoa: tek hücreli canlılar filumu; amipler ve algler örnek
verilebilir) in vitro olarak biyolojik aktivitesi araştırılmıştır. Pseudomanas aeruginosa
haricinde bütün altın(I) kompleksleri test organizmalarına karşı aktif olduğu
bulunmuştur. Birçok durumda minimum inhibitör konsantrasyonları (MIC) 1 mg/ml’
nin altında olduğu görülmüştür. Antimikrobiyal aktivite sadece basitçe altın içeriğine
bağlı değildir, aynı zamanda metale bağlı hem fosfin hem de aminotiyol ligandlarına
20
2. ÖNCEKİ ÇALIŞMALAR
bağlı
olduğu
Belkız AKKUŞ
belirtilmiştir.
Ayrıca
1,2-bis(difenilfosfino)etan-bis(altın(I)
lupinilsülfidhidroklorür(4) ve trietilfosfino altın(I)(2-dietilamino)etilsülfidhidroklorür
(6) kompleksleri rahim kanserine karşı iyi bir antitümör aktivite göstermiştir
.
C2H5
C2H5
N
C2H5
CH2
CH2
(6)
S
Au
P
C2H5
C2H5
H3C
N
N
CH2
C2H5
CH2
S
(7)
Au
P
C2H5
C2H5
Şekil 2.3.Altın (I) kompleksi
Bruno Longato ve arkadaşları (2003), Bu çalışmada dinükleer hidrokso kompleksinin
cis-[L2Pt(m-OH)]2(NO3)2 (L=PMePh2) 9-metiladenin deprotonlanması sonucu
cis(L2Pt(9-meAd)(-H)]3(NO3)3 oluşur. Nükleobazlar N(1) ve N(6) tarafından merkez
atoma bağlanarak siklik trimer yapı oluşur. X-ray ve
31
P,1H,
15
N NMR ile
aydınlatılmıştır Inorganic Chemist Vol. 42, No. 24,
Şekil. 2. 4. 9-metil adenin bazının deprotonlanması ile siklik trimer yapı oluşumu
21
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil. 2. 5. 9-metil adenin bazının Pt kompleksiyle oluşturabileceği tüm yapılar
A.Garcia.Rosa ve arkadaşları (2005); Bu çalışmada Rutenyumun pürin türevleriyle
yapmış olduğu kompleksler incelenmiştir. [RuIIICl4(DMSO)(H-Hypoxanthine)] ve
[RuIIICl4(DMSO)[H-(N6-butyladenine)]] komplekslerinin yapı aydınlatılmasında Xray, elektroforez, AFM yöntemleri kullanılmıştır.
Ru
komplekslerinin
nitrojenlerle
oluşturduğu
kompleksler
yaygın
olarak
kullanılmaktadır. İmidazol yapılar kanserli hücrelerin yayılmasını önleyici ajanlar,
indozal halkalalarla oluşan kompleksler ise kolon tümörlerine karşı klinik testler
sonucu antikanser ilaçları olarak kullanılmaktadır.
22
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil.2.6 Rutenyum nükleobaz kompleksleri
Şekil.2.7. [RuIIICl4(DMSO)(H-Hypoxanthine)] kristal yapısı,
Şekil.2.8 [RuIIICl4(DMSO)[H-(N6-butyladenine)]] kristal yapısı
Alessandra Romanelli Ve arkadaşları (2005),
Bu çalışmada amaç yeni Pd nükleozid kompleksleri oluşturmaktır. Oluşan bu
kompleks potansiyel antikanser ilaçlarında veya sentetik oligonükleotidin içerisinde
metal nükleozid blok oluşturmuştur ve bu da biyolojik deneylerle açıklanmıştır.
Çalışmada timidin bazı ile Pd(PPh3)4 ve KCl kullanılmıştır.
23
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil 2. 9. Pd(II) Nükleozid kompleksleri
Oluşan kompleks aşağıdaki yapılara dönüşebilir.
Şekil 2.10.Pd(II) kompleksinin rezonans yapıları
Jose Ruiz ve Arkadaşları (2006), Bu çalışmada Pt(II) ve Pd(II) bileşiklerinin DNA
bazları olan(Timin,Urasil ve Sitozin) ile oluşturduğu kompleks Atomic force
microscopy ‘de incelendiğinde plasmid DNA pBr322 hücresi
modifikasyona
uğramıştır. Bunun yanı sıra HL-60 (tümörlü hücre) karşı kullanılmıştır.
Karakterizasyonu X- ışınları, 1H, 13C ve 31P NMR ile yapılmıştır
24
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil 2.11.Pirimidin bazlarının türevlendirilmiş yapıları
25
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil 2.12.Pd(II) ile pirimidin bazlarının oluşturduğu kompleksler
Mohammed
S.
Ali
ve
arkadaşları
(2006);
[PtII(hmp)XCl]NO3
ve
II
[Pt (hmp)X2](NO3)2 (hmp=homopiperazin ve X=adenin,9-etilguanin,7-metilguanin,
sitozin, 1-metilsitozin veya sitodin) ile oluşturulmuştur. Karakterizasyonunda
elementel analiz yoluyla
1
H,13C,195Pt NMR kullanılmıştır. X-ray ile yapı
aydınlatıldığında homopiperazindeki iki nitrojen atom Pt’nin iki köşesinde ve diğer
köşelerde nükleobazların köşeleri gelir ve kare düzlem ve C2 moleküler simetrisi
olduğu saptanmıştır.
Şekil.2.13 a) PtII(hmp)XCl b) PtII(hmp)X2 yapısı (X= adenin,9-etilguanin,7metilguanin, sitozin, 1-metilsitozin veya sitodin
Pt(hmp)Cl2 kompleksinde bulunan sekonder aminler cis-platinden daha çabuk
hidroliz olmasını sağlar. Nükleobazla oluşturulan Pt kompleksinin tümör hücrelerine
karşı sitotoksik etki gösterdiği ve kanserli hücrenin replikasyon ve transkripsiyonuna
etki gösterdiği saptanmıştır.
26
2. ÖNCEKİ ÇALIŞMALAR
Pt(hmp)Cl2 + AgNO3
Belkız AKKUŞ
[Pt(hmp)(H2O)Cl]NO3 + AgCl
(A)
[Pt(hmp)(H2O)Cl)]NO3 + X
[Pt(hmp)(X)Cl]NO3 + H2O
(B)
Pt(hmp)Cl2 + 2AgNO3
[Pt(hmp)(H2O)2](NO3)2 +2AgCl
(C)
[Pt(hmp)(H2O)2](NO3)2 +2X
[Pt(hmp)(X)2](NO3)2
(D)
Şekil.2.14 Pt –nükleobaz kompleksinin oluşma basamakları (X= adenin,9etilguanin,7-metilguanin, sitozin, 1-metilsitozin veya sitodin
Şekil.2.15. [PtII(hmp)(9-etilguanin)2](NO3)2 yapısı
Diego Montagner ve Arkadaşları (2007), Bu çalışmada DNA bazlarından
türevlendirilmiş Adenin bazını cis-[(PPh3)2Pt(µ-OH)]2 X2
(X-=NO3) ile karışık
ligand şeklinde bir kompleks sentezlemiş ve karakterize edilmiştir. DNA bazı olan
(9-metiladenin) ligandı 6 nolu amin(NH2) deprotonlanma ile NH şeklinde bağlanır ve
kompleksin +1 şeklinde oluştuğu belirtilmiştir.
Şekil.2. 16. Adenin bazı ile oluşturulan Pt(II) kompleks
27
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Akmal S.Gaballa ve arkadaşları (2008), H2[PtCl6]. 6H2O ve (H3O)[PtCl5(H2O)]
2(18C6). 6H2O (18C6 = 18-crown-6) ile 9-metil guanin,9-etil guanin ve gunozinin
deprotonlanması sonucu PtII ve PtIV ile kompleks oluşturur. Bu çalışmada
nükleobazların hangi taraftan bağlanabileceği açıklanmıştır. Genellikle N9,N7 ve N3
üzerinden bağlanma gerçekleşir.
Şekil.2.17. Pt(II) ve Pt(IV) ile gunanin ligandının oluşturduğu kompleks.(N9
tarafından bağlanma oluşmuştur.)
Şekil. 2.18. Pt(IV) ile guanozin ligandıyla oluşturduğu kompleks (N7 üzerinden
bağlanması)
Iwona Lakomska (2008), Bu çalışmada pürin anologlarının Pt(II) oluşturduğu
komplekslerin antitümör aktiviteleri ve molekül yapıları incelenmiştir. Yapıyı
açıklayabilmek için spektroskopik yöntemler ve kristal yapılarını bağ uzunluğu ve
bağ açılarına göre belirlenmiştir. Çalışmalar tümörlü hücrelerin tedavisinde trans
PtCl2(dmso)(dptp) de cisplatine göre hastaların vücut direncinin daha az düşürdüğü
gözlenmiştir.
28
2. ÖNCEKİ ÇALIŞMALAR
Belkız AKKUŞ
Şekil 2.19.Pürin anologlarının Pt (II) ile oluşturduğu kompleksler
29
3. MATERYAL VE METOD
Belkız AKKUŞ
3. MATERYAL VE METOD
3.1. Materyal
3.1.1. Sentezler ve Karakterizasyonlarında Kullanılan Kimyasallar
·
Azot Gazı (N2) : BOS firmasından temin edilmiştir (% 99,99).
·
Çözücüler: Diklormetan (CH2Cl2), etanol (C2H5OH), metanol (CH3OH)
ligand ve metal komplekslerinin sentezinde kullanıldı.
·
Dietileter
((C2H5)2O):
Sentezlenen
kompleksleri
çöktürmek
için
kullanılmıştır. Analitik saflıkta, Merck firmasından temin edildi.
·
Metanol (CH3OH): Fosfonyum tuzunu sentezlerken, tekrar kristallendirme
aşamasında kullanılmıştır. Analitik saflıkta, Merck firmasından temin edildi.
·
Difenilfosfin (Ph2PH): Fosfonyum tuzunu sentezlerken çıkış maddesidir.
Analitik saflıkta, Fluka firmasından temin edildi.
·
Formaldehit (HCHO): Fosfonyum tuzunun sentezinde kullanıldı. Analitik
saflıkta, Merck firmasından temin edildi.
·
Hidroklorik asit (HCl): Fosfonyum tuzunu sentezinde kullanıldı. Analitik
saflıkta, Riedel-de Haën firmasından temin edildi.
·
Sodyum Sülfat (Na2SO4): Kurutucu olarak kullanıldı. Analitik saflıkta,
Merck firmasından temin edildi.
·
Trietilamin (N(C2H5)3): Ligandların sentezinde kullanılmıştır. Analitik
saflıkta, Merck firmasından temin edildi.
·
ter-bütilamin (H2NC(CH3)3): dppatbu ligandının sentezinde kullanılmıştır.
Analitik saflıkta, Merck firmasından temin edildi.
·
Metilamin H2N(CH3): dppam ligandının sentezinde kullanılacaktır. Analitik
saflıkta, Merck firmasından temin edildi
·
AgClO4:
nukleobaz
ile
oluşturulan
karışık
ligand
komplekslerin
oluşturulmasında kullanılacaktır. Merck firmasından temin edildi
30
3. MATERYAL VE METOD
·
Belkız AKKUŞ
[PdCODCl2], [PtCODCl2]: Pt(II) ve Pd(II) komplekslerinin sentezinde
kullanılmıştır. Analitik saflıkta, Aldrich firmasından temin edildi.
·
Urasil, Timin, Teofilin:
Karışık
ligandlı komplekslerin
sentezinde
kullanılmıştır. Analitik saflıkta, Aldrich firmasından temin edildi
3.1.2. Kullanılan Araç ve Gereçler
·
Cam malzemeler: Beher, geri soğutucu, balon, yandan boyunlu balon,
Schlenk tüpü, ayırma hunisi.
·
Manyetik Karıştırıcılı Isıtıcı: Chiltern Hotplate Manyetik Stirrer HS 31
·
FT-IR: Mattson 1000 cihazı Perkin Elmer Spektrum RXIFT-IR, First Marka
Satellite cihazları.
·
(1H,
31
P,
13
C) - NMR: Bruker-Avance DPX–400 (TÜBİTAK ATAL
Enstrumental Analiz Laboratuarı ANKARA).
3.2.Metod
Bu
çalışmada
litaratüre
göre
N,Nbis(difenilfosfinometil)aminoter-bütil,
[(Ph2PCH2)2NC(CH3)3)], ligandı ve bu ligandın Pt(II) ve Pd(II) geçiş metali
kompleksleri
Schlenk
metoduna
göre
azot
atmosferinde
sentezlenmiştir.
Nükleobazlar (timin, urasi, teofilin) ile sentezlenmiş olan komplekslerin klor
uçlarının kopması ve klorların yerine nükleobazların metale koordine olması ile
karışık ligandlı metal kompleksler elde edilir. Sentezlenen komplekslerin yapıları (
FT-IR, 1H-NMR,
13
C NMR ve
31
P-NMR ) spektrometrik cihazları kullanılarak
aydınlatılmıştır.
3.2.1. Ligand ve Komplekslerin Sentezi
N,N-bis(difenilfosfinometil)aminoter-butil,
[(Ph2PCH2)2NC(CH3)3],
(dppatbu)
ligandı, N,N-bis(difenilfosfinometil)aminometil [(Ph2PCH2)2NCH3], (dppam) ve
metal kompleksleri sentezi azot atmosferinde Schlenk tekniği ile yapılmıştır (Keleş,
31
3. MATERYAL VE METOD
Belkız AKKUŞ
2008). N,Nbis(difenilfosfinometil)aminoter-butil: [(Ph2PCH2)2NC(CH3)3] ligandının
Pt(II)
metal
kompleksleri
ve
N,Nbis(difenilfosfinometil)aminometil:
[(Ph2PCH2)2NCH3] ligandının Pd(II) metal kompleksi sentezlenmiştir.
İlk aşama, fosfonyum tuzu sentezi, ikinci aşama dppatbu ve dppam ligandlarının
sentezi, üçüncü aşama ise metal komplekslerinin sentezi son aşama ise nükleobaz
(timin, urasil, teofilin) ile karışık ligandlı metal komplekslerinin sentezidir.
3.2.1.1. [Ph2P(CH2OH)2]Cl Sentezi (1)
Schlenk düzeneği içerisinde azot atmosferinde karışan difenilfosfin (10 g, 54
mmol) üzerine formaldehit (9 cm3, %40) ve hidroklorik asit (5 cm3, %36)
eklenmiştir. (Şekil 3.1). Bulanık renkte ekzotermik bir karışım elde edildi. Oluşan
karışım oda şartlarında soğurken beyaz katı kristaller oluştu ve süzülüp kaynar
metanolde tekrar kristallendirildi. Metanole geçen az miktardaki fosfonyum tuzu ise
dietileter ile çöktürülmüştür. (15 g, verim% 80) (Serindag, 1995 ).
Ph2PH
Ph2PH
+
+
2HCHO +
2HCHO
+
HCl
[Ph2P(CH2OH)2]Cl
HCl
[Ph2P(CH2OH)2]Cl
Şekil 3.1. Fosfonyum Tuzu Eldesi
3.2.1.2 ( Ph2PCH2)2NBu, (dppatbu) Sentezi (2)
Yandan boyunlu balon içerisinde fosfonyum tuzu, [Ph2P(CH2OH)2]CI, (1 g,) 3,
537 mmol), 30 mL etilalkol-su (1:2) karışımında çözündü, bazik ortam oluşturmak
için 1mL trietilamin (% 99) eklendi. Beyaz bulanık çözeltiye azot atmosferinde 1.8
ml ter-bütilamin eklendi (Şekil.3.2). Karışım geri soğutucu altında 1 saat
32
3. MATERYAL VE METOD
Belkız AKKUŞ
kaynatıldıktan sonra oda koşullarına soğutuldu ve 15 mL diklormetan ile ekstrakte
edildi, Na2SO4 ile kurutuldu. Diklorometan fazına geçen yağımsı fosfin ligandı elde
edildi ( MTeorik: 449 g/mol ), verim 1,21 g (% 80). (Serindag, 1993)
[Ph2P(CH2OH)2Cl]
NEt3/RNH2
H2O/EtOH
(Ph2PCH2)2NR + Et3NHCl + HCHO
R = CH3,-C(CH3)3
Şekil 3.2. Ligand (dppatbu) Sentezi
3.2.1.3 [PtCl2(Ph2PCH2)2NBu] Kompleksinin Sentezi (3)
Yandan boyunlu balon 10 mL CH2Cl2 içerisinde bulunan (0,383g 0,186 mmol)
dppatbu ve (0,305g 0,816 mmol) 10 mL CH2Cl2 [Pt(COD)Cl2] metal tuzu çözeltisi
azot gazı ortamında ilave edildi (Şekil 3.4). Karışım 2 saat boyunca azot
atmosferinde manyetik karıştırıcı ile karıştırıldı. Çözücü hacmi döner buharlaştırıcıda
5 mL’ ye azaltılarak üzerine dietileter ilave edilip metal kompleksinin katı halinde
çökmesi sağlandı. Oluşan katı süzülüp, dietileter ile birkaç kez yıkanarak vakumda
kurutuldu. Beyaz-sarı renkte katı elde edildi (Mteorik: 735,08 g/mol), Verim (% 78 ).
Kompleks; su, etil alkol, dietil eter ve petrol eterinde çözünmezken; kloroform,
diklorometan ve dimetilsülfoksitte çözünmektedir. (Serindağ, 1993)
Ph 2
Ph2
P
P
Cl
Pt
Cl
+
R- N
N
P
Ph2
Pt COD Cl2
(Ph2PCH2)NC(CH3)3
Şekil 3.3. Pt (II)Metal Kompleksi Sentezi
33
(H3C)C
Ph2P
Cl
Pt
Cl
3. MATERYAL VE METOD
Belkız AKKUŞ
3.2.1.4. [(Ph2PCH2)2NCH3] , (dppam) Sentezi (4)
Fosfonyum tuzu, [Ph2P(CH2OH)2]CI, (1,0 g, 3,537 mmol), 30 mL etilalkol-su
(1:2) karışımında çözüldü, bazik ortam oluşturmak için 1 mL trietilamin (NEt3) (%
99) eklendi. Beyaz bulanık çözeltiye azot atmosferinde 1,8 mL metilamin (%40)
eklendi. Karışım geri soğutucu altında 1 saat geri soğutucu altında kaynatıldıktan
sonra ürün 15 mL diklormetan (%99.5) ile ekstrakte edildi ve Na2SO4 ile kurutuldu.
ve diklorometan fazına geçen yağımsı ligand elde edildi. Verim 1,21 g (%80)
(Mteorik: 427,468 g/mol) (Serindag, 1993).
3.2.1.5 [PdCl2(Ph2PCH2)2NCH3] Metal Kompleksi Sentezi (5)
10 mL CH2Cl2 içerisinde bulunan 0.28 g, (0.655 mmol [(Ph2PCH2)2N(CH3)]
ligandı ve (10 mL ) CH2Cl2 (0.080 g, 0.2 mmol) [PdCl2(COD)] metal tuzu çözeltisi
azot gazı ortamında ilave edildi. Karışım 2 saat oda sıcaklığında karıştırıldı. Çözücü
hacmi döner buharlaştırıcıda 5 mL’ ye azaltılarak üzerine dietileter ilave edilip metal
kompleksinin sarı katı halinde çökmesi sağlandı. Oluşan sarı katı süzülüp, dietileter
ile birkaç kez yıkanarak vakumda kurutuldu. Verim: 0.353g (% 88) (Serindağ, 1993)
Ph2
Ph 2
P
P
Cl
Pd
Cl
+
R- N
N
P
Ph2
Pd COD Cl2
(Ph2PCH2)NCH3
Şekil 3.4. Pd (II)Metal Kompleksi Sentezi
3.2.2. Karışık Ligandlı Metal Komplekslerinin Sentezi
3.2.2.1. [Pt(dppatbu) (tym)2] Kompleksinin Sentezi (6)
34
H3C
Ph 2P
Cl
Pd
Cl
3. MATERYAL VE METOD
Belkız AKKUŞ
Yandan boyunlu balon içerisine [PtCl2(dppatbu)] metal kompleksi (0,24 g, 0,32
mmol) ve 20 mL diklormetan eklendi, üzerine (132mg, 0,64 mmol ) AgClO4 eklendi
ve oda sıcaklığında 30 dakika karıştırıldı. Bu karıştırma sonucu beyaz renkli AgCl
çökmesi sağlandı ve bu karışım selit’den geçirilerek süzme işlemi tamamlandı
Süzüntü tek boyunlu balon içerisine alındı üzerine 10 ml etanol ve aseton(1:1)
karışımı içerisinde çözünen timin (80,72 mg 0,64 mmol) ilave edildikten sonra
karışım oda sıcaklığında 10 saat boyunca geri soğutucu altında karıştırıldı. Daha
sonra süzüntünün hacmi döner buharlaştırıcı ile 15 mL’ye düşürüldü. Süzüntü dietil
eter ile çöktürüldü ve çökelek beyaz bantlı Whatman kağıdı ile süzüldü. Dietil eter
ile yıkama işlemi tekrarlandı. beyaz renkli ürün elde edildi (MTeorik: 925,11 g/mol ).
Kompleks 277 oC de erimektedir. Kompleks su, alkol, dietil eter ve petrol eterinde
çözünmezken diklorometan, dimetilsülfoksitte çözünmektedir. (Ruiz, 2006)
O
O
H3C
NH AgClO
N
4
[PtCl2dppatbu] +2
N
H
CH2Cl2
O
(H3C)3
PPh2
Ph2
P
Pt
H
N
N
CH3
O
O
H3C
N
O
NH
Şekil 3.5.[Pt (dppatbu) (tym)2] kompleksi
Ürün: 0,148 g
Teorik: 0,29 g
Verim: % 50
FT-IR (KBr) : 3400 cm-1 (ş, N-H gerilmesi ); 3061.81 cm-1 (o, Ar-CH gerilmesi);
2969 cm-1 (o, Alifatik C-H ); 1737.99 cm-1 (ş, Aromatik C=O gerilmesi ); 1681.64
cm-1 ( o, C=C); 1434 cm-1 ( ş, P-Ar ); 1099-1029.41 (C-N (ter amin) ); 1214.04 cm-1
35
3. MATERYAL VE METOD
Belkız AKKUŞ
(o, Aromatik C-N eğilme titreşimi) 760.04, 741.32, 704.58, cm1 ( ş, monosübstitüe
benzen C-H );
1
H-NMR (DMSO-d6 , 25 oC ppm) : 7.54-7.06 (m, 20H (P-Ph)), 7.35 (s, 2H (H-C6
timin), 5.80 (s,2H (N1-H timin)), 3.75 (s, 4H (N-CH2-P)), 1.84-2.08 (m,9H NC(CH3)3 ve 6H (-CH3-C6 timin
13
C-NMR (DMSO-d6 , 25 oC ppm) : 165.365 (C4 timin), 151.945 (C2 timin),
138.152 (C6 timin), 134.820-128.920 (P-Ph), 108.137 (C5), 25.01(-ter C), 12.22(C6CH3)
31
P-NMR (DMSO-d6 , 25 oC ppm) d = -13.188 [ P-Pt]] J-Pt=2229.6 Hz
3.2.2.2. [Pt(dppatbu) (urasil)2] Kompleksinin Sentezi (7)
Tek boyunlu balon içerisine [PtCl2(dppatbu)] metal kompleksi (0,24 g, 0,32 mmol)
ve 20 mL diklormetan eklendi, üzerine (132mg, 0,64 mmol ) AgClO4 eklenir ve oda
sıcaklığında 30 dakika karıştırıldı. Bu karıştırma sonucu beyaz renkli AgCl çökmesi
sağlandı ve bu karışım selit’den geçirilerek süzme işlemi tamamlandı Süzüntü tek
boyunlu balon içerisine alındı üzerine 10 ml etanol ve aseton(1:1) karışımı içerisinde
çözünen urasil (71,72mg 0,64 mmol) ilave edildikten sonra karışım oda sıcaklığında
10 saat boyunca geri soğutucu altında karıştırıldı. Daha sonra süzüntünün hacmi
döner buharlaştırıcı ile 15 mL’ye düşürüldü. Süzüntü dietil eter ile çöktürüldü ve
çökelek beyaz bantlı Whatman kağıdı ile süzüldü. Dietil eter ile yıkama işlemi
tekrarlandı, beyaz renkli ürün elde edildi
(MTeorik: 897,12 g/mol). Kompleks 252 oC de erimektedir. Kompleks su, alkol, dietil
eter
ve
petrol
eterinde
çözünmezken;
çözünmektedir. (Ruiz, 2006)
36
diklorometan,
dimetilsülfoksitte
3. MATERYAL VE METOD
Belkız AKKUŞ
O
H
N
O
AgClO4
NH
[PtCl2dppatbu] +2
N
CH2Cl2
N
H
PPh2
Ph2
P
Pt
(H3C)3C
O
O
N
N
O
O
NH
Şekil 3.6.[Pt (dppatbu) (urasil)2] kompleksi
Ürün: 0,150 g
Teorik: 0,287 g
Verim: % 55
FT-IR (KBr) : 3414.13 cm-1 ( ş, N-H ); 3062.74 cm-1 ( o, Ar-CH gerilmesi););
2932.29 cm-1 (o, Alifatik C-H ); 1713.98cm-1 ( ş, C=O); 1436.18 cm-1 ( ş, P-Ar );
1099.20-1003.30 cm-1 (C-N (ter amin) gerilmesi ); 1229.94 cm-1 (o, Aromatik C-N
eğilme titreşimi) 760.02, 740.77 703.78 cm-1 ( ş, monosübstitüe benzen C-H );
1
H-NMR (DMSO-d6, 25 oC ppm): 7.77-6.82 (m, 20H (P-Ph)),7.81 (t, 2H (H-
C6urasil)), 5.66 (t, 2H (H-C5 urasil)), 5.73 (s, 2H (N1-H urasil)), 3.89 (s, 4H (NCH2-P)), 1.18 (m, 9H (C(CH3)3))
13
C-NMR (DMSO-d6, 25 oC ppm): 164.787 (C4 urasil), 157.52 (C2 urasil),
142.610(C6 urasil), 134.818-128.970 (P-Ph), 100.695 (C5 urasil), 55.340 (N-C-P),
25.520 (-ter-C), 16.643 (-CH3)3
31
P-NMR (DMSO-d6, 25 oC ppm): d = -13.156 [ P-Pt] J-Pt=2230.8 Hz
37
3. MATERYAL VE METOD
Belkız AKKUŞ
3.2.2.3[ Pt (dppatbu )( teofilin)2] Kompleksinin Sentezi (8)
Tek boyunlu balon içerisine [PtCl2(dppatbu)] metal kompleksi (0,24 g, 0,32 mmol)
ve 20 mL diklormetan eklendi, üzerine (132mg, 0,64 mmol ) AgClO4 eklenir ve oda
sıcaklığında 30 dakika karıştırılır. Bu karıştırma sonucu beyaz renkli AgCl çökmesi
sağlandı ve bu karışım selit’den geçirilerek süzme işlemi tamamlandı Süzüntü tek
boyunlu balon içerisine alındı ve üzerine 10 ml etanol ve aseton(1:1) karışımı
içerisinde çözünen teofilin(115,31mg 0,64 mmol) ilave edildikten sonra karışım oda
sıcaklığında 10 saat boyunca geri soğutucu altında karıştırıldı. Daha sonra
süzüntünün hacmi döner buharlaştırıcı ile 15 mL’ye düşürüldü. Süzüntü dietil eter ile
çöktürüldü ve çökelek beyaz bantlı Whatman kağıdı ile süzüldü. Dietil eter ile
yıkama işlemi tekrarlandı ve vakum altında kurutulduktan sonra beyaz renkli ürün
elde edildi (MTeorik:1032,22 g/mol).
Kompleks 255 oC de erimektedir. Kompleks su, alkol, dietil eter ve petrol eterinde
çözünmezken; diklorometan, dimetilsülfoksitte çözünmektedir.(Romerosa, 19999)
N
O
Teofilin
N
O
N
CH3
N
N
PtdppatbuCl2
+2
N
H
Ph2
P
AgClO4
N
CH2Cl2
N
O
2PhP
CH3
N
CH3
Pt
O
N
3(3HC)C
N
CH3
O
CH3
N
N
CH3
O
Şekil 3.7 [Ptl(dppatbu) (teofilin)2] kompleksi
Ürün: 0,33 g
Teorik: 0,165 g
Verim: % 50
FT-IR (KBr): 3349.88 cm-1 ( ş, N-H gerilmesi); 3059.99 cm-1 (o, Ar-CH ); 2982.82
cm-1 (o, Alifatik C-H ); 1716.33 cm-1 (ş, C=O); 1667.73 cm-1 (o, N-H eğilmesi );
38
3. MATERYAL VE METOD
Belkız AKKUŞ
1567.33 cm-1 (o C=C gerilmesi) 1438.84 cm-1 ( ş, P-Ar ); 1099.77 cm-1 (o, C-N(ter
amin gerilmesi ); 1223.24 cm-1 (o, Aromatik C-N eğilme titreşimi) 763.73, 743.38,
668,09 cm-1 (, monosübstitüe benzen C-H )
1
H-NMR (DMSO-d6 , 25 oC ppm): 7.55-7.36 (m, 20H (P-Ph)), 5.74 (s, 2H (N-H
teofilin)) 3.43 (s, 6H (CH3-N1 teofilin)), 3,22 (s, 6H (CH3-N3 teofilin)), 3.79 (s, 4H
(N-CH2-P))
13
C-NMR (DMSO-d6, 25 oC ppm): 154.832 (C6 teofilin), 151.656 (C2 teofilin),
148.379 (C8), 134.817-128.964 (P-Ph), 106.799 (C5 teofilin), 55.508 (N-C-P),
25.509 (-ter- C)
31
P-NMR (DMSO-d6, 25 oC ppm): d =-13.228 [ P-Pt] J-Pt=2232.8 Hz
3.2.2.4. [Pd(dppam ) (timin)2] Kompleksinin Sentezi (9)
Tek boyunlu balon içerisine [PdCl2(dppam)] metal kompleksi (0,196 g, 0,32 mmol)
ve 20 mL diklormetan eklendi, üzerine (132mg, 0,32 mmol ) AgClO4 eklenir ve oda
sıcaklığında 30 dakika karıştırıldı. Bu karıştırma sonucu beyaz renkli AgCl çökmesi
sağlandı ve bu karışım celitden geçirilerek süzme işlemi tamamlandı Süzüntü tek
boyunlu balon içerisine alındı üzerine 10 ml etanol ve aseton(1:1) karışımı içerisinde
çözünen timin(80,72mg 0,64 mmol) ilave edildikten sonra karışım oda sıcaklığında
10 saat boyunca geri soğutucu altında karıştırıldı. Daha sonra süzüntünün hacmi
döner buharlaştırıcı ile 15 mL’ye düşürüldü. Süzüntü dietil eter ile çöktürüldü ve
çökelek beyaz bantlı Whatman kağıdı ile süzüldü. Dietil eter ile yıkama işlemi
tekrarlandı ve vakum altında kurutulduktan sonra yeşil renkli ürün elde edildi.
(MTeorik: 766,18 g/mol).
Kompleks 316 oC de erimektedir. Kompleks su, alkol, dietil eter ve petrol eterinde
çözünmezken; diklorometan, dimetilsülfoksitte çözünmektedir.(Ruiz, 2006)
39
3. MATERYAL VE METOD
Belkız AKKUŞ
O
H
N
O
AgClO4
NH
[PdCl2dppam] +
N
CH2Cl2
N
H
O
H3C
PPh2
Ph2
P
Pd
N
CH3
O
O
N
O
H3C
NH
Şekil 3.8.[Pd(dppam) (timin)2] kompleksi
Ürün: 0,08 g
Teorik: 0,122 g
Verim: % 65
FT-IR (KBr): 3455.23 cm-1 ( ş, N-H gerilmesi ); 3050 cm-1 ( o, Ar-CH ); 2915cm-1
(ş, Alifatik C-H gerilmesi); 1697 cm-1 ( ş, C=O); 1530.81 cm-1 (o, Aromatik C=C
gerilmesi ); 1436.18 cm-1 ( ş, P-Ar ); 1327 cm1 (o, CH3 ) ; 1122 cm-1 ; 1222.85 cm-1
(o, Aromatik C-N eğilme titreşimi) 749.34, 689.86, 647.23 cm-1 (ş, monosübstitüe
benzen C-H gerilmesi ) ; 700
1
H-NMR (DMSO-d6, 25 oC ppm): 7.37-7.09 (m, 20H (P-Ph)), 7.39 (s, 2H (H-C6)),
5.82 (s, 2H (N1-H)), 3.34 (s, 4H (N-CH2-P)), 1.70, (m,6H N-CH3 ve 6H (CH3 -C6
timin).
13
C-NMR (DMSO-d6, 25 oC ppm) : 165.35 (C4 timin), 151.930 (C2 timin),
138.139(C6 timin), 134.820-128.920 (P-Ph), 108.128 (C5) 12.226(-CH3)
31
P-NMR (DMSO-d6, 25 oC ppm) : d =20.483 [ P-Pt]
40
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
4. BULGULAR VE TARTIŞMA
Metal
fosfin
komplekslerinin
nükleobazlarla
oluşturduğu
karışık
ligandlı
komplekslerinin sentezinde çıkış maddesi olarak dppatbu ve dppam fosfinlerinin
ligand olarak yer aldığı metal fosfinler aşağıda gösterildiği gibi literatürlere göre elde
edilmiştir. (Serindağ 1995)
Ph2
Cl
M
Ph2
P
P
+
R
N
N
Cl
P
Ph2P
Cl
M
Cl
R
Ph2
M COD Cl2
R= -C(CH3)3, -CH3
M= Pt(II), Pd(II)
Şekil 4.1. Metal fosfin kompleksleri
[Pt(dppatbu)Cl2]
ve
[Pd(dppam)Cl2]
kompleksleri
sentezlendikten
sonra
diklorometan içerisinde uygun nükleobazlar (timin, urasil, teofilin) ile etkileştirilerek
karışık ligandlı kompleksler oluşturulmuştur. Nükleobaz komplekslerinin oluşması
için öncelikle metal fosfin komplekslerinde klorların koparılması gerekmektedir. Bu
amaçla tepkime AgClO4 varlığında gerçekleştirilmiştir. Daha sonra eklenen
nükleobazın ortamda bulunan ClO4- iyonları etkisi ile üzerinden bir proton atarak
metale koordine olmaları sağlanmış olur. Elde edilen komplekslerin yapıları FT-IR
ve
1
H,
31
P-NMR,
13
C
gibi
spektoskopik
yöntemlerden
çıkan
sonuçlar
değerlendirilerek aydınlatılmış ve bu verilere dayanılarak yapılar önerilmiştir.
41
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
N
O
Ph2 PPh2
P
Pt
(H3C)3
NH
N3
2 1
6
4 5
O
O
CH3
N
O
H 3C
NH
Şekil 4.2. [ Pt (dppa bu ) (timin)2] Kompleksinin Açık Yapısı (6)
t
H
N
O
N
Ph2
P
(H3C)3C
N3
Pt
O
1
2
PPh2
N
6
5
4
O
O
NH
Şekil 4.3. [ Pt (dppatbu ) (urasil)2] Kompleksinin Açık Yapısı (7)
O
N
7
8
6
5
N
Ph2
P
9
4
CH3
1 NH
2
4
3
N
N
Ph2
P
O
Pt
CH3
3(3HC)C
N
N
4
O
CH3
N
NH
O
CH3
Şekil 4.4. [ Pt (dppatbu ) (teofilin)2 ] Kompleksinin Açık Yapısı (8)
42
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
H
N
O
N
Ph2
P
H 3C
1
2
PPh2
N3
4
Pd
6
5
CH3
O
O
N
O
H 3C
NH
Şekil 4.5. [ Pd (dppam) (timin)2 ] Kompleksinin Açık Yapısı (9)
4.1. Infrared Spektrumlarının Değerlendirilmesi
Literatüre göre sentezlenen fosfin metal komplekslerinin FT-IR spektrumu
incelendiğinde dppatbu ve dppam ligandlarına ait pikler görülmüştür. Bu piklerden
birisi aminometilfosfinler için karakteristik tersiyer amin (-(CH2)2NR) pikleridir.
Sentezlenen komplekslerin FT-IR spekturumlarında ( Ek 2.1-2.4 ) [PtdppatbuCl2 ]
metal kompleksinde tersiyer bütildeki C-N bağ gerilmesi için 1395 -1302 cm-1
aralığında pik ((CH3)3C-N), [PddppamCl2] kompleksinde metil için bu değer 1409 1384 cm-1 dedir. (CH3-N) ve 1162, 1120 ve 1040 cm-1 civarında ise piklerin (C-N-C
gerilmesi ) görülmesi metal kompleksin sentezlendiğini göstermektedir.
Spektrumlarda dikkat edilmesi gereken diğer önemli kısım ise; fosfora ait
piklerdir. Sentezlenen komplekslerin FT-IR spektrumlarında 1436 cm-1 de görülen
keskin pik P-aril’in varlığını ispatlamaktadır. Fonksiyonel grup bölgesindeki; 1952,
1894, 1816 cm-1 zayıf pikler monosubstitüe benzen C-H düzlem dışı eğilmesinin
katlı ve bileşik tonları ve 763,73, 743,38, 668,09 cm-1 keskin pik monosubstitüe
benzendeki düzlem dışı gerilmeleridir. FT-IR spektrumundaki (Ek 2.1-2.4 ) diğer
önemli bölgeler; 3010-3100 cm-1 aromatik C-H gerilmesi orta şiddette, 2965-2915
cm-1 alifatik C-H gerilmesi görülür.
Nükleobazlarla (timin, urasil ve teofilin) oluşturulan karışık ligandlı metal fosfin
komplekslerinde ise bakılması gereken metale koordine olup olmamasıdır. Primer
43
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
aminler 3500-3300 cm-1 frekansında keskin dublet pik, sekonder aminler aynı
frekansta keskin singlet bir pik verirler ancak tersiyer aminler fonksiyonel grup
bölgesinin bu frekansında keskin pikler vermez. Nükleobazların varlığından
kaynaklanan NR2H, ve C=O pikleri sıra ile 3400-3100 cm-1 (Mohammad S. Ali
2006)
ve
1700cm-1
civarında
görülmektedir.
(Erdik
1998).
Sentezlenen
komplekslerde nükleobazların sekonder amin (R2NH) piki 3500 -3300 cm-1
aralığında görülmüştür. Sekonder aminlerin(-NH gerilmesi) soğurması zayıf şiddette
keskin bir pik olarak görülür ve 1580-1490 arasında (-NH ) zayıf bir soğurma bandı
olarak ortaya çıkar. FT-IR spektrumunun orta bölgesinde, 1700 cm-1 civarında, güçlü
bir soğurma, C=O grubuna karşılık gelir ki keskindir; aynı bölge de gözlenebilecek
C=C piki ise orta şiddette veya zayıftır. Aralarındaki fark; C=O bandının daha güçlü
soğurmasıdır (Erdik, 1993). Sentezlenen komplekslerde C=O 1730 cm-1 ve C=C
pikleri 1600 cm-1 civarında görülmüştür.
Sentezlenen [Pt(dppatbu)(tym)2], [Pt(dppatbu)(urasil)2], [Pt(dppatbu)(teofilin)2],
[Pd(dppam)(timin)2] komplekslerinin (Ar-N)1280-1210 cm-1 arasında aromatik
yapıya bağlı azottan dolayı oluşan C-N bağı eğilme titreşim piki görülür, bu da
yapılardaki nükleobazın varlığını göstermektedir. Parmak izi bölgesinde bulunan PtN ise 580 cm-1civarında pik verir. (Mohammad S. Ali 2006).
Sentezlenen komplekslerin FT-IR spektrum değerleri ayrıntılı olarak (Çizelge 4.1)
de verilmiştir.
44
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
Çizelge 4.1 Sentezlenen Komplekslerin FT-IR Spektrum Değerleri
FT-IR Spektrumları
BİL.
ADI
R2NH
ArCH
AlifCH
ArCH
6
3175
3061
2930
19601815
7
3414
3062
2932
8
3349
3059
9
3455
3050
C=O
P-Ar)
CH3-
C-N-C
C=C
C(CH3)3
1737
1681
1301
1436
-
1099
19891816
1713
1689
1304
1436
-
1099
2982
19901819
1716
1667
1368
1438
-
1099
2950
19951800
1697
1680
-
1436
1409
1110
4.2 1H NMR Spektrumlarının İncelenmesi
Sentezlenen komplekslerde FT-NMR spektrumları DMSO-d6 + CDCl3 çözücüsü
kullanarak 25oC de alınmıştır. Verilen proton sayıları hesaplanan integrasyon
değerleriyle uyumludur. 1H-NMR spektrumunda (Ek 1.1-1.4), bütün bileşikler için
d= 7,5-7 ppm civarında monosübstitüe benzen çoklu pikleri gözlenmektedir.6 ve 9.
komplekslerde d= 7,3 ppm deki singlet pik timin nükleobazındaki Ar-C-H pikidir.
d= 5,8 ppm deki singlet pik ise N-H protonlarına aittir.7.bileşikte ise d=7,8 (HC6urasil), d= 5,6 ppm de (H-C5 urasil)) ve 5,7 (N1-H urasil)), piki gözlenmektedir.
8. komplekste ise, d= 5,7 ppm de (N-H teofilin)) 3,4 ve 3,2 ppm de azota bağlı –CH3)
bulunmaktadır. Bu sonuçlara göre 6, 7 ve 9. bileşiklerde (N3) ve 8.bileşikte (N9)
üzerinden bir protonunu ortamda bulunan ClO4 - iyonlarına aktararak metale koordine
olduğu saptanmıştır.(Ruiz Jose, 2006). Sentezlenen bileşiklerde d= 3,7 ppm de NCH2-P singlet piki görünmektedir. 6, 7 ve 8. bileşiklerde d= 1,8 ppm civarında
C(CH3)3 eşdeğer protonlarına ait pikler gözlenmiştir. 9. bileşikte ise 2,5 ppm de
dppam ligandında bulunan N-CH3 singlet piki görünmektedir (Çizelge 4.2 )
45
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
Çizelge 4.2 Sentezlenen Metal Komplekslerinin 1H-NMR Spektrum Değerleri
1
H-NMR (δ,ppm) DMSO + CDCl3 25 oC,
Metal Kompleksleri
(6)
[Pt(dppatbu)(timin)2]
(7)
[Pt(dppatbu)(urasil)2]
(8)
[Pt(dppatbu)(teofilin)2]
(9)
[Pd(dppam)(timin)2]
7.54-7.06 (m, 20H (P-Ph)), 7.35 (s, 2H (H-C6 timin), 5.80 (s,2H
(N1-H timin)), 3.75 (s, 4H (N-CH2-P)), 1.84-2.08 (m,9H NC(CH3)3 ve 6H (-CH3-C6 timin).
7.77-6.82 (m, 20H (P-Ph)),7.81 (t, 2H (H-C6urasil)), 5.66 (t, 2H
(H-C5 urasil)), 5.73 (s, 2H (N1-H urasil)), 3.89 (s, 4H (N-CH2-P)),
1.18 (m, 9H (C(CH3)3))
7.55-7.36 (m, 20H (P-Ph), 5.74 (s, 2H (N-H teofilin)) 3.43 (s, 6H
(CH3-N1 teofilin)), 3,22 (s, 6H (CH3-N3 teofilin)), 3.79 (s, 4H (NCH2-P))
7.37-7.09 (m, 20H (P-Ph)), 7.39 (s, 2H (H-C6)), 5.82 (s, 2H (N1H)), 3.34 (s, 4H (N-CH2-P)), 1.70 , (m,6H N-CH3ve 6H (CH3 -C6
timin).
4.4 13C NMR Spektrumlarının Değerlendirilmesi
13
C-NMR spektrumunu incelendiğinde(şekil 4.2-4.5) bütün bileşiklerde (Ek 1.5-1.8)
d=134 -128 ppm monosübstitüe benzenin çoklu pikleri gözlenmektedir. 6. ve 9.
bileşiklerde d= 165,3 ppm’de görülen singlet pik (C4) timin bazına aittir. 7.bileşikte
(Ek 1.6) 164,7 ppm de (C4, urasil), 100,7 (C5 urasil) bazına aittir. 8. bileşik
incelendiğinde(Ek 1.7) 154,8 ppm de (C2 teofilin), 106,7 (C5 teofilin) bazına aittir.
Nükleobazın metal kompleksine koordine olması
13
C piklerini daha düşük alana
kaydırmasıdır. Bunun sebebi ise nükleobazın metale koordine olduktan sonra
elektronegatif grupların elektron yoğunluğunun azalmasıdır bu da litaratürdeki
değerlerle uygunluk göstermektedir.(Longato Bruno, 2006, Ruiz Jose,2006,
Romerosa Antonio, 2000, Akmal S.Gaballa, 2008)
. 6, 7, 8. bileşiklerde 25,5 ppm de (-ter-C-N) elektronegatif atoma bağlanmasıyla
düşük alana doğru kaymaktadır ve 16,6 ppm de (-CH3)3 pikleri gözlenmektedir. 9.
46
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
bileşikte ise dppam ligandında 12,2 ppm de (N-CH3) ait pik görülmektedir. (Çizelge
4.3)
Çizelge 4.3. Sentezlenen Metal Komplekslerinin 13C-NMR Spektrum Değerleri
Metal
13
C-NMR (δ,ppm) DMSO + CDCl3 25 oC,
Kompleksleri
(6)
165.365 (C4 timin), 151.945 (C2 timin), 138.152 (C6 timin), 134.820128.920 (P-Ph), 108.137 (C5), 25.01(-ter C), 12.22(C6-CH3)
164.787 (C4 urasil), 157.52 (C2 urasil), 142.610(C6 urasil), 134.818-
(7)
128.970 (P-Ph), 100.695 (C5 urasil), 55.340 (N-C-P), 25.520 (-ter-C),
16.643 (-CH3)3
(8)
(9)
154.832 (C6 teofilin), 151.656 (C2 teofilin), 148.379 (C8), 134.817128.964 (P-Ph), 106.799 (C5 teofilin), 55.508 (N-C-P), 25.509 (-ter- C)
165.35 (C4 timin), 151.930 (C2 timin), 138.139(C6 timin), 134.820128.920 (P-Ph), 108.128 (C5) 12.226(-CH3)
4.5. 31P NMR Spektrumlarının Değerlendirilmesi
31
P-NMR verileri (Ek 1.9-1.12 ) aminometilfosfinin metale fosfor üzerinden
koordine olduğunu gösteren önemli bir kanıttır. Spektrum incelendiğinde, metale
dppatbu ligandının yanısıra ikinci bir ligand olarak timinin azot üzerinden
bağlandığını göstermektedir. Literatürlere göre [PtdppatbuCl2] metal kompleksinin
monosübstitüe benzene bağlı olan elektronegatif fosfor atomu, elektropozitif olan
Pt(II) metal iyonuna koordine olup ortaklanmamış elektron çiftini metal iyonuna
sunar, d-orbitallerindeki boşluğa metalden geri bağlanma etkisi ile metalin
etrafındaki elektron yoğunluğu azalır ve kimyasal kayma değeri d= -8,5 ppm de
görülür. Nükleobazın metal iyonuna koordine olması ile bu değer daha negatif
değere doğru kayar bunun nedeni Pt ile heterosiklik sekonder aminin bir protonunu
atıp Pt(II) metaline elektron çifti sunarak sigma bağı yapması ve elektronegatifliği
yüksek olan N ile Pt(II) arasında p geri bağlanmasının gerçekleşmesi şeklinde
47
4. BULGULAR VE TARTIŞMA
Belkız AKKUŞ
yorumlanabilir. (Lakomska Iwona, 2008) Komplekste
P
Pt
N
hem P hem
de N p geri bağlama etkisi birbirini zayıflatır ve kompleks daha negatif alana doğru
bir kayma gösterir.( d= -13,1 ppm ) J (P-Pt)= 2230.8 Hz (Julia, 2006)
Sentezlenen Pt-metal komplekslerinde metalin NMR aktif olması sebebiyle fosfor PPt yarılması gerçekleşir. J(P-Pt) değerleri incelendiğinde tek bir yarılma
gözlenmiştir. Bu da metale koordine olan nükleobazın (1:2) şeklinde bağlandığının
kanıtıdır. Ayrıca arjentometrik titremetri yöntemi ile yapıda klorun olmadığı
gözlenmiştir. Eğer kompleks (1:1) şeklinde olsaydı fosfor; Cl ve nükleobazın N ile
trans durumda olup iki farklı fosfor çevresine sahip olacaktı ve iki tane J(P-Pt) değeri
olacaktı (Serindag 1995; Montagner Diego, 2008) (Çizelge 4.3).
31
P-NMR spekturumu (Ek 1.12 ) incelendiğinde, metale dppam ligandının yanısıra
ikinci bir ligand olarak N3 atomu üzerinden timin bazı bağlanmıştır Oluşan
komplekste fosfor tek bir pik olarak gözlenmiştir. Bunun nedeni Pd’un NMR aktif
olmamasıdır. Sonuç olarak da kompleksin yarılmadan kaynaklanan J(eşleşme sabiti)
değeri yoktur. Oluşan kompleks de kimyasal kayma değeri d=20,4 ppm de
gözlenmiştir bu da literatürdeki değerlerle uygunluk göstermektedir. (Romanelli,
2005, Gaballa, 2008)
Çizelge 4.4 Sentezlenen Metal Komplekslerinin 31P-NMR Spektrum Değerleri
31
Bileşikler
(6)
P{1H}-NMR (δ,ppm)
(DMSO- d6, 25 oC)
dA=-13.188
∆δ = δkompleks - δligand
J (P-Pt)
Δd =13.812
2229.6
(7)
dA=-13.156
Δd =13.843
2230.8
(8)
dA=-13.228
Δd =13.771
2232.8
ΔdA =47.483
-
(9)
dA= 20.483
48
5. SONUÇ VE ÖNERİLER
Belkız AKKUŞ
5. SONUÇ VE ÖNERİLER
N,N bis(difenilfosfinometil)aminoter-butil (dppatbu): [(Ph2PCH2)2NC(CH3)3] ve
N,N bis(difenilfosfinometil)aminometil (dppam): [(Ph2PCH2)2NCH3] ligandları ve bu
ligandların Pt (II) ve Pd (II) metal kompleksleri literatüre göre sentezlenmiştir. Daha
sonraki aşamada ise oluşan metal komplekslerinin nükleobaz (timin, urasil ve
teofilin) içeren karışık ligandlı geçiş metali kompleksleri sentezlenmiştir.
Sentezlenen kompleksler; FT-IR,
1
H,
31
P-NMR teknikleri kullanılarak
karakterize edilmiştir. Nükleobazların Pt (II) ve Pd(II) metal komplekslerine
koordine olduğu
31
P-NMR spektrumları değerlendirilerek saptanmıştır.
31
P-NMR
spektrumlarında, nükleobazların ikinci bir ligand olarak metale koordine olmasıyla
komplekslerin sıra ile (6) +13.812; (7) +13.843; (8) +13.771 (9) +47.483 ppm civarında
pikler gözlenmiştir. Oluşan karışık ligandlı metal komplekslerinde ilk olarak
[Pt(dppatbu)Cl2] ve [Pd(dppam)Cl2] metal komplekslerinden iki klorun kopması ve
yerine nükleobazların; timin ve urasilin N3, teofilinin ise N9 üzerinden
deprotonlanması ile metale bağlanmıştır ve aynı kimyasal çevre fosforlara sahip
olduğu belirlenmiştir. Fakat platin komplekslerinin NMR aktif bir çekirdeğe sahip
olması nedeni ile P-Pt arasında da bir yarılma görülmüştür. FT-IR sonuçlarına göre
spektrumlarda
görülen
karbonil
piklerinin
varlığı
aminometilfosfin
metal
kompleksine nükleobazın bağlandığının bir kanıtıdır. Ayrıca, komplekslerin sentezi
sırasında ani renk değişimleri saptanmıştır ve Pd kompleksinde yeşil renkli kompleks
oluşmuştur, Pt(II) komplekslerinde ise renk değişimi gözlenmemiştir.
Fosfin içeren karışık ligandlı metal komplekslerinin in vivo olarak, yani canlı
ortamında
antimikrobiyal
bilinmektedir
ve
veya
grubumuz
antitümoral
tarafından
aktitivitelerinin
çalışılmaktadır.
etkin
Sentezlenmiş
olduğu
olan
komplekslerin de etkin olabileceği düşünülmektedir ve de aynı amaç doğrultusunda
çalışılacaktır.
49
KAYNAKLAR
A.GARCIA-RASO, J.J. FIOL, A. TASADA, M.J. PRIETO, V. MORENO, I.
MATA, E. MOLINS, T. BUNIC, A. GOLOBIC, I. TUREL (2005),
“Ruthenium complexes with purine derivatives: Syntheses, structural
characterization and preliminary studies with plasmidic DNA” Inorganic
Chemistry Communications 8, 800–804.
AKMAL S. GABALLA, HARRY SCHMIDT, CHRISTOPH WAGNER, DIRK
STEINBORN (2008), “Structure and characterization of platinum(II) and
platinum(IV) complexes with protonated nucleobase ligands”, Inorganica
Chimica Acta 361, 2070–2080
ANN L. PINTO, LISA J. NASER, JOHN M. ESSIGMANN, AND STEPHEN J.
LIPPARD (1986), “Site-Specifically Platinated DNA, a New Probe of the
Biological Activity of Platinum Anticancer Drugs” J. Am. Chem. Soc., 108,
7405-7407
ANTONIO
ROMEROSE,
phosphine
complexes
CARLOS
from
LOPEZ-MAGANA(2000),
8-(thio)-theophyllline
and
“Palladdium
8-(benzylthio)-
theophyllline’’ Inorganica Chimica Acta 307, 125-130
BERNER-PRICE, S.J., SADLER, P.J., Structure Bonding (Berlin), 70, (1988), 27
BERNHARD LIPPERT (1981), “Platinum Complexes of Uracil. Multiplicity and
Interconversion of Binding Sites’’ Inorg. Chem., 20,4326-4343
BRUNO LONGATO, LUCIA PASQUATO, ADELE MUCCI, LUISA SCHENETTI
and ENNIO ZANGRANDO (2003), “Complexes of Platinum(II) Containing
Neutral and Deprotonated 9-Methyladenine. Synthesis, X-ray Structures, and
NMR Studies on the Cyclic Trimer cis-[L2Pt9-Methadenine)]3(NO3)3 and the
Dinuclear
cis-[L2Pt(ONO2)
9-Methadenine(H)PtL2](NO3)2
(L)
PMePh2
Inorganic Chemistry, Vol. 42, No. 24
COATES, H., HOYE, P.A.T., 1960, Br.Patent, 854182.
DIEGO MONTAGNER A, BRUNO LONGATO (2007), “Synthesis and
characterization of cis-[(PPh3)2Pt{9-MeAd(-H),N6N7}]X X_=NO3, PF6): The
50
first example of a platinum(II) complex containing the N6,N7-chelated 9methyladenine anion” Inorg. Chim. Acta,doi:10.1016/j.ica
DONG, Y. Et. Al., ‘‘Serine protease inhibition and mitochondrial dysfunction
associated with cisplatin resistance in human tumor cell lines
targetsfor therapy’’, Biochem. Pharmacol., 53, (1997), 1673-1682
ELISA GIL BARDAJ, EVA FREISINGER, BURKHARD COSTISELLA,
CHRISTOPH A. SCHALLEY, WOLFGANG BRUNINIGr, MICHAL
SABAT, AND BERNHARD LIPPERT (2007), “Mixed-Metal (Platinum,
Palladium),
Mixed-Pyrimidine
(Uracil,
Cytosine)
Self-Assembling
Metallacalix[n]arenes: Dynamic Combinatorial Chemistry with Nucleobases
and Metal Species” Chem. Eur. J, 13, 6019 – 6039
ERDİK. E (1998), Organik Kimyada Spektroskopik Yöntemler, Gazi Kitabevi, 2.
Baskı, Ankara Üniversitesi Fen Fakültesi, 82-385.
FELIX ZAMORA, M PILAR, AMO-OCHOA, PABLO J SANZ, MIGUEL OSCAR
CASTILLO (2008), “From metal-nucleobase chemistry towards molecular
wires” Inorganica Chimica Acta revie
IWONA LAKOMSKA (2008), “Molecular structure and antitumor activity of
platinum(II) complexes containing purine analogs”, Inorganica Chimica Acta
İKİZLER AYKUT (1985), Hetereohalkalı Bileşikler
KELES M, ALTAN O, SERİNDAĞ O. (2008), ‘‘Synthesis and charecterization of
Bis(diphenylphosphinomethyl) amino Ligands and Their Ni(II), Pd(II)
Complexes: Aplication to Hydrogeneration of Styrenes’’, 19, 1
LAPOINTE, A. M., Paralel Synthesis of Aminomethylphosphine Ligands,
J. Comb. Chem. 1, (1999), 101-104
LAKOMSKA IWONA (2008), “Molecular structure and antitumor activity of
platinum(II) complexes containing purine analogs”, Inorganica Chimica Acta
LOUIS Y. KUO, MERCOURI GTOBIN J. MARKS (1991), ‘‘Metallocene
Antitumor Agents. Solution and Solid-state Molybdenocene Coordination
Chemistry of DNA Constituents’’ J. Am. Chem. SOC. 1991, 113, 9027-9045
MCKEAGE, M.J, MAHARAJ, L. BERNERS-PRICE, S.J (2002), ‘‘Mechanisms of
Cytotoxicity and antitumor activty of gold (I) phosphine complexes: the
51
Possible role of mitochondria’’.Coordination Chmistry Reviews 232)
127-135
MIRABELLI, C.K., JOHNSON, R.K., SUNG, C., FAUCETTE, L.F., MUIRHEAD,
K., CROOKE, S.T., Cancer Res., 45, (1985), 32.
MOHAMMAD S. ALI, EDIO LONGORIA JR, TEYEB OULD ELY,
KENTON H. WHITMIRE, ABDUL R. KHOKHAR (2006), “Homopiperazine
Pt(II) adducts with DNA bases and nucleosides: Crystal structure of
[PtII(homopiperazine)(9-ethylguanine)2](NO3)2” Polyhedron, 25, 2065–2071
NICOLE PASCHKE A, AXEL RONDIGS A, HEIKE POPPENBORG B,
JOHANNES E.A. WOLFF B, BERNT KREBS (1997), “Reaction of the diaqua
( 2- (pyridin-2-yl)-2-oxazoline) platinum (II) and palladium(II) dications with
the model nucleobases 1-methylthymine and 1-methyluracil-” 264 239-248
NOVELLI F., RECINE M., SPARATORE F., JULIANO C., 1999. Gold(I)
complexes as antimicrobial agents, Il Farmaco, 54, 232-236.
ROMENELLI ALLESANDRA (2005), “Reaction of Pd(PPh3)4 with 3,5-Di-Oacetylthymidine:Oxidative Addition Pd(PPh3)4 on Thymidine N3 and C4 atoms
RUIZ JOSE (2006), “Palladium(II) and Platinum(II) Organometallic Complexes with
the Model Nucleobase Anions of Thymine, Uracil, and Cytosine: Antitumor
Activity and Interactions with DNA of the Platinum Compounds
SADLER P.J (2003), “Medicinal Inorganic Chemistry”, Medicinal Chemistry and
Biotechnology.
SHI CHENG JI, KANG SHENG- BEI and C. W. MAK THOMAS (1997), “Selfassembly of a chiral phosphinegold(I) building block into a two-dimensional
netsheet based on a hydrogen bond between one Cl- anion and three hydroxy
groups, co-ordination and aurophilicity interactions” J. Chem. Soc, Dalton
Trans, 2171 - 2176, DOI: 10.1039/a701434a
SERINDAĞ. O (1993), “The synthesis of aminobis(methylphosphynes) and their
transitionmetal complexes”, PhD Thesis, Department of ChemisFtry,
University of Leicester.
52
URUŞ, S., SERİNDAĞ, O. DİĞRAK, M. (2005), “Synthesis characterization and
antimicrobial activies of Cu(I), Ag(I), and Co(II) complexes with ligand
dppam”, Heteroatom Chemistry, 16, 6.
TAKAHARA P.M., FREDERICK C.A., LIPPARD S.J., “Crystal structure of the
anticancer drug cisplatin bound to duplex DNA”, J. Am. Chem. Soc., 118,
(1999), 12309-12321.
YANG P., GUO M., “İnteractions of organometallic anticancer agents with
nucleotides and DNA”, Coord. Chem. Rev.,185-186, (1999), 189-221
YONGWON JUNG AND STEPHEN J. LIPPARD (2007), “Direct Cellular
Responses to Platinum-Induced DNA Damage”, Chemical Reviews,. 107,. 5
53
ÖZGEÇMİŞ
1983 yılında Seyhan / ADANA’ da doğdu. İlköğrenimini Emine Nabi
Menenemencioğlu, Recep Birsin Özen ilköğretim okulu’nda, orta öğrenimini, lise
öğrenimini ise Hacı Ahmet Atıl Lisesi (Yabancı Dil Ağırlıklı)’nde tamamladı. 2002
yılında Çukurova Üniversitesi Kimya Bölümü’nde lisans eğitimine başladı ve 2006
yılında mezun oldu. Aynı yıl Çukurova Üniversitesi Fen Bilimleri Enstitüsü Kimya
Anabilim Dalında Yüksek Lisans eğitimine başladı. Yabancı Dili İngilizcedir.
54
Ek 1.1. [Pt(dppatbu) (timin)2] Kompleksinin 1H-NMR Spektrumu
55
Ek 1.2. [Pt(dppatbu) (urasil)2] Kompleksinin 1H-NMR Spektrumu
56
Ek 1.3. [Pt(dppatbu) (teofilin)2] Kompleksinin 1H-NMR Spektrumu
57
Ek 1.4. [Pd(dppam) (timin)2] Kompleksinin 1H-NMR Spektrumu
58
Ek 1.5. [Pt(dppatbu) (timin)2] Kompleksinin 13C-NMR Spektrumu
59
Ek 1.6. [Pt(dppatbu) (urasil)2] Kompleksinin 13C-NMR Spektrumu
60
Ek 1.7. [Pt(dppatbu) (teofilin)2] Kompleksinin 13C-NMR Spektrumu
61
Ek 1.8. [Pd(dppam) (timin)2] Kompleksinin 13C-NMR Spektrumu
62
Ek 1.9. [Pt(dppatbu) (timin)2] Kompleksinin 31P-NMR Spektrumu
63
Ek 1.10. [Pt(dppatbu) (urasil)2] Kompleksinin 31P-NMR Spektrumu
64
Ek 1.11. [Pt(dppatbu) (teofilin)2] Kompleksinin 31P-NMR Spektrumu
65
Ek 1.12. [Pd(dppam) (timin)2] Kompleksinin 31P-NMR Spektrumu
66
Ek 1.1. [Pt(dppatbu) (timin)2] Kompleksinin 1H-NMR Spektrumu
55
Ek 1.2. [Pt(dppatbu) (urasil)2] Kompleksinin 1H-NMR Spektrumu
56
Ek 1.3. [Pt(dppatbu) (teofilin)2] Kompleksinin 1H-NMR Spektrumu
57
Ek 1.4. [Pd(dppam) (timin)2] Kompleksinin 1H-NMR Spektrumu
58
Ek 1.5. [Pt(dppatbu) (timin)2] Kompleksinin 13C-NMR Spektrumu
59
Ek 1.6. [Pt(dppatbu) (urasil)2] Kompleksinin 13C-NMR Spektrumu
60
Ek 1.7. [Pt(dppatbu) (teofilin)2] Kompleksinin 13C-NMR Spektrumu
61
Ek 1.8. [Pd(dppam) (timin)2] Kompleksinin 13C-NMR Spektrumu
62
Ek 1.9. [Pt(dppatbu) (timin)2] Kompleksinin 31P-NMR Spektrumu
63
Ek 1.10. [Pt(dppatbu) (urasil)2] Kompleksinin 31P-NMR Spektrumu
64
Ek 1.11. [Pt(dppatbu) (teofilin)2] Kompleksinin 31P-NMR Spektrumu
65
Ek 1.12. [Pd(dppam) (timin)2] Kompleksinin 31P-NMR Spektrumu
66