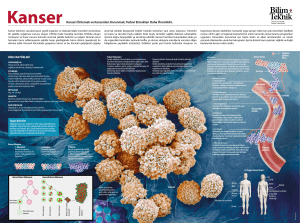
östrojen reseptörü negatif invaziv meme karsinomlarının morfolojik
advertisement

T.C. Sa lık Bakanlı ı stanbul E itim ve Ara tırma Hastanesi Patoloji Laboratuvarı. ef: Doç. Dr. Erol Rü tü Bozkurt ÖSTROJEN RESEPTÖRÜ NEGAT F NVAZ V MEME KARS NOMLARININ MORFOLOJ K - MMUNFENOT P K ANAL Z VE YEN FONKS YONEL MEME KARS NOMU SINIFLAMASINDAK YER Dr. Fadime BAHADIR UZMANLIK TEZ stanbul-2008 ÖNSÖZ E itime ve bilime önem veren, bizlere rahat bir çalı ma ortamı sa layan ba hekimimiz; Operatör Dr. Özgür Yi it’e, Patoloji bilgisi ve bilimselli i ile tanıma ansına sahip oldu um,,etik yönüyle herkese kar ı samimi, özverili, her zaman sevgi ve saygı ile anaca ım de erli hocam, klinik efim; sayın Doç. Dr. Erol Rü tü Bozkurt’a, Asistanlı ım süresince destek olan klinik ef yardımcımız Dr. Bilgin Aksoy’a, Bilgisi, karakteri ve yardımseverli i ile bana çok ey ö retti ine inandı ım, tez danı manım; Dr. Zuhal Gücin’e, Asistanlı ım süresince bilgi ve tecrübelerini esirgemeyen, her zaman destek olduklarını hissettiren, uzmanlarım Dr.Osman Nuri Hüten, Dr.Feray Günver, Dr. Gülben Erdem Huq, Dr. Kemal Behzato lu, Dr.Cem Leblebici, Dr.Esra Pa ao lu, Dr.Nevra Dursun’a, Asistanlık sürecini payla tı ım, dostluk ve arkada lıklarını unutamayaca ım; Dr. Melin Özgün Geçer, Dr. Nilsen Erdo an, Dr.Tu çe Güzel Çay, Dr. Meltem Öznur, Dr. Melike Özcan, Dr. Gülzade Karaman, Dr. ule Canberk, Dr. Pelin Yıldız’a, Hiçbir zorunlulukları olmamasına ra men çalı malarımda özverileriyle teknik olarak titizlik ve destek sa layan Burcu Atay, Aslı Tüysüz, Hacı Ali Kurt, Osman Saman, . Koray Cengiz, Tu ba Ay ar'a, Her zaman yanımda olan sevgili e ime, canım kızlarım Esra ve Elif’e Ömür boyu benden deste ini esirgemeyen, beni yeti tiren anneme ve babama Sonsuz te ekkür ederim. i Ç NDEK LER 1.G R VE AMAÇ .................................................................................. 2.GENEL B LG LER ............................................................................... 1 3 2.1.TAR HÇE ................................................................................................................. 2.2.EMBR OLOJ ........................................................................................................... 2.3.ANATOM ................................................................................................................ Memenin arterleri..................................................................................................... Memenin sinirleri ..................................................................................................... Memenin lenfatik direnajı ........................................................................................ 2.4.F ZYOLOJ VE H STOLOJ ................................................................................... 2.5.YEN PROGEN TÖR HÜCRE MODEL .......................................................... 2.6.MEME KANSER .................................................................................................... nsidans ve Epidemiyoloji ........................................................................................ WHO Sınıflaması...................................................................................................... Etyoloji...................................................................................................................... nvaziv meme karsinomu.......................................................................................... nvaziv duktal karsinom...................................................................................... nvaziv lobüler karsinom .................................................................................... Tubuler karsinom ................................................................................................ nvaziv kribriform karsinom ............................................................................... Medüller karsinom .............................................................................................. Müsin üreten karsinom ....................................................................................... Nöroendokrin tümörler ....................................................................................... nvaziv papiller karsinom ................................................................................... nvaziv mikropapiller karsinom......................................................................... Apokrin karsinom ............................................................................................... Metaplastik karsinom.......................................................................................... Prognostik parametreler.................................................................................................. 2.7.MEME KANSER SINIFLAMASINA YEN YAKLA IM VE BAZAL BENZER MEME KARS NOMLARI...................................................... 3 4 4 5 5 5 6 7 10 10 10 13 14 14 16 17 18 18 18 18 18 19 19 19 20 28 3.MATERYAL-METOD .......................................................................... 34 Kullanılan antikorlar ................................................................................................ 35 HK Boyama yöntemi ve de erlendirme ................................................................ 36 statiksel De erlendirme .......................................................................................... 37 4.BULGULAR ........................................................................................... 5.TARTI MA ............................................................................................ 6.RES MLER............................................................................................. 7.SONUÇLAR ........................................................................................... 8.KAYNAKLAR........................................................................................ ii 38 58 65 73 75 KISALTMALAR BLBC :Basal like breast carcinoma (bazal benzeri meme kanseri). BRCA1: Breast Carcinoma- 1. CK : Cytokeratin. EGFR : Epidermal Growth Factor Receptor(epidermal büyüme faktör reseptör) ER : Öströjen Reseptör. GEP : Gen Ekspresyon Paterni. H&E : Hematoksilen Eozin. EAH : stanbul E itim ve Ara tırma Hastanesi. HK : mmunhistokimya. NOS : Non othervise spesificiated. PBS : Phosphate Buffered Saline. PR : Progesteron Reseptör. SMA : Smooth Muscle Actin (Düz kas aktini). TDLU : Terminal Duktal Lobuler Unit. WHO : World Health Organization(Dünya sa lık örgütü). iii ÖZET Meme kanserleri oldukça sık görülen ancak; biolojik davranı olarak geni bir yelpazede da ılan; heterojenöz bir hastalık grubudur. Klinik olarak bu kadar geni da ılıma ra men ço u meme kanseri (%75-80) aynı histolojik tanıyı (NOS- invaziv duktal karsinom) almaktadır. Büyük bir bölümü luminal fenotipte olup; memenin duktus ve asinüslerindeki luminal yüzde yer alan hücrelerin salgıladı ı proteinleri ekspresse ederler. Bunlar; ER, PR, CK8, CK18 ve CK19’ dur. %2-18’i ise memenin duktus ve asinüslerindeki dı kısımda yer alan kontraktil miyoepitel veya bazal tabaka hücrelerinin salgıladı ı proteinleri ekspresse ederler. Bu proteinler yüksek molekül a ırlıklı sitokeratinler (CK5/14) ve düz kas aktini markerleridir. ( SMA, Calponin, p63 ). Henüz bu grup tümörler rutin pratikte tanınamamakta ve terminolojileri konusunda da net bir konsensus yoktur. Bu tümörlere bazaloid, bazal benzeri veya myoepitel diferansiasyon gösteren duktal karsinom gibi de i ik isimler verilmektedir. Son yıllarda belirgin olarak birbirlerinden farklı meme kanseri tipleri tanımlanmaktadır. Bunlar: Luminal A , Luminal B, HER-2(+), Bazal benzeri ve Normal meme benzeri. Bu ayırım temel olarak tümörün köken aldı ı hücre tipine özgü genler ile belirlenmektedir. Östrojen reseptörü ta ıyan karsinomlar luminal tipe uymakta ve iyi prognoz gösterip antiöstrojen tedaviden yüksek oranda yarar görmektedir. En kötü prognozlu grup ise HER-2(+) ve bazal benzeri meme karsinomlarıdır.. Bazal benzeri meme karsinomları rutin patikte gözden kaçan ya da farkında olunmayan oysa gelecekte yeni tedavi modelleri için aday tümör gruplarıdır. Bu çalı manın amacı ER (-) meme kanserlerinin morfolojik ve immunhistokimyasal profillerini analiz ederek incelemek; HER-2 pozitif, üçlü negatif/ bazal benzeri altgrupları ve bunların görülme sıklıklarını ara tırmak; benzer ve farklı özelliklerini tanımlamaktır.. Çalı mamızda; 47 ER(-), 16 ER (+) olgunun patoloji ar ivinden blok ve lamları çıkarılarak yeniden incelendi. H&E ile boyalı tümöral doku kesitlerinde çe itli morfolojik parametreler olan; tümör marjini, lenfoid stromal infiltrasyon, , berrak hücreli ,basaloid, undiferansiye/küçük hücreli patern, skuamöz /i si hücreli de i iklik, tumoral dev hücre varlı ı, belirgin santral fibroz/nekroz varlı ı de erlendirildi. Uygun bloklara HK olarak: ER, PR, HER-2, SMA, Calponin, p63, CK5/6, CK14, CK17, CK18, BRCA1 antikorları çalı ıldı.. Miyoepitelyal diferansiasyonu belirlemek için; Calponin , SMA, P63 ,Luminal diferansiasyon için; CK18, Bazaloid diferansiasyon için; CK5/6, CK14, CK17 kullanıldı. Sonuç olarak ER(-) meme karsinomlarında; yüksek grade, belirgin lenfoid stroma, santral fibroz/nekroz, itici invazyon sınırı gibi morfolojik bulgular daha sık izlenmi olup buna ilaveten skuamoid, berrak hücreli ve i si hücreli de i ikliklerde saptanmı tır.Bazal CK, Düz kas markerleri, BRCA1 ER(+) kanserlere oranla daha yüksek bulundu. Anahtar kelimeler: Bazal fenotip, meme kanseri, östrojen reseptörü, yeni fonksiyonel sınıflama,. iv SUMMARY Breast carcinoma is a very common but extremely heterogeneus disease that exhibits a full range of bilogical behaviour. Despite this range of behaviour most tumors (75%) are categorized within a single histological diagnostic category of invasive ductal cancer of NST. The majority of those have a luminal phenotype; that is they express smilar proteins to those found in the normal inner luminal cells of breast ducts and asini and such as express ER, CK8/18. But 2-18% also coexpress proteins normally found in the outer contractile myoepithelial or basal layer of normal breast duct and asini. These proteins include CK5/14, Smooth muscle markers (SMA, Calponin, p63). These tumors are usually ER(-), PR(-), HER-2(-) (Triple negative ). There are not identified in routine practice and there is no consensus terminology about these tumors. Their own preferred name, such as basaloid, basal-like or ductal carcinoma with myoepithelial phenotype to describe them. In recent years; have identified several distinct breast cancer subtypes.These are: luminalA, luminalB , Basal-like , HER-2 overexpressing and Normal breast like. These results strongly support the notion that different tumor subtypes originate from different cell types. The worst prognosed group is Basal like and HER-2 (+) subtypes. Basal like breast carcinomas can escape observation in routine practice or not realised however these tumour groups are candidates for future treatment models. The purpose of this study was to determine the characteristics of 47 ER(-) breast cancers through analysis of several morphological and immunophenotypical profile and research the HER-2 positive and triple negative/ basal like subsets and their frequency, common and diverse features by routin morphologic and immunohistochemical examination. 47 ER (-), 16ER(+) cases with retrievable histological material (blocks and slides) were included in this study. Patients' clinical history and cancer characteristics including tumor type, histological grade, tumor size, lymph node status were obtained from the pathology database. An H&E stained section from a representative tumor block was examined for the various morphological parameters such as pushing margin, lymphoid stromal infiltrate, clear cell changes, basaloid change, undifferentiated/small cell pattern, squamoid or spindle cell changes, tumor giant cells and prominent central fibrosis/necrosis. The antibodies utilized included ER, PR, CK5/6, CK18, CK14,CK17, SMA, BRCA1, CerbB-2, p63. Calponin, SMA, p63 were utilized to identify myoepithelial differentiation, CK5/6, CK14, CK17 which identify basal; CK18 luminal epithelial differentiation respectively were also included. Finally: High grade,, lymphoid stroma, and central fibrosis/necrosis are the dominant morphological findings. In addition, squamoid, clear cell and spindle cell differentiation may be identified. Alterations in protein expression of basal type cytokeratins, SMA, Calponin and BRCA1, are also more commonly seen than ER(+) invasive breast cancers. Key words: Basal phenotype, breast cancer, estrogen receptor, new functional classification. v 1) G R VE AMAÇ Meme kanseri kadınlarda en sık görülen karsinomdur. Tüm kanserler içinde kadınlarda görülme sıklı ı %22 dir; bu oran geli mi Mortalite riski ülkelerde %26’ya kadar yükselir. %18 olup akci er karsinomundan sonra ikinci sırada yer alır (1). Ülkemizde bu konuda yeterli istatiksel veri bulunmamakla birlikte Türkiye Bilimsel Ara tıma Kurumu’nun 1994 yılı verilerine göre 1985-1990 yılları arasında kadınlarda görülen kanserler arasında %23,2 ile ilk sırada yer almaktadır (2) Meme karsinomları; morfolojik, klinik, hormon reseptör düzeyi, tedaviye yanıtlarına göre farklı özellikleri olan, heterojenöz gruplara sahip tümörlerdir. Bu farklılı ın sebebi: altta yatan hedef hücre (kanser hücresi) popülasyonundaki farklılık, aktivasyonu ve/veya tümör supresor gen fonksiyon farklı onkogen kayıplarındaki de i ik kombinasyonlardır. Fakat yıllardır kullanılan klasifikasyon morfoloji esaslıdır (3). Günümüzde meme karsinomlarına yapılan medikal tedavilerde östrojen / progesteron reseptörü varlı ı ve CerbB-2 overexpresyon düzeyi oldukça önemlidir. ER (+) meme karsinomlarında antiöströjen tedavisi (Tamoxifene ve Raloxifene ) primer medikal tedavi yöntemi olarak uzun yıllardır kullanılmaktadır. Yakla ık meme karsinomlarının % 60-65’i ER ve PR pozitiftir (4,5). Histolojik olarak iyi diferansiye tümörler genelde ER(+) olup bu tümörlerin büyük bir kısmı iyi prognoza sahiptir (6). Buna kar ılık meme karsinomlarının %30’u ER negatiftir. ER( –) meme karsinomları incelendi inde, genelde az diferansiye, tedaviye yanıtları zayıf olan, kötü prognoza sahip tümörler oldu u anla ılmı tır (4,1,6). Pek çok meme karsinomu vakası NOS nvaziv Duktal Karsinom tanısı almasına ra men çok farklı klinikler gösterebilmektedir. Histopatolojik özellikleri benzer gibi 1 gözükse de farklı davranı ların nedeni tümörün genetik özelliklerinde aranmaya ba lanmı ve tümörlerde gen ekspresyon paternleri ile ilgili ara tırmalar hız kazanmı tır. cDNA mikroarray yöntemi ile olu an gen ekspresyon paternlerine göre meme karsinomları 5 tipe ayrılmaktadır. Luminal A , Luminal B, HER2(+), Bazal benzeri ve Normal meme benzeri. Bu ayırım temel olarak tümörün köken aldı ı hücre tipine özgü genler ile belirlenmektedir (3,5,9,10). Yeni fonksiyonel meme karsinomu sınıflamasına göre östrojen reseptörü ta ıyan karsinomlar luminal tipe uymakta, iyi gidi li grupta yer almakta ve antiöstrojen tedaviden yüksek oranda yarar görmektedir. En kötü prognozlu grup ise HER2(+) ve bazal benzeri meme karsinomlarıdır. Bu 2 grup karsinom da genelde östrojen reseptörü negatif olmakla birlikte HER2(+) olanlar Trastuzumab(Herceptin) tedavisinden faydalanırken bazal benzeri grupta hem hormon reseptörleri hem de HER2/neu onkogen ekspresyonu olmadı ından ( triple negatif: ER, PR, HER-2 negatif ) tedavi seçene i kısıtlıdır (3,9). Bazal benzeri meme karsinomlarının tüm meme karsinomları içinde ortalama (%218) % 10 kadar kısmı olu turdukları; ER (-) grupta % 30; triple (-) grupta ise % 50 den fazla yer aldıkları belirtilmekte, ancak rutin pratikte gözden kaçan ya da bu ekilde isimlendirilmedikleri için farkında olunmayan oysa gelecekte yeni tedavi modelleri için aday tümör grubu oldukları vurgulanmaktadır (7-10). Tümör grupları içinde prognozu kötü, medikal tedavilere dirençli, ER (-), PR(-), HER2(-) (triple negatif) olan bazal benzeri meme karsinomları üzerinde çok çe itli çalı malar mevcuttur (5,9). Bu çalı mada; triple negatif / bazal benzeri karsinom sıklı ının daha fazla olma olasılı ından hareketle östrojen reseptörü (-) meme karsinomları çalı ma grubu olarak seçildi. 47 ER(-) invaziv meme karsinomu vakasında; ortak morfolojik prognostik parametreler, HER2 (+)grup ve bazal benzeri grup oranı, triple negatif tümörlerdeki bazal benzeri grubun oranı, karsinomunun tanısında bu iki subgrup arasındaki farklılıklar ve bazal benzeri meme kullanılabilecek immunhistokimyasal panel de erlendirildi. Sonuç olarak; ER(-) meme karsinomlarının morfolojik, immunhistokimyasal özelliklerini daha iyi anlamak ve yeni fonksiyonel klasifikasyona göre de erlendirmek hedeflendi. 2 2) GENEL B LG LER TAR HÇE Meme kanseri insanlık tarihinde tanımlanmı ilk kanser türlerinden biridir. lk olarak tarihçi Herodot (M.Ö. 484-425), bir yazısında Darius’un karısı Atossa’nın memesinde ülserle mi bir tümör oldu unu ve bunun Pers’li doktor Democedes tarafından tedavi edildi ini belirtmi tir. Hipokrat (M.Ö 460-370), ilk olarak meme tümörlerini iyi huylu ve kötü huylu olarak ikiye ayırmı ; kötü huylu olanın yayılabildi ini ve ölüme sebep oldu unu yazmı tır. Daha sonraları skenderiye’de ya ayan D.r Leonides (M.S 80), mastektomi ameliyatını anlatmı ; Alman cerrah Wilhelm Fabry von Hilden (M.S. 1560-1624) aksiller lenf dü ümlerinin de çıkartılması gerekti ini belirtmi tir. Fransız cerrah Henri François Le Dran (1685-1770) 1757 yılında ‘‘ meme kanserinin ba langıçta lokal bir hastalık oldu unu, büyüdükçe aksiller lenf dü ümlerine ve buradan da genel dola ıma geçerek uzak organlara yayıldı ını’’ bildirmi tir. William Stewart Halsted, 1894’te ilk radikal mastektomiyi yapmı ve yaptı ı 50 vakalık radikal mastektomi serisi meme cerrahisinin temelini olu turmu tur. 1948 yılında Patey ve Dyson “Modifiye Radikal Mastektomi” tekniklerini açıklamı lardır. Son yıllarda “meme koruyucu cerrahi” teknikleri popülerlik kazanmı tır. 3 EMBR YOLOJ nsanlarda embriyonal hayatın 6. haftasında, embriyonun üzerinde, aksilladan inguinal bölgeye, do ru seklinde olan ektodermal kalınla ma süt çizgisini olu turur. Süt çizgisinin pektoral bölgedeki 1/3’lük parçasının orta kısmı daha belirgin bir ekil alarak memenin ilk tasla ını olu turur; 2/3’ lik kısmı embriyonal hayatın 9. haftasında atrofiye olarak kaybolur (13,14). Bu pektoral ektodermal kalınla ma geli mesine devam ederken, di er taraftan da derine do ru, gö üs duvarı ve mezenkimine invagine olur ve epitelial tomurcuklar geli ir. Sayıları yakla ık 15-25 kadar olan bu sekonder solid yapılar, fetal hayatın 4. ayında olu an ve yüzeyden derine do ru radier bir ekilde da ılan uzantılardır. Gebeli in son üç ayında plasentaya ait seks hormonları fetal dola ıma girerler ve bu dallanmı epitelial dokuların kanalize olmasını sa larlar. Bunlar memenin ana duktal sistemini olu tururlar. Zamanla bunlarında sekonder olarak dallanması sonucu küçük duktus ve asiniler ortaya çıkar. Do uma yakın ana kanallar ile bunların büyük dallarının geli ti i gözlenir. Parenkimal differensiasyon gebeli in 32 ile 40. haftalarında lobülo-alveoler yapıların geli mesiyle olu ur. Ayrıca meme glandı kitlesinde dört misli bir artı olur ve meme ba ını areola kompleksi geli ir.Yeni do anda uyarılan meme dokusu kolostrum salgılar ve bu salgı plasental hormonların ortadan kalkmasından sonra, memenin involusyonu sonucu 3-4 hafta içinde kesilir (13,14,15). Erken dönemlerde memenin büyümesi seks steroid hormonlarından ba ımsızdır; ancak 15. haftada meme dokusu testesterona duyarlıdır. Testesteronun mezenkimal komponentin geli mesinde etkili oldu u dü ünülmektedir (13,14,15). ANATOM Eri kin bir kadında meme glandı, genellikle ön gö üs duvarının süperfisyal pektoral fasyasının süperfisyal ve derin tabakaları arasında bulunur. Memeler 2. veya 3. kaburga ile 6. veya 7. kaburgalar arasında yer alırlar(13,14,15). Memenin yukarı-a a ı çapı ortalama 10-12 cm ve santral bölgede maksimum kalınlı ı yakla ık 5-7 cm’dir. Laktasyonda olmayan bir memenin a ırlı ı, 150-200 gr ve laktasyonda ise 400-500 gr kadardır. Areola yakla ık 2,5 cm kadardır. 4 Memenin arterleri: nternal meme arteri’nin (internal torasik arter) ön perforan dalları. Memenin yakla ık % 60’ını, özellikle medial ve santral kısımlarını besler. Lateral torasik arter (eksternal meme arteri). Memenin %30’unu, özelikle üst ve dı kadranları besler. Torakoakromial arterin pektoral dalı En üst torasik arter (Supreme torasik arter) Posterior interkostal arterlerin lateral dalları Sub kapsuler arter Torakodorsalarter Memenin venleri: nternal meme veninin perforan dalları (memenin kan ta ıyan en büyük venleridir). Aynı taraftaki innominat venlere dökülürler. Aksiller ven;gö üs duvarından ve memenin derin yüzeylerinden gelen birçok dalı alır.Bunlar genellikle aksiller arterin dallarına yanda lık ederler. nterkostal venler.Bu venler ile vertebral venler ve sonuç olarak döküldü ü azigos venler arasında ili ki mevcuttur.Her üç venöz drenaj da tümörlerin akci ere metastazında önemli rol oynarlar. Memenin sinirleri: Sensorial ve sempatik efferentlifler ta ıyan 4.,5.,6. interkostal sinirlerin anterior ve lateral dallarından geli irler. Memenin lenfatik drenajı: Memenin lenfatik drenajının %75’i aksiller lenf nodlarına, %3-25’i internal mamarial lenf nodlarına ve az bir kısmı posterior interkostal lenf nodlarınadır. Aksiller lenf nodları meme kanserinin yayılımındaki major yoldur. Aksiller lenf nodları, 1)pektoral kasın orta kısmındaki apikal ve subklaviküler lenf nodları, 2) pektoralis minorun lateralinde bulunan, aksiller veni izleyen lenf nodları, 3) pektoralis minörün altında bulunan santral lenf nodları diye üç grupta incelenir (14). Metastatik ilerlemeyi belirlemek için, aksiller lenf nodları memedeki aksiller lenfatik drenajın izledi i yola göre derecelendirilmi tir. 1. lenf nodları iki lateral kenarı arasıdır; 2. derece pektoralis minörün lateral ve medial kenarlarının arası ve arkasıdır; 3.pektoralis minörün ikik lateral kenarı ve superior kenarı arasıdır. Ayrıca 3. derece subklavikuler, intraklaviküler ve apikal nodları da içerir (16). 5 F ZYOLOJ VE H STOLOJ Meme; asini ve duktusları olu turan epitelial parenkim ve onları destekleyen muskuler ve fasyal elemanlar, de i ik miktarlarda ya , kan damarları, sinirler ve lenfatikler içerir. Epitelial parenkim, her biri ayrı bir salgı kanalı ile meme ba ına açılan 15-20 lobdan olu ur. Her lob da 20-40 kadar lobül içerir.Yani her duktus bir meme lobunu ve 2040 kadar lobülü drene eder. Lobül memedeki temel yapıdır. Lobül içi stroma interlobüler stromadan daha gev ek ve hücreseldir.Aynı stroma ince bir tabaka halinde tüm kanal sistemini çevreler. Her bir lobülde bir toplayıcı duktus çevresinde gruplanmı , sayıları 10 ile 100 arasında de i en ‘alveol’ ( asinüs duktuli) içerirler ( ekil1). Bunların sayıları ya a ve fizyolojik artlara göre de i ir. Genç kadınlarda sayıları en fazladır ve en büyük görünümdedirler.Menapozdan sonra ise lobüllerin sayısı azalır ve her biri ancak birkaç asini içeren küçük üniteler ekline dönü ürler(32). ekil 1: nsan memesindeki lobulüsler ve TDLU görünümü (Anatomy of the human breast). Kanallar asinüs grubundan ilk çıkı larında ‘terminal duktus’ , birkaç terminal duktus birle erek ‘subsegmental duktus’ , bunlar birle erek ‘segmental (laktifer ) duktus’ adını alır.Laktifer duktuslar meme ba ının hemen altında geni leyerek ‘laktifer sinüsü’ olu tururlar.Laktifer sinüsler laktasyon sırasında süt depolarlar. Kanal en son ‘toplayıcı duktus’ adını alarak meme ba ına açılırlar. Her lobül asinüsler ile terminal duktusun bu asinüs grubu içindeki kısmını içerir, buna ‘Terminal Duktus-Lobuler Ünite (TDLU)’ denir. Bu kanal sistemi memenin i levsel bölümüdür. Ancak kanal sistemini çevreleyen fibroadipöz doku meme hacminin büyük bölümünü olu turur(32,33). Toplayıcı kanalın meme ba ına açıldı ı küçük bir parçanın çokkatlı yassı epitelle dö eli olması dı ında kanal sisteminin tamamı içte lüminal kenar boyunca uzanan ve kesintisiz olarak devam eden epitelial hücre tabakası, dı ta myoepitel tabakası ile kaplıdır (5,7). 6 Epitel tabakasının uzun ekseni myoepitelial tabakanın uzun eksenine diktir. Myoepitel hücreleri duktuslarda i si görünümdedir ve az çok devamlı bir tabaka olu turur, alveollerde daha çok yıldızsı görünümdedir ve asinüsler çevresinde sepet benzeri bir yapı yaparlar, burada luminal epitel hücreleri bazal membranla daha fazla temas eder.Lobül içinde myoepitel hücreleri effaf halo ile çevrili çıplak nüveler biçiminde oldu u gibi, myoid görünüm yada ince i si hücreler biçimindede olabilir. Bu ikili tabakayı lamininden zengin bazal membran çevreler. Bununda çevresinde bir yada iki tabaka ‘sınırlayıcı fibroblastlar’ vardır (5,7,17,27). YEN PROGEN TÖR HÜCRE MODEL Deneysel çalı malar uzun zamandır meme epiteli içinde kendini ve memeyi yenileyen /tamir eden adult stem hücre varlı ını dü ündürmektedir. Ancak 10 yılı a an süredir öne sürülen bu hücreleri gösteren spesifik bir belirleyici ortaya konamamı tır. Son zamanlarda yüksek molekül a ırlıklı keratinler (CK5/14) ve hücre dizisine spesifik markerlar kullanılarak (CK8/18 ve SMA) ortak progenitör hücre varlı ı hakkında daha çok delil elde edilebilmi tir. Bildi imiz üzere meme dokusu meme ba ından terminal ünitelere kadar 2 temel tip hücreden olu ur. Dı ta-bazalde kontraktil özellikli, myoepitel hücreleri; içte ise sekretuar özellikli luminal hücre (7,17, 18). Yeni progenitör hücre modeline göre insan memesindeki progenitör hücreler; myoepitelial hücre ve glandüler hücre diferansiasyonu olmak üzere iki yönde diferansiasyon göstermektedir ( ekil2). Bu diferansiasyon sırasında ara formlarda mevcuttur (18) . Memede stem hücre konsepti giderek kabul görmekte ve bu konsepte göre fonksiyonel meme gland yapısı tek bir stem hücreden kurulabilmektedir. Karsinogenezdeki stem hücre modeline göre; stem hücrenin kendini yenileme ve diferansiasyonunda olu an aberasyon malign formasyonda anahtar rol oynamaktadır (3). 7 ekil2: Memenin progenitör hücresi ve glandüler epitel/ myoepitel hücre yönünde diferansiasyon a aması. ekil3: Progenitör hücre modeline göre meme epitel hücrelerinin diferansiasyon a amasına göre immunhistokimyasal boyanma özellikleri. Progenitör hücre modeline göre hücrelerin mmunhistokimyasal olarak boyanma özellikleri özetle u ekildedir ( ekil:3 ). 8 CK5/14 (+): Progenitör hücre. CK5/14 (+) ve CK8/18 (+) : ntermediate glandüler hücre. CK5/14 (+) ve SMA(+) : ntermediate miyoepitelial hücre. CK8/18 (+): Diferansiye glandüler hücre. SMA(+),Calponin(+),P63(+) : Diferansiye miyoepitelial hücre. Progenitör hücre: mmunhistokimyasal olarak belirgin yüksek molekül a ırlıklı sitokeratinlerin (CK5/14) ekspresyonu ile karakterize primitif hücrelerdir.Her iki yöne diferansiye olma gücüne sahiptir. ntermediate glandüler hücre:Bu hücreler glandüler diferansiasyon ile progenitör hücre arasında bulunan geçi a amasındaki ara form hücrelerdir. mmunhistokimyasal olarakda yüksek molekül a ırlıklı sitokeratinler olan CK5/14 ile beraberinde CK18 ekspresyonu gösterirler.Östrojen reseptörleri ço unlukla gözlenmez. Diferansiye glandüler hücre:CK 8/18 ekspresyonu ile karakterizelerdir.Östrojen reseptörleri vardır. Glandüler diferansiasyonun son a amasındaki hücrelerdir.Laktasyonda sayıları belirgin olarak artı gösterir. ntermediate miyoepitelial hücre:CK5/14 ve Düz kas aktini ekspresyonu ile karakterize hücreler olup, Calponin ekspresyonuda mevcuttur.Bu hücrelerde miyoepitel hücre ile progenitör hücre arasında bulunan geçi a amasındaki ara form hücrelerden olu maktadır. Miyoepitelial hücre:Düz kas aktini ve Calponin ekspresyonu gösteren terminal dönemin diferansiye hücresidir (18). 9 MEME KANSER NS DANS VE EP DEM YOLOJ Meme kanserleri, meme parenkim epitelinden, özellikle de terminal duktal lobüler ünitenin hücrelerinden geli ti i dü ünülen adenokarsinomlardır. Meme kanseri kadınlarda en sık görülen karsinomdur.Tüm kanserler içinde kadınlarda görülme sıklı ı %22 dir; bu oran geli mi ülkelerde %26’ya kadar yükselir. Mortalite açısından %18 ile akci er karsinomundan sonra ikinci sırada yer alır (1). Türkiye’de Bilimsel ve Teknik Ara tırma Kurumu’nun 1994 verilerine göre; 19851990 yıllarında kadınlarda %23,2 ile en sık görülen kanserdir (2). Tahmin edilen meme kanseri insidansı yakla ık 10-15/100 000’dir. En yüksek risk ta ıyan Kuzey Amerika, Avrupa ve Avusturalya gibi zengin ülkelerdeki tüm kadınların %6’sı 75 ya ından önce meme kanserine yakalanmaktadır (16). Ancak Afrika ve Güney ve Do u Asya ( Japonya dahil ) da bu oran di er ülkelerin üçte biri kadardır. 1980’lerden itibaren hem geli mi hem de geli mekte olan ülkelerde meme kanseri insidansı artmaktadır. Ancak erken tanı ve tedavi yöntemlerinde geli meler nedeniyle bazı ülkelerde son yıllarda mortalitede azalma saptanmı tır (16). Meme kanserleri insidansı di er pek çok epitelyal tümörde oldu u gibi ya la artar. SINIFLAMA Meme tümörlerinde günümüzde en çok Dünya Sa lık Örgütünün ( WHO ) önerdi i sınıflama kullanılmaktadır (tabo1,2) (16). 10 TABLO 1: DÜNYA SA LIK ÖRGÜTÜ SINIFLAMASI ( WHO 2003) EP TEL AL VE MYOEP TEL AL TÜMÖRLER nvaziv Duktal karsinom(NOS) Mikst tip DC. Pleomorfik tip DC. Osteoklastik dev hücreli tip DC. Koryokarsinomatöz tip DC. Melanositik tip DC. • nvaziv lobüler karsinom • Tubüler karsinom • nvaziv kribriform karsinom • Medüller karsinom • Müsinöz karsinom ve belirgin müsin • içeren di er tümörler Müsinöz karsinom Kistadeno Ca ve kolumnar hücreli müsinöz karsinom Ta lı yüzük hücreli karsinom • Nöroendokrin tümörler Solid nöroendokrin karsinom Atipik karsinoid tümör Küçük hücreli/yulaf hücreli karsinom Büyük hücreli nöroendokrin karsinom • nvaziv papiller karsinom • nvaziv mikropapiller karsinom • Apokrin karsinom • Metaplastik karsinom Pür epitelyal metaplastik karsinom Skuamöz hücreli karsinom si hücreli metaplastik karsinom Adenoskuamöz karsinom Mukoepidermoid karsinom Mikst epitelyal ve mezenkimal metaplastik karsinom. • Ya dan zengin karsinom • Sekretuar karsinom • Onkositik karsinom • Adenoid kistik karsinom Asinik hücreli karsinom • Glikojenden zengin berrak hücreli karsinom • Sebasöz karsinom • nflamatuar karsinom Lobüler neoplazi Lobüler in situ karsinom • ntraduktal proliferatif lezyonlar Basit duktal hiperplazi Flat epitelyal atipi Atipik duktal hiperplazi Duktal in situ karsinom • Mikroinvaziv karsinom • ntraduktal papiller neoplaziler Santral papillom Periferal papillom Atipik papillom ntraduktal papiller karsinom ntrakistik papiller karsinom • Benign epitelyal proliferasyonlar Adenozis ve varyanları Sklerozan adenozis Apokrin adenozis Blunt-duct adenozis Mikroglandüler adenozis Adenomiyoepitelyal adenozis Radyal skar/kompleks sklerozan lezyon Adenomlar Tubüler adenom Laktasyonel adenom Apokrin adenom Pleomorfik adenom Duktal adenom Miyoepitelyal lezyonlar • Miyoepiteliyozis • Adenomiyoepiteliyal adenozis • Adenomiyoepiteliyoma • Malign miyoepiteliyoma 11 TABLO 2: DÜNYA SA LIK ÖRGÜTÜ SINIFLAMASI ( WHO 2003) MEZENK MAL - F BROEP TEL AL VE D ER TÜMÖRLER Mezenkimal tümörler • • • • • • • • • • • • • • • • • • Hemanjiyom Anjiyomatozis Hemanjiyoperistom Psödoanjiyomatöz stromal hiperplazi Myofibroblastom Fibromatozis( agresif ) nflamatuar Myofibroblastik tümör Lipom Anjiyolipom Granüler hücreli tümör Nörofibrom Schwannom Anjiyosarkom Liposarkom Rabdomyosarkom Osteosarkom Leiomyom Leiomyosarkom Meme ba ı tümörleri • Meme ba ı adenomu • Siringomatöz adenom • Meme ba ının Paget hastalı ı Malign lenfoma • Diffüz B-hücreli lenfoma • Burkitt lenfoma • Ekstranodal malt tipi marjinal zon B-hücreli lenfoma • Folliküler lenfoma Metastatik tümörler Erkek memesinin tümörleri - Jinekomasti - Karsinom nvaziv/in situ Fibroepiteliyal tümörler • Fibroadenom • Filloides tümör Benign Borderline Malign • Periduktal stromal sarkom Mamaryal hamartom 12 ETYOLOJ Meme kanserinin etyolojisi multifaktoriyeldir ve genetik, diet, üreme faktörleri, hormonal dengesizlik gibi pekçok faktöre ba lıdır.Yapılan çalı malar meme kanserinin fiziksel egzersizin az oldu u ancak yüksek kalorili, hayvansal ya lar ve proteinlerden zengin olan "Batılı" ya am tarzı ile arttı ı gösterilmi tir ( 16). Genetik ve ailesel öykü: Meme kanseri di er kanserlere göre çok daha fazla ailesel kümelenme gösterir. Meme kanserlerinin ortalama %5-10’unun spesifik herediter mutasyonlarla ilgili oldu u kabul edilmektedir..Herediter meme kanserli kadınlarında ortalama yarısı BRCA1 geninde (kromozom 17q21.3’de lokalize ) mutasyonlara sahiptir ve ayrıca 1/3’ünde BRCA2’de mutasyonlar (kromozom 13q12-13’te) söz konusudur. Bunlar büyük kompleks yapıya sahip tümör supressör geni özelli inde genlerdir ve bu genlerin karsinogenezisteki rolü ve meme kanserine ili kin rölatif spesifitesi hala tam olarak açıklı a kavu mu olmamakla birlikte, bu genlerin ikisininde DNA tamirinde kritik bir rol oynadı ı dü ünülmektedir. (11,15,16). Reprodüktif ya am tarzı Meme kanseri riski sıklıkla erken menarj, nulliparite ve/veya geç ya ta az sayıda çocuk do urmu kadınlarda,infertil hastalarda, geç ya ta menapoza girmi kadınlarda artmı tır (19). Ayrıca laktasyonun meme kanserinde koruyucu bir faktör oldu u bulunmu tur (16). Eksojen hormonlar ki tip hormonal komponentin meme kanseri artı ıyla ilgisi bulunmu tur: oral kontraseptifler ve menapozda kullanılan hormon replasman tedavisi. Her iki ilacın kullanımında da uzun süre ve tekrarlayan kullanımlarda çok az rölatif artmı bir risk mevcuttur (15). Beslenme Yüksek oran da meyve ve sebze alımı meme kanseri riskini azaltır. Yüksek vücut kitlesi, postmenopozal hastalarda kanser geli me riskini artırır. Benzer olarak hayvansal ya ların yüksek alımı, kırmızı et tüketimi de kanser geli im riskini artırır (20). 13 Alkol ve sigara Alkol tüketimi meme kanseri riskini azaltır. Ancak sigaranın anti-östrojenik etki ile kanser geli im riskini azalttı ı dü ünülmektedir (21). Vücut a ırlı ı Otuz yıldır yapılan 100’den fazla çalı ma yüksek vücut a ırlı ının postmenopozal hastalarda meme kanseri riskini artırdı ını göstermi tir. Vücut a ırlı ı, reprodüktif, ya am tarzı risk faktörleri ve fiziksel aktiviteden ba ımsız bir risk faktörüdür. Vücut-kitle indeksi 24kg/m²’nin üstünde olan postmenapozal kadınlarda insidans oranı artmı tır (16). Fiziksel aktivite Fiziksel aktivite ve meme kanseri arasındaki ili ki menopozdan ba ımsızdır. Fiziksel olarak aktif kadınlarda bu oran %20-40 oranında azalmaktadır (20). Endojen hormonlar Epidemyolojik çalı malar seks steroidlerinin (östrojen, progesteron ve androjenlerin) meme kanserinin geli mesinde önemli rol aldı ını göstermektedir. Meme kanseri riski, ovaryal östrojen ve progesteron sentezinin kesildi i ve ovaryal androjen sentezinin kademeli olarak arttı ı, menopoz öncesi dönemde menapoz sonrası döneme göre çok daha hızlı bir artı gösterir. Yapılan havyan çalı malarında östrojenin meme dokusunda hücresel proliferasyonu artırdı ı ve apopitozisi inhibe etti i gösterilmi tir. Azalmı seks hormonu ba layan globuline ra men, artmı testesteron ve androstenodion seviyesi olanlarda,ayrıca seks hormonu ba layan globuline ba lanmamı serbest östron, östrodiol ve biyolojik olarak kullanılabilen östrodiol seviyesi yüksek postmenopozal kadınlarda artmı risk bulunmu tur. NVAZ V MEME KARS NOMU nvaziv meme kanserleri, kom u dokulara invazyon gösteren ve uzak bölgelere metastaz yapmaya meyilli olan tümör grubudur. nvaziv meme karsinomlarının yakla ık %70-80’i invaziv duktal karsinomlardır (16). NVAZ V DUKTAL KARS NOM nvaziv duktal karsinom özel tiplerin herhangi biri içinde sınıflandırılamayan tüm meme kanserleri için kullanılan bir terimdir ve bu tümörün özel bir biçimde duktal sistemden köken aldı ını göstermez.Ancak meme kanserlerinin ço unun köken aldı ı gibi, 14 invaziv duktal karsinomun da terminal duktal lobüler üniteden kaynaklandı ı dü ünülmektedir. Son yıllarda invaziv duktal karsinom adının, duktal NOS karsinom olarak kullanılması tercih edilir hale gelmi tir.Duktal NOS karsinomlar di er meme tümörlerinde oldu u gibi nadiren 40 ya altında görülürler. En sık görülen meme kanseridir. Meme kanserlerinin yakla ık %75’i invaziv duktal karsinomdur (15,16,23). Makroskobik olarak tipik vakalar sarımsı-gri renkte, çevre meme dokusuna ı ınsal uzanımlar gösteren santral bir kitle eklindedir. Kesit yüzü kumludur, nekrozun sebep oldu u beyazımsı çizgilenmeler (chalky white) bu tipe özgü bir özelliktir. Gri-beyaz sert alanlar desmoplastik stromal yanıtı gösterir. Bazen iyi sınırlı ve lobule konturlu olabilir.Tümör boyutu 10mm ile 100mm arasında de i kenlik gösterir (15,16,20,23). Mikroskobik olarak tümör hücreleri solid adalar ya da trabeküller eklinde dizilim gösterebilir, tümörün diferansiyasyonuna göre de i ken oranlarda tubül yapıları olu turabilir. Duktal karsinom hücreleri ekil ve boyutta oldukça de i kenlik gösterir, lobüler karsinoma oranla daha büyük ve pleomorfiktir, nükleolleri belirgindir. Mitoz oranı de i kendir, atipik mitozlar görülebilir. Bazen psödokist formasyonuna neden olacak kadar yo un nekroz bulunabilir. ntrasellüler ya da intralüminal müsin bulunabilir. Epitel hücrelerinde apokrin, skuamöz ya da berrak hücre metaplazisi görülebilir. nvaziv duktal karsinomlarda stroma miktarı büyük de i kenlik gösterir. Yo un hyalin ya da sellüler fibroblastik stroma görülebilir. Büyük oranda yo un hyalin stroma içermesi nedeniyle sert kıvamlı olan tümörlere eskiden skiro karsinomlar adı verilmekteydi. Kalsifikasyon sıktır, genelde epitelyal komponentin içinde bazen de stroma yer alır. Nadiren stroma da osteoklast benzeri dev hücreler ve dev hücreli granülomlar görülebilir. nvaziv duktal karsinomların %20’sinde de i en oranlarda lenfoplasmositik yanıt geli ir. Perinöral invazyon (%28), lenfatik invazyon (%33) ve kan damarı invazyonu görülebilir(15,16,20,23). Yeterli örnekleme yapıldı ında in situ karsinom oda ı görülebilir. n situ komponent genellikle duktaldir, ancak bazen in situ duktal ve in situ lobüler karsinom birarada bulunabilir (15,20). Olguların küçük bir kısmında intraduktal karsinom olmaksızın in situ lobüler karsinom invaziv duktal karsinom ile birlikte bulunabilir. nvaziv duktal karsinomun %50’sinden fazlası özel bir yapı olu turuyorsa mikst tip karsinom olarak adlandırılır (16). Duktal komponenet tümörün %10-%49’unu olu turmalıdır. Mikst karsinomlar iki grup olarak tanımlanırlar: mikst duktal ve özel tip veya mikst duktal ve lobüler karsinom. 15 Duktal NOS karsinomda 10 yıllık ya am %30-%50 arasında de i ir. Prognoz, grade, tümör boyutu, lenf nodu tutulumu ve östrojen-progesteron ve c-erbB-2 durumuna göre de i iklik gösterir (15,16). Ayrıca tümörün fokal olması ve memedeki pozisyonu da prognozda etkilidir. Pleomorfik karsinom Pleomorfik ve bizar dev tümör hücrelerinin, tümörün %50’den fazlasını olu turdu u veya tümör hücrelerinin yüksek oranda i si ve skuamöz diferansiyasyon gösterdi i yüksek gradeli bir duktal NOS karsinom tipidir. Tümöre tanı konuldu unda %12 aksiller metastaz vardır ve tümör boyutu ortalama 5,4 cm kadardır. Kavitasyon ve nekroz sık görülür. Grade III tümörlerdir. %19 lenfovasküler invazyon görülür. 3 veya daha aksiller lenf nodu metastazı olguların %50’sinde izlenir (15,16,24). Osteoklastik dev hücreli karsinom Osteoklastik dev hücrelerin karsinomların stromasında bulunmasıyla karekterlidir. Bu olguların 1/3’ünde lenf nodu metastazı mevcuttur. Be yılık ya am di er karsinomlardan daha yüksektir (%70). Prognoz karsinomun özellikleriyle ilgilidir (16). Koryokarsinomatöz özellik ta ıyan karsinom Duktal NOS karsinomlu hastaların serumlarında bazen ß-HCG düzeyleri nadiren yüksek bulunabilir(16). Melanositik özellikleri olan karsinomlar Literatürde duktal karsinom ve melanom birlikteli i sadece birkaç vakada vardır (16). NVAZ V LOBÜLER KARS NOM nvaziv lobüler karsinom varyantlarıyla birlikte tüm invaziv meme karsinomlarının yakla ık %15’ini olu turur ( 24). Makroskopik olarak düzensiz infiltratif ya da iyi sınırlı olabilece i gibi bazen lezyon çıplak gözle görülmeyebilir. Kalsifilasyonun sık görülmeyi i, diffüz büyüme paterni ve multifokal olabilmesi mamografide saptanmasını güçle tirir. Bilateral karsinom de i ik serilerde %6-28 oranında bildirilmi tir (15). 16 Mikroskobik olarak kohezyonları zayıf, küçük, üniform, yuvarlak hücrelerin lineer bir dizilim göstermesi (indian file) ya da stroma içinde dar trabeküller eklinde infiltrasyonu ile karakterizedir. Kohezyon yoklu u bu tümör için ayırt edici bir özelliktir. Tümör hücreleri duktuslar ve lobülüsler etrafında targetoid dizilim gösterirler (16,21,28). Normal glandüler yapıların korunmasına lobüler karsinomlarda sık rastlanır. Atlayıcı lezyonlar da lobüler karsinomlarda sık görülür (21). Malign hücreler daha küçük, daha az pleomorfik, mitotik figürler daha az, nekroz nadirdir. ntrasitoplazmik lümen varlı ı sık görülür. Ta lı yüzük hücreli alanlar görülebilir (15,16). nvaziv lobüler karsinomlarda stroma genellikle abondan ve yo un fibröz tiptedir. Hemen her vakada periduktal ve perivenöz elastozis oda ı görülür. nvaziv lobüler karsinomun farklı büyüme paternine sahip ancak klasik tiple aynı sitolojik özellikleri ve kohezyon kaybını gösteren bir takım varyantları vardır: solid patern, alveoler patern, tubülolobüler patern, pleomorfik-apokrin varyant (15,,16,28). nvaziv lobüler karsinomun subtiplerini mikroskopik olarak invaziv duktal karsinomdan ayırt etmek bazen çok güçtür. Klasik invaziv lobüler karsinomda %80-90 varyantlarında %50’den az in situ lobüler karsinom birlikteli i görülmektedir (15). nvaziv lobüler karsinomda aksiller lenf nodu tutunumu %3-10 arasında de i ir. Metastatik yayılım bazen izole hücreler eklinde olabilir ve histiyositlerden ayırım için immunhistokimyasal boyama gerekebilir. nvaziv lobüler karsinomun metastatik kapasitesi invaziv duktal karsinoma göre daha fazladır (15). TUBÜLER KARS NOM Meme kanserlerinin %2’sini olu turan iyi prognozlu bir tümörüdür. Genellikle duktal NOS karsinomdan daha ya lı hastalarda daha küçük boyutta, daha az aksiller metastaz yapmı olarak kar ımıza çıkar (16,20). Makroskobik olarak duktal NOS karsinomdan farkı yoktur. Ancak boyutu genellikle 0,2-2 cm arasında de i ir. Mikroskobik olarak açık bir lümen etrafını çevreleyen tek tabaka epitelyal hücrelerin olu turdu u yuvarlak veya oval tubüllerle karakterlidir. Tubüllerin bir kenarı uzamı görünümdedir. Nükleer plemorfizm ve mitotik aktivite azdır. Myoepital tabakası yoktur. Bu durum sklerozan adenozis ile ayırıcı tanısında önemlidir (15). 17 NVAZ V KR BR FORM KARS NOM Meme kanserlerinin %0.8-3.5’ini olu turur. yi prognozludur. 53-58 ya ları arasında görülür. Genellikle kitle olu turmaz. Mamografide mikrokalsifikasyonlarla karakterlidir. On yıllık ya am süresi %90-100 arasında de i ir (24). MEDÜLLER KARS NOM Meme karsinomlarının %1-7’sini olu turur. Ortalama görülme ya ı 45-52’dir. Makroskobik olarak yuvarlak iyi sınırlı ve yumu aktır. Griden beyaza kadar de i en, sıklıkla nekroz ve kanama içeren kesit yüzü vardır. Boyutu genellikle 2.0-2.9 cm arasındadır. Mikroskobik olarak medüller karsinom çok az stroma, belirgin lenfoplazmositer infiltrasyon içerisinde az diferansiye hücrelerin olu turdu u kordonlarla karekterize iyi sınırlı bir tümördür. Tümör hücrleri genellikle belirgin kırmızı bir sitoplazmaya sahiptir. Nükleer pleomorfizm ve mitoz yüksek seviyededir. Sinsityal bir yapı mevcuttur. Tümör hücreleri glandüler yapı olu turmazlar. yi bir prognoza sahiptir (15,16). MÜS N ÜRETEN KARS NOMLAR Belirgin ekstrasellüler ve intrasellüler müsin üreten tümörlerdir. Bu tümörler; müsinöz karsinom, müsinöz kist adenokarsinom ve ta lı yüzük hücreli karsinom olarak üçe ayrılırlar (16). NÖROENDOKR N TÜMÖRLER Memenin nöroendokrin tümörleri gastrointestinal sistem ve akci erdeki nöroendokrin tümörlerle aynı morfolojik özellikleri ta ırlar. %2-5 oranında görülürler ve hastaların ço unlu u altıncı veya yedinci dekadtadır. Solid nöroendokrin karsinom, küçük hücreli karsinom ve büyük hücreli nöroendokrin karsinom olarak üçe ayrılırlar (15,20). NVAZ V PAP LLER KARS NOM yi prognozlu, %1-2’den az görülen meme tümörleridir. Sıklıkla postmenopozal hastalarda görülür. Di er meme kanserlerinden ayırıcı belirgin makroskobik bir özelli i yoktur (15,16). Mikroskobik olarak, sınırlı ince veya künt papillalar ve bunların solid alanlar eklinde stromaya uzanımları ile karakterlidir. Genellikle grade II tümörlerdir. Vakaların %25’inde duktal in situ karsinom mevcuttur. Üçte birinde lenfatik invazyon vardır (15). 18 NVAZ V M KROPAP LLER KARS NOM Meme kanserleri içinde görülme sıklı ı %2’den azdır. Klini e solid kitle olarak gelirler ve ilk ba vuruda hastaların %72-75’inde aksiller lenf nodu metastazı mevcuttur (16). APOKR N KARS NOM Tümör hücrelerinin sitolojik ve immunhistokimyasal olarak %90’dan fazlasını apokrin hücrelerin olu turdu u bir karsinomdur. Prospektif serilerde meme tümörleri içinde görülme sıklı ı %0.4 bulunmu tur (15,21). METAPLAST K KARS NOMLAR Bütün meme kanserleri içinde görülme sıklı ı %1’den azdır. A a ıdaki gibi sınıflandırılırlar: Saf epitelyal Skuamöz:Büyük hücreli keratinize, i si hücreli, akantolitik tip skuamöz karsinom. si hücre differasiyasyonu gösteren adenokarsinom. Adenoskuamöz, mukoepidermoid karsinomu da içerir. Epitelyal ve mezenkimal karı ık Kondroid metaplazili karsinom Osseoz metaplazili karsinom Karsinosarkom 19 PROGNOST K PARAMETRELER 1- Hasta ya ı: 50 ya üzeri ve 35 ya altı hastaların kötü prognoza sahip oldu u bulunmu tur (10). 2- Nodal metastaz: Mastektomi ile tedavi edilen invaziv karsinomlu hastalarda, pozitif aksiller lenf nodu en önemli prognostik faktördür. Hastalıksız ya am süresi, rekürrens, rekürrens hızı ve tedaviye yanıtsızlık pozitif aksiller lenf nodu sayısı ile orantılıdır(15). Ayrıca lenf nodu metastazında ekstranodal yayılımın varlı ı da kötü bir prognostik faktördür (29). 3-Stromal invazyon:Morfololojik parametreler içinde en önemli prognostik belirleyicidir(10). 4- Tümör çapı: Evreleme sisteminde kullanılan ba ımsız bir prognostik faktördür. Primer tümörün çapı, nodal metastaz insidensi ve survi ile iyi korelasyon gösterir (15,16). 5- Tümör tipi: Klasik duktal ve lobüler karsinom arasında anlamlı prognostik bir farklılık yoktur. Tubüler karsinom, kribriform karsinom ,müsinöz karsinom, papillaer karsinom ve adenoid kistik karsinomda prognoz daha iyi, ta lı yüzük hücreli karsinom ve karsinosarkom da prognoz oldukça kötüdür (15,16,21). 6- Grade: nvaziv duktal karsinom ve di er tüm invaziv tümörler, tubül/gland formasyonu, nükleer pleomorfizm, mitotik sayıya göre "grade"lendirilir (Tablo 3) (16,20). 20 Tablo 3:Meme’nin histolojik semi-kantitatif grade’leme metodu. (Elston ve Elis’e göre) Özellik Skor Tubül ve gland formasyonu Tümörün büyük ço unlu u (>%75) 1 Orta derecede (10-75%) 2 Az veya hiç (<10%) 3 Nükleer pleomorfizm Küçük, regüler uniform hücreler 1 Orta derecede boyut artı ı ve de i kenlik 2 Belirgin de i kenlik 3 Mitotik sayı Mikroskop sahası alanına ba lıdır 1-3 Üç de i ik alan yüzölçümünde mitotik sayım örnekleri Alan çapı (mm) 0.44 0.59 0.63 Alan yüzölçümü (mm²) 0.152 0.274 0.312 1 puan 0-5 0-9 0-11 2 puan 6-10 10-19 12-22 3 puan >11 >20 >23 Mitotik sayım Grade 1 – iyi diferansiye: 3-5 puan Grade 2 – orta diferansiye: 6-7 puan Grade 3 – az diferansiye: 8-9 puan Ancak yapılan bazı çalı malar yukarıdaki histolojik gradelemenin yanında nükleer bir gradeleme sistemininde yapılması gerekti ini, nükleer gradelemenin histolojik gradeleme dı ında prognostik bir faktör oldu unu savunmu lardır. Ayrıca duktal karsinom dı ındaki meme karsinomlarında histolojik grade kullanıllamaz, daha çok nükleer gradeleme sistemi kullanılır. Contesso ve arkada larının nükleer gradeleme sistemi a a ıdaki gibidir: Nükleer Grade I- Uniform boyutta ve ekilde nukleuslar. Nükleer Grade II- Nukleuslarda orta derecede boyut artı ı ve de i kenlik. Nükleer Grade III- Yüksek seviyede de i ken, bizar, dev nukleuslar (15). 7- Evre: Çok güçlü bir prognostik faktördür. Meme kanserinin evrelendirilmesi hastalı ın anotomik yaygınlı ını de erlendirmek ve tedavinin tipini belirlemek için gereklidir. Evrelemede tümörün boyutu (T), lenf nodu metastazının olup olmaması (N) ve uzak metastazın olup olmamasını (M) esas alan TNM evreleme sistemi kullanılmaktadır (16). 21 MEME KARS NOMUNDA TNM SINIFLAMASI (WHO 2003) T- Primer tümör Tx Saptanamayan tümör. T0 Primer tümöre ait bulgu yok. Tis Karsinoma in situ. Tis(DC S) Duktal karsinoma in situ. Tis(LC S) Lobüler karsinoma in situ. Tis(Paget) Tümör olmaksızın meme ba ının Paget hastalı ı. Not:Tümörlü Paget hastalı ı tümörün boyutuna göre sınıflandırılır. T1 Tümör en büyük boyutunda 2cm veya daha az. T1mic Mikroinvazyon en büyük boyutunda 0,1cm veya daha az.* T1a Tümör en büyük boyutunda 0,1cm’den büyük , 0,5cm’den küçük ölçüde. T1b Tümör en büyük boyutunda 0,5cm’den büyük , 1cm’den küçük ölçüde. T1c Tümör en büyük boyutunda 1cm’den büyük , 2cm’den küçük ölçüde. T2 Tümör en büyük boyutunda 2cm’den büyük , 5cm’den küçük ölçüde. T3 Tümör en büyük boyutunda 5cm’den büyük ölçüde. T4 Tümörün boyutuna bakmaksızın gögüs duvarına veya deriye direkt yayılımın bulunması. Not:Gö üs duvarı tanımı, kaburgalar, interkostal kaslar,ve serratus anterior kasını içerir, ancak pektoral kası içermez. T4a Gö üs duvarına yayılım. T4b Ödem (portakal kabu u görünümü) veya meme derisinde ülserasyon veya aynı taraf memede satellit deri nodülleri. T4c Yukarıda belirtilen 4a ve4b’nin birlikte görülmesi. T4d nflamatuar karsinom.** Not:*Mikroinvazyon en büyük çapında 0,1cm’den büyük bir oda ı içermeyen kanser hücrelerinin bazal membranı a arak çevre dokulara yayılmasıdır.birden fazla mikroinvazyon oda ı varsa mikroinvazyonu sınıflamak için sadece en büyük oda ın ölçüsü de erlendirilir(tüm odakların toplamını kullanmayınız).Birden çok mikroinvazyon oda ının varlı ı, birden çok ve daha büyük invaziv karsinomlarla birlikte olabilece inden belirtilmelidir. ** Memenin inflamatuar karsinomugenellikle altta bir kitle olmaksızın meme derisinin erizipeloid sınırları olan diffüz belirgin deri endürasyonu ile karekterlidir.Klinik olarak inflamatuar karsinomun patolojik evrelemesi sırasında (T4d) ,e er deri biopsisisi negatifse ve lokalize ölçülebilir primer bir kanser yoksa T kategorisi evre pTx kabul edilir.Evre T4b veT4d’de belirtilenler hariç, meme ba ının retraksiyonu,veya di er deri de i iklikleri T1,T2,T3,,2de de sınıflamayı etkilemeksizin görülebilir. 22 N- Bölgesel Lenf Nodları Nx Bölgesel lenf nodları elde edilemiyor (örn: daha önce çıkartılmı ). N0 Bölgesel lenf nodu metastazı yok. N1 Aynı taraf fikse olmayan lenf nodları metastazı. N2 Aynı tarafın fikse lenf nodlarında metastaz veya aksiller lenf nodlarıının metaztazı olmadı ı durumlarda aynı taraf internal mamaryal lenf nodlarında klinik olarak belirgin metastaz. N2a Birbirlerine veya di er yapılara fikse olan aksiller lenf nodlarında metastaz. N2b Klinik olarak tesbit edilebilen* aynı taraf internal mamaryal lenf nodlarında metastaz, kinik olarak aksiller lenf nodları tespit edilemiyor. N3 Aynı taraf infraklaviküler lenf nodları aksiller lenf nodu metastazı olarak veya olmaksızın metastazlı;veya klinik olara aynı taraf aksiller lenf nodları ve internal mamaryal lenf nodları metastazlı; veya aynı taraf supraklaviküler lenf nodlarında aksiller ve internal mamaryal lenf nodu tututlumu olarak veya olmaksızın metastazlı. N3a nfraklaviküler lenf nodu(ları) metastazı. N3b nternal mamaryal ve aksiller lenf nodu metastazları. N3c Supraklaviküler lenf nodu(ları) metastazı. M- Uzak Metastaz Mx Uzak metastaz de erlendirilemiyor. M0 Uzak metastaz yok. M1 Uzak metastaz var. PTNM Patolojik Sınıflama pT- Primer Tümör Primer kanserin patolojik sınıflaması için rezeksiyon sınırlarında makroskobik olarak tümör hücresi görülmemelidir.Cerrahi sınırlarda sadece mikroskobik boyutlarda tümör varsa bu olgu pT olarak sınıflanabilir. pN- Bölgesel lenf nodları pNx Bölgesel lenf nodları de erlendirilemedi (daha önce çıkartılmı veya hiç çıkartılmamı ). pN0 Bölgesel lenf nodu metastazı yok.* pN1mi Mikrometastazlar (hepsi 0,2mm’den büyük fakat hiçbiri en büyük boyutunda 2mm’den büyük de il). 23 pN1 Aynı taraf 1-3 aksiller lenf nodunda metastaz ve/veya klinik olarak tespit edilemeyen, ancak sentinel lenf nodu ara tırılmasında internal mamaryal lenf nodlarında mikroskobik metastaz.** pN1a En azından bir tanesi en geni boyutunda 2mm’den büyük, 1-3 aksiller lenf bezinde metastaz. pN1b Klinik olarak tespit edilemeyen ancak sentinel lenf nodu biopsisi ile tespit edilen internal mamaryal lenf nodlarında mikroskobik metastaz. pN1c 1-3 aksiller lenf nodunda metastaz ve klinik olarak tespit edilemeyen ancak sentinel lenf nodu incelemesinde tespit edilen internal mamaryal lenf nodlarında mikroskobik metastaz. pN2 Aynı taraf aksiller lenf nodlarında 4-9 metastaz ve/veya aynı taraf aksiller lenf nodu metastazı olmaksızın, aynı taraf internal mamaryal lenf nodlarında klinik olarak tespit edilmi . pN2a 4-9 aksiller lenf nodu metastazı,en az bir tanesinde çap 2mm’den büyük. pN2b Aksiller lenf nodu metastazı olmaksızın klinik olarak tespit edilebilen internal mamaryal lenf nodlarında metastaz. pN3 Aynı taraf aksiller lenf nodlarında 10 veya daha fazla lenf nodu, veya infraklaviküler lenf nodlarında metastaz, veya klinik olarak tespit edilmi aynı taraf internal mamaryal lenf nodu metastazı ve bununla birlikte bir veya daha fazla aksiller lenf nodu metastazı, veya 3’den daha fazla aksiller lenf nodu metastazı ve bununla birlikte klinik olarak tespit edilememi ancak internal mamaryal lenf nodlarında metastaz, veya ipsilateral supraklaviküler lenf nodlarında metastaz. pN3a Aksiller lenf nodlarında 10 veya daha fazla metastaz (en az bir tanesi 2mm’den büyük) veya infraklaviküler lenf nodlarında metastaz. pN3b Klinik olarak tespit edilmi internal mamaryal lenf nodu metastazı ve bununla birlikte bir veya daha fazla aksiller lenf nodu pozitifli i, veya 3’den fazla aksiller lenf nodunda metastaz ve klinik olarak tespit edilmemi ancak sentinel lenf nodu biopsisi ile tespit edilmi internal mamaryal lenf nodunda metastaz. pN3c Supraklaviküler lenf nodlarında metastaz. Not:* Rejyonel lenf nodlarında sadece izole tümör hücrelerinin oldu u vakalar pN0 olarak sınıflandırılır. sole tümör hücreleri H&E ile bulunamayan ancak immunhistokimyasal veya moleküler metodlarla bulunan 0,2mm’den daha küçük çapa sahip tek tümör hücresi veya küçük hücre kümeleridir. TC’ler tipik olarak metastatik aktivite kanıtları göstermezler. pM- Uzak metastaz. pM kategorileri di er m kategorileri ile aynıdır (15). 24 STAGE SINIFLAMASI WHO 2003 Stage0 Tis N0 M0 Stage I T1 N0 M0 StageIIA T0 N1 M0 T1 N1 M0 T2 N0 M0 T2 N1 M0 N0 M0 T0 N2 M0 T1 N2 M0 T2 N2 M0 T3 N1,2 M0 T4 N0,N1,N2 M0 StageIIB T3 StageIIIA StageIIIB StageIIIC Herhangi T N3 M0 StageIV Herhangi T Herhangi N M1 8- Vasküler invazyon: Tümör hücrelerinin vasküler bo luklarında görülmesi lenf bezi metastazı ile kuvvetli ili kilidir. Vasküler invazyon erken lokal rekürrens ve uzak metastazın önemli bir belirleyicisidir (15). 9- Stromal reaksiyon (30). 10- Tümör nekrozu (15). 11- Cilt ve meme ba ı invazyonu (21). 12- Bilateralite (15,16). 13- Hormon reseptörleri: (ER ve PR) Hormon reseptörlerinin pozitifli i hormon tedavisi ve kemoterapiye cevap ile ili kili oldu undan meme kanserlerinde tedavinin düzenlenmesi için öströjen ve progesteron reseptörlerinin belirlenmesi günümüzde standart bir çalı madır.(10 ). Öströjen pozitif hastalarda tedaviye yanıt oranı %70 iken reseptör negatif hastalarda bu oran %5’dir.Her iki resptörüde pozitif olan hastalarda tedaviye yanıt çok daha iyidir (2,20,30). Östrojen ve benzeri ligandlar etkilerini hücre içine sızarak ve çekirdekteki ER’ne ba lanarak yapmaktadır. Bu ba lanma ile dimerize olan reseptör DNA üzerindeki hedef noktalara ba lanmaktadır (10). 25 Alfa ve Beta iki izoformu olan ER’nün alfa izoformu ‘’klasik’’ER olarak bilinen ve 595 aminoasitlik bir moleküldür.Beta formu daha kısadır ve 530 amiasitten olu ur.Her iki molekülün DNA’yı ba layan bölümü %95’e yakın bir benzerlik gösterir.Bu iki izoformun kendilerine has fizyolojik rollerini yapan hormon ba ladıkları bölümlerdeki farklılıklardır (49). ER ve PR onkogen veya tümör supressör gen sınıfına dahil edilmezler ancak meme kanserinin hem ba langıcında hemde ilerlemesinde aracı rol oynadıkllarından kanser geni gibi dü ünülebilir (49). 14- Hücre proliferasyonu: Yüksek proliferasyon hızına sahip tümörler daha kötü prognozludur. Hücre proliferasyonu mitoz sayımı, immun histokiyasal olarak ki-67, PCNA, katepsin D, p53, bcl-2, CerbB-2, EGFR ekspresyonu analizi ve flow sitometri gibi yöntemlerle belirlenir (16). Katepsin D:Asidik lizozomal bir proteazdır.Meme kanser hücrelerinin proliferasyonu ve tümör invazyonunda rol oynayan prognozla ili kili bir enzimdir (20). p53: 17. Kromozomun kısa kolunda yer alan bir tümör supressör genidir. Hücre siklusunda özellikle DNA hasarında hücrenin G1 fazından S fazına geçi in denetlenmesinde görevi vardır. p53 geninde mutasyon geli mesi bu fonksiyonun durmasına yol açar (20,30). Yapılan bir çok çalı mada meme kanserlerindeki 17 P’nin kaybı ile malign histolojik özellikler arasında yakın ili ki gösterilmi tir. P53 ekspresyonu gösteren meme kanserlerinde; yüksek histolojik grade,yüksek proliferasyon indeksi, aneploidi, ER ve PR yoklu u arasında korelasyon mevcuttur. Meme kanserlerinin %20-30’unda p53 inaktivasyonu gözlenmi tir (32). bcl-2:Mitokondrion, Endoplazmik retikulum ve nükleus membranında yerle ik bir proteindir.Hücrelerin apopitoza gidi inde rolleri vardır. bcl-2’nin meme tümör dokularında varlı ını gösteren bir çok çalı ma mevcuttur.Genelde bcl-2 ekspresyonu ER varlı ı ile korelasyon gösterirken EGFR ve p53 ekspresyonu ile zıt korelasyon gösterirler (25). CerbB-2: (Her2 /Neu): p185 olarak isimlendirilen bu onkogen 17.kromozomda q122ye yerle mi tir ve protein ürünü hücre bölünmesi ve farklıla masına katılır. Ancak gen yapısında bir de i iklik meydana geldi inde veya amplifikasyonu ve a ırı ekspresyonu nedeniyle kanser patogenezine katılan bu onkogen meme kanserleri için önemli bir prognostik marker olarak kabul edilmektedir (26). 26 CerbB-2 onkoproteini plazma membranına yerle en epidermal büyüme faktörüne benzer bir transmembran reseptör proteinidir.Bu onkogen EGFR ailesinin ikinci üyesidir. Meme karsinomlarının %15-25’unda FISH ile saptanan HER-2 amplifikasyonu ve immunhistokimyasal yöntemle saptanan protein overekspresyonu vardır (26). HER-2overekspresyonu kötü prognostik parametredir ve genellikle histolojik grade’i yüksek, lenf nodumetastazı olan ve hormon reseptörleri negatif tümörlerde görülmektedir(.mavi kitap 31,26.) CerbB-2 genini a ırı ekspreyonu veya amplifikasyonu meme kanserlerindeki transforme hücrelerin %10-40’ında gösterilmi tir.Bu onkogenin kopya sayılarının yüksek bulunu u, tümörün grade’i ile do ru orantılı olarak saptanmı tır.CerbB-2 geninin amplifikasyonuna sahip hastalarda ve metastazı bulunan meme kanserli hastalarda kullanılan ve de ilk olu turulan bioiojil düzenleyici Trastuzumab (Herceptin )’dir.Bu ilaç CerbB-2 proteinine yüksek ba lanma kapasitesine sahip, insana göre geli tirilmi rekombinant monoklonal antikordur ve CerbB-2’yi a ırı üreten meme kanser hücrelerinin büyümesini baskılar (26) EGFR:(Epidermal Büyüme Faktör Reseptörü,HER1):Hücre memebran reseptörü olan EGFR ailesi HER1,HER2,HER3,HER4’den olu ur.Her üçüde yapısal homoloji gösterirler.EGFR;170 kD’luk bir transmembran glikoproteinidir ve stoplazmik parçası trozin kinaz aktivitesi gösterir.Ligandları EGF,Heregulin ve Kripto-1’dir. EGFR gen amplifikasyonunun kötü prognozla il kili oldu u bir çok karsinomda gösterilmi tir.Kanser hücrelerinde gen amplifikasyonunun gözlenmesi onun onkogen oldu unun göstergesidir. Hormona ba ımlı ve ba ımsız meme kanserleri üzerinde yapılan bir çok çalı mada ER (-) olan tümör gruplarının ER(+) gruplardan anlamlı olarak EGFR ekspresyonu daha yüksek oranda izlenmi tir (31). BRCA1 ve BRCA2: Son 20 yıllık bir çalı mada meme karsinomlarında BRCA1 ve BRCA2 yatkınlık genleri klonlanmı tır. Bu genler DNA hasarının tamirinde rol oynayan proteinleri kodlar.Bu genlerin eksikli inde ortaya çıkan DNA hasar birikimleri kansere yol açar.Meme karsinomlarının %10’unda BRCA gen mutasyonları saptanmı tır.BRCA1 17.kromozomun q21 bölgesinde lokalizedir.BRCA2 geni ise 13.kromozomun q12-13 bölgesindedir (31). 27 Meme kanseri olan kadınların %5-10 ‘unda BRCA1 ve BRCA2 mutasyonlarının oldu u tahmin ediliyor. BRCA1 ve BRCA2 mutasyonları, Yahudi kökenli kadınlarda daha yaygın. BRCA1 ve BRCA2 mutasyonları ta ıyan kadınlarda, ya am boyu meme kanseri olu ma riski %40-85 arasında de i iyor. Meme kanseri hikayesi olan ta ıyıcıların kontralateral hastalık riski, yılda %5 kadar yüksektir. BRCA2 mutasyonları ta ıyan erkekler de yüksek meme kanseri riski ta ıyorlar. Her iki gendeki mutasyonlar aynı zamanda yüksek over kanseri riskine de yol açar. Ek olarak, mutasyon ta ıyıcıları di er kanserler için de yüksek risk ta ıyor olabilirler ( 31,47 ). MEME KANSER SINIFLAMASINA YEN YAKLA IM VE BAZAL BENZER MEME KARS NOMLARI Meme kanseri; morfolojik, prognostik ve tedaviye cevap açısından oldukça heterojen bir hastalık olup bu heterojenite nedeni olarak altta yatan hedef hücre (kanser hücresi) popülasyonundaki farklılık, farklı onkogen aktivasyonu ve/veya tümör supresor gen fonksiyon kayıplarındaki de i ik kombinasyonlar suçlanmaktadır. Fakat yıllardır morfoloji temelli bir klasifikasyon temelinden hareket edilmektedir. Son çalı malar meme kanserlerinde CK5 ve CK14 ve CK 17 varlı ını ara tırmakta ve klasifikasyonu buna dayanarak yapmaya yönelmektedir. Bu tip keratin ekspresyonunu gösteren sporadik karsinomların kötü prognozlu ve BRCA1 ile ili kili oldukları üzerinde durulmaktadır (47). Bu önemli gözlem “fonksiyonel meme kanseri”denen yeni bir sınıflamaya götürmektedir. Bu sonuçlar kanserli meme dokusu kadar normal meme dokusunun da incelenmesi ve ekspresyon profilinin ara tırılmasına yöneltmi tir. Meme dokusu meme ba ından terminal ünitelere kadar 2 temel tip hücreden olu ur. Dı ta-bazalde kontraktil özellikli, epitel hücreleri (myoepitel) ; içte ise sekretuar özellikli luminal hücre. Deneysel çalı malar uzun zamandır meme epiteli içinde kendini ve memeyi yenileyen /tamir eden adult stem hücre varlı ını ara tırmaktadır. Ancak 10 yılı a an süredir öne sürülen bu hücreleri gösteren spesifik bir belirleyici ortaya konamamı tır. Son zamanlarda yüksek molkül.a ırlıklı keratinler (CK5/14) ve hücre dizisine spesifik markerler kullanılarak (CK8/18 ve SMA) ortak progenitör hücre varlı ı hakkında daha çok delil elde edilebilmi tir (9). 28 1980’li yılların ba larında Moll ve arkada ları de i ik insan tümörlerinde CK ekspresyonlarını ara tırarak katalog haline getirmeyi amaçladılar ve çalı maya alınan 7 meme kanseri olgusundan 4’ü basit tip sitokeratinleri (CK 7, 8,18 ve 19) eksprese ederken 3’ünde ilaveten Ck 6 ekspresyonu bulundu. Daha sonraki 3 yılda epidermisin bazal tabaka hücrelerinin CK 5 ve CK14’ ün de içinde oldu u bir grup sitokeratini eksprese etti i anla ıldı ve bu keratinlere bazal tip keratinler dendi. Meme ve bazı organlarda myoepitel denilen hücrelerin bazal CK eksprese etti i de anla ıldı. Ayrıca myoepitelial tümör / karsinomlar yanısıra duktal ve lobüler karsinomlarda da bazal tip siitokeratinlerin ekspresse olabildi i görüldü ( % 0- % 17,4) (34). 1987’de Dairkee ve arkada ları memede bazal CK(+) karsinomların daha erken rekürrens yaptı ını ve prognostik öneme sahip olabilece ini belirttiler (35). 1990 da Domagala ve arkada ları vimentin ekpresse eden lenf nodu metastazı negatif, fakat 5 yıl içinde kötü gidi gösteren bir grup tümör tanımladılar. Bunlar aynı zamanda geni santral nekrozlu, yüksek grade’li, mitotik indeksi yüksek, ER(-) tümörlerdi.(35) Santini ve arkada ları da benzer özellikte ayrıca EGFR(+), CK14-17 (+), SMA(+) tümörler tanımladılar (36). 1998’de Malzahn ve arkada ları vimentin(-), grade3 ve ER(-) tümörler içinde CK5-14-17 pozitifli i gösteren küçük bir alt grubun tüm sa kalım ve hastalıksız sa kalım açısından kısa survive sahip olabilece ini ileri sürdüler. Sonuç olarak bu grup tümörler son zamanlarda sık bahsedilen moleküler çalı malarında ilgi oda ı haline gelmi ve son 10 yılda moleküler çalı malar hız kazanmı binlerce genin e zamanlı olarak de erlendirilmesi imkanı do mu tur. Tümör dokusu örneklerinden gen ekspresyon profili (GEP) çıkarılarak meme kanserlerinde yeni moleküler klasifikasyona gidilmi tir (37). Memede GEP’e dayalı kanser klasifikasyon çalı maları ilk kez 2000’de Perou ve arkada ları tarafından ba latıldı ( 38 ). Meme karsinomlarının cDNA mikroarray yöntemi ile gen ekspresyonları incelendi ve bu sonuçlara göre gruplara ayrıldı (38). GEP sonuçları genellikle 5 ana gruptan bahsetmektedir ( ekil4). Luminal A, Luminal B, Normal meme benzeri, Her-2 overeksprese eden, Bazal benzeri (9). 29 Luminal: ER(+)dir.ve ER ‘ye cevap veren genler ekspresse olmu tur. Ayrıca PR, GATA3, BCL2 ekspresyonuda yüksektir. Her-2 overekspresyonu zayıftır. Luminal A’da ER ile ili kili genler daha fazla ekspresse edilirken, Luminal B’de proliferatif genlerin ekspresyonu daha fazladır. Özellikle Her-2 overekspresyonu yüksektir. CK8/18 Luminal A’da yüksek orandadır, Luminal B’de de i kendir . Bazal benzeri : ER(-), Her-2(-), Myoepitel marker ekspresyonu dü ük, EGFR, Pcatherin, cKit, Bazal sitokeratin(CK5/6,CK14,CK17) ekspresyonu yüksek, kötü prognoz, genç ya , BRCA1 gen mutasyonu ile ili kili tümörlerdir . ncelenen bazal benzeri tümörlerin morfolojik olarak genelde grade 3, Duktal/NOS veya metaplastik., co rafik nekrozu sık, itici invazyon sınırı, stromal lenfositik cevabı yüksek oldu u gözlenmi tir. Her-2 overekspresse eden:HER-2 onkogen ekspresyonu yüksek olup, ER(-) tümörlerdir. Normal meme benzeri: Gen ekspresyonu olarak Bazal epitel hücre ve adipöz doku hücre genleri yüksek derecede eksprese edilirken, lüminal epitel gen ekpresyonu. Zayıftır. Bazı literatürlerde yapılan HK çalı malarında boyanma izlenemedi inden dolayı isimlendirilemeyen (undetermine) grup da denilmektedir(18,40,47,51). ekil 4: Perou ve arkada larının 82 meme karsinomu olgusunda 689 intrensek gen seti hazırlanarak yapılan GEP sonucunda olu an 4 subgrup. Her-2 pozitif (kahverengi), luminal (mavi), normal meme benzeri (ye il), bazal benzeri (turuncu). (From Rouzier R, Perou CM, Symmans WF et al. Breast cancer molecular subtypes respond differently to preoperative) . 30 Nielsen ve arkada ları bazal benzeri tümör grubunu incelediler ve bu gruba yapılan IHK çalı malar sonucu: ER(-), HER.2(-), Bazal CK(+), EGFR(+), c.kit(+) buldular (tablo 4). Bu panelin basal benzeri meme karsinomların identifikasyonu için çok uygun oldu unu, EGFR (HER.-1) ve c.kit pozitifli inin yeni tedavi hedefi olabilece ini vurguladılar (40). Tablo 4: Nielsen.O.T ve arkada larının çalı masında 663 meme karsinomu olgusuna uygulanan cDNA Mikroarray analizi sonucu olu an 4 grubun mmun histokimyasal karakterleri . (a) HER2 pozitif ( 3+ membranöz boyanma ) grup H olarak isimlendirilmi .; (b) HER2 negatif ve ER pozitif, ise grup E; (c) E er tümor HER-2 ve ER negatif ama bazal sitokeratin ve veya EGFR ile pozitif ise (CK 5/6, ve/veya EGFR) grup B; (d) E er tumor 4 marker ile boyanmıyorsa , grup N (undetermine) olarak isimlendirilmi tir. Bazal grup % 15 oranında izlenmi tir (40). Grup HER2 ER sitokeratin 5/6 ve/veya EGFR H (HER2) Pozitif negatif negatif Boyanma oranı (%) 150 (%23) E (luminal) Negatif Pozitif negatif 263 (%40) B (bazal tip) Negatif Negatif Biri veya her ikisi pozitif 102 (%15) N (negatif) Negatif Negatif Negatif 148 (22) Fulford ve Easton a göre; meme kanseri yaygın ve heterojen bir hastalık grubudur. Klinik olarak bu kadar geni da ılım göstermelerine ra men ço u meme kanseri (%75-80) aynı histolojik tanıyı (NOS- invaziv duktal karsinom) almaktadır. Tümörlerin büyük bir bölümü luminal fenotipte olup; memenin duktus ve asinüslerindeki iç kısımda (luminal yüz) yer alan hücrelerin salgıladı ı proteinleri ekspresse ederler. Bunlar; ER, PR, CK8, CK18 ve CK19’ dur. Ancak meme kanserlerinin %2-18’i ise memenin duktus ve asinüslerindeki dı kısımda yer alan kontraktil miyoepitel veya bazal tabaka hücrelerinin salgıladı ı proteinleri ekspresse ederler. Bu proteinler yüksek molekül a ırlıklı sitokeratinler CK14, CK5/6, CK17 ) ve düz kas aktini markerleridir. ( SMA, Calponin, p63 ). Henüz bu grup tümörler rutin pratikte tanınamamakta ve terminolojileri konusunda da net bir konsensus yoktur. Bu kadar büyük oranda görülen kanserin tek bir histolojik kategoriye sokulması çok anlamlı de ildir. Farklı ara tırmacılar, bu tümörlere bazaloid, bazal benzeri veya miyoepitel diferansiasyon gösteren duktal karsinom gibi de i ik isimler vermektedir. Bu tipler genelde kötü prognozlu, beyin ve akci er metastazları sıktır. Surveyleri kısa, ER(-) ve HER-2 (-) oldukları için monoterapi ansları yoktur. 31 Sonuç olarak; mmunhistokimyasal olarak CK5/6, ER, HER-2, EGFR paneli basal benzeri meme karsinomlarını belirlemek için iyi bir kombinasyon’dur (9). Fulford G ve arkada ları ba ka bir çalı masında bazal benzeri meme karsinomlarını uzun dönem survey ve metastaz açısından incelediler ve 443 grade3 Invaziv duktal karsinom olgusunda yapılan HK çalı mada %20 olguda CK14 (+) bulundu. Basal benzeri tümörlerin farklı biyolojik davranı a sahip olup lenf nodu , karaci er ve kemik metastazları az ancak beyin metastazı daha çok oldu u gözlendi. Uzun süreli survey CK14 pozitiflerde negatiflere göre daha iyi gibi görünsede metastaz yaptı ında kötü klinik seyirin hızlandı ı gözlendi. Bazal benzeri tümörlerinde kendi aralarında da heterojen oldu u; >%90 CK 14 (+) ise : Diffüz Bazal : daha iyi prognozlu, < %90 CK(+)ise Bazoluminal tip : Daha kötü prognozlu oldu u gözlendi ( ekil 5) (41). Laakso M ve arkada larına göre, bazal CK eksprese eden meme kanserleri tipik olarak ER(-)’dir ve farklı gen ekspresyonları ile ayrı bir antitedir denildi. Bu grup içinde de birden fazla biyolojik antite oldu u ileri sürüldü. IHK olarak CK5/14 ekspresyonlarına bakıldı, image analizi ile boyanma yüzdeleri de erlendirildi. Sonuçlar olguların klinikopatolojik özellikleri ve relapssız geçen süreleri ile kar ıla tırıldı. CK5/14 pozitifli i % 10,5 olguda saptandı. %5-69 boyanma heterojen (dama tahtası benzeri) bazoluminal, %70> boyanma diffüz bazal olarak kabul edildi (grafik1) (42). Grafik1: Tümör hücrelerinin CK5/14 ekspresyon derecelerine göre da ılımı. Hetrojenöz boyanma gösterenler bazoluminal, uniform boyanma gösterenler diffüz bazal subtip olarak isimlendirilmi tir. CK14 ile boyanma oranı: %5-69:bazoluminal tip , % 70 ise diffüz bazal tip ( 42). 32 ekil 5 .Bazal CK ve Luminal CK ekspreyonuna göre meme karsinomu klasifikasyonu. Bazal benzeri tümörler ço unlukla memenin (primitif )progenitör hücreleri ile aynı özellikte olup luminal fenotipli tümörler; memenin diferansiye glandüler hücresiyle benzer özellik gösterirler. Bazoluminal tümörler intermediate fenotipte olup, heterojenöz bazal sitokeratin ekspresyonu ve yüksek HER-2 overekspresyonu gözlenir (41 ). 33 3) MATERYAL VE METOD Çalı mamızda 2001-2007 tarihleri arasında stanbul E itim ve Ara tırma Hastanesinde meme karsinomu nedeniyle opere edilerek patoloji labaratuarına gönderilen mastektomi ve eksizyonel biopsi materyalleri incelendi. Bunlardan 47 Öströjen reseptörü ile negatif boyanan, 16 Öströjen reseptörü ile pozitif boyanan invaziv meme karsinomu olgusu de erlendirilmeye elveri li bulunarak çalı ma kapsamına alındı. Hastalara ait klinik bilgiler, tümörün lokalizasyonu, boyutu ve aksiller lenf nodlarına yayılıp yayılmadı ı ar iv kayıtlarından elde edildi. Olgulara ait labratuarımızın ar ivinde bulunan H&E ile boyalı preparatlar yeniden incelendi. Tümörün histolojik tipi, histolojik grade, anjiolenfatik invazyon, aksiller lenf nodu metastaz sayısı, santral nekroz ve fibroz, inflamatuar stromal cevap, infiltrasyon paterni de erlendirildi. Her olgu için kanama ve nekroz içermeyen ve tümörü en iyi temsil eden bloklar seçildi. Bu bloklardan 4 mikron kalınlı ında kesitler elde edilip immunhistokimyasal olarak; ER, PR, CerbB-2, SMA, Calponin, P63, CK5/6, CK14, CK17, CK 18, BRCA1 antikorları uygulandı. Olgular tümör boyutuna göre pTNM sınıflaması esas alınarak 0-2cm (T1), 2-5cm (T2), 5cm’nin üstü (T3) olarak gruplara ayrıldı. Gradeleme Elston ve Ellis’in histolojik grade’leme sistemine göre ve Contesso’nun nükleer gradeleme sistemine göre yapıldı. Tümöral lenfositik yanıt, tümör çevresindeki lenfoplazmositer infiltrasyonun iddetine göre hafif, orta, a ır eklinde gruplandırıldı. 34 Anjiolenfatik invazyon için lenfatikleri ve vasküler yapıları dö eyici endotel hücrelerinin seçilmesi ve bu hücre gruplarının, endotel hücreleri ile temasta olması esas alınarak pozitif ve negatif olarak de erlendirildi. Aksiller lenf nodu durumu de erlendirmesi pTNM sınıflamasındaki N sınıflaması esas olarak alınarak; aynı taraf lenf nodunda metastaz yok(N0), aynı taraf 1-3 aksiller lenf nodunda metastaz (N1), aynı taraf 4-9 aksiller lenf nodunda metastaz (N2), aynı taraf aksiller lenf nodunda 10 veya daha fazla metastaz (N3) eklinde de erlendirildi. nternal mamaryal ve di er bölgesel lenf nodları klinik bilgi yetersiz oldu u için de erlendirilemedi. Östrojen-progesteron reseptör boyanması %5’dan az ise ( - ), %5’dan fazla ise (+) olarak de erlendirildi. CerbB-2 için overekspresyon skoru kullanıldı. Yaygın, kuvvetli komplet membranöz boyanma: skor3 pozitif olarak kabul edidi. KULLANILAN ANT KORLAR Çalı mamızda toplam 63 olguya ER, PR, CerbB-2, Calponin, SMA, p63, CK5/6, CK14, CK17, CK18, BRCA1 antikorları çalı ıldı . Kullandı ımız antikorlardan CK14 kullanıma hazır olup di erleri liyofilize doku kültürlerinden elde edildi i için, kendi dilüsyon oranlarına göre distile su ile sulandırıldı (Tablo5). TABLO 5: KULLANILAN PR MER ANT KORLAR Antikor Firma Klon Dilusyon ER Neomarkers SP1 1:80 PR Neomarkers SP2 1:200 CerbB2 Neomarkers e-4001+3B5 1:600 SMA Neomarkers 1A4 1:150 P63 Neomarkers 4A4+Y4A3 1:300 Calponin Neomarkers CALP 1:200 CK5/6 Dako D5/6B4 1:100 CK14 Neomarkers LL002 Kullanıma hazır. CK17 Neomarkers E3 1:100 CK18 Thermo DCLO 1:200 BRCA-1 Dako GLK-2 1:100 35 MUNH STOK MYASAL BOYAMA YÖNTEM mmunhistokimyasal çalı ma streptovidin – avidin – biotin yöntemiyle yapıldı. Olgulara immunhistokimyasal yöntem ile boyama için formalin fiksasyonlu parafin gömülü bloklardan Pozitif Charge'li lamlara 4-5 mikronluk kesitler alındı. Tüm kesitler deparafinize edilmek üzere etüvde bir gece bekletildi. 15 dakika içinde be kez ksilenden geçirilmek suretiyle deparafinizasyona devam edildi. Daha sonra 20 dakika içinde üç farklı %99’luk etil alkol ve üç farklı %96’lık alkolden geçirilerek kesitler hidrate edildi. Distile suda be dakika yıkandı. Mikrodalga fırında 4 defa 5 dakika CK5/6 için 0.01M’lik edta buffer, di erleri için 0.01M’lik sitrat buffer uygulaması yapıldı. Mikrodalgadan sonra, 20 dakika oda ısısına gelinceya kadar bekletildi. Distile su ile yıkandı. PBS (Phosphate Buffered Saline)‘de 2 kez 3’er dakika bekletildi. Lam üzerindeki dokuların etrafı hidrofobik kalemle çizildi. %3’lük Hidrojen peroksit ile 15 dakika bekletildikten sonra, enzim isteyen antikorlardan Calponin için; Tripsin, CK5/6 için Proteinaz K damlatılıp 5 dakika bekletildikten sonra PBS’de 2 kez 3’er dakika bekletildi. Ultra V Blok damlatılarak 10 dakika inkübasyona bırakıldı. Yıkamadan sonra primer antikorları damlatılarak 1 saat süreyle inkübasyona bırakıldı. PBS’de 2 kez 3’er dakika geçirildi. “Polyvalent secondary antibody” ile 15 dakika inkübe edildi. PBS’de 2 kez 3’er dakika bekletildikten sonra 15 dakika süreyle Streptavidin Peroksidaz serumu uygulandı. Tekrar PBS’den geçirilen dokular AEC(kromojen) ile 15 dakika inkübe edildi. Renk alan camlar çe me suyunda yıkandıktan sonra mayer hematoksilende bir dakika bekletildi. Son olarak kesitler su bazlı bir balsam ile kapatıldı. MMUNH STOK MYASAL DE ERLEND RME Boyanan preparatlar ı ık mikroskobunda incelendi. ER, PR, Sitokeratinler (CK5/6, CK14, CK17, CK18), BRCA1, p63, Calponin, SMA için pozitif kontrol olarak internal alanlardaki normal memenin epitelial ve miyoepitelial ve düz kas hücreleri kullanıldı. CerbB-2 için pozitif kontrol olarak, daha önce kuvvetli pozitif boyandı ı bilinen, eksternal kontrol bloklar kullanıldı. Hücrelerdeki boyanma semikantitatif bir skala ile de erlendirildi (H skoru). - Boyanma yok. - Fokal alanlarda seyrek boyanma( %1-4 ) veya arada tek tek pozitif hücreler. - En azından bir odakta( %5-69) kuvvetli boyanma veya çok sayıda alanda ortadan zayıfa kadar de i en boyanma. 36 - Neoplastik hücrelerin %70’inden daha fazlasında kuvvetli boyanma . ER, PR, P63 için nükleer boyanma, CerbB-2, için stoplazmik membranöz boyanma, Sitokeratinler, SMA, Calponin, BRCA1 için stoplazmik boyanma paternleri pozitif olarak kabul edildi. STAT KSEL DE ERLEND RME Bu çalı mada istatistiksel analizler GraphPad Prisma V.3 paket programı ile yapılmı tır. Verilerin de erlendirilmesinde tanımlayıcı istatistiksel metotların (ortalama,standart sapma) yanı sıra nitel verilerin kar ıla tırmalarında ki-kare gerçeklik testi ve Fisher’in kesin olasılık testi kullanıldı. Sonuçlar, anlamlılık p<0,05 düzeyinde de erlendirilmi tir. 37 4) BULGULAR 2000-2007 yılları arasında stanbul E itim ve Ara tırma Hastanesi’nde, eksizyonel biopsi, lumpektomi, basit mastektomi, modifiye radikal mastektomi ve aksiller disseksiyon yapılan, patoloji bölümünde invaziv meme karsinomu tanısı alan, öströjen reseptörü negatif 47 olgu çalı ma grubunu olu turdu. Kontrol grubu olarak 16 Östrojen reseptörü pozitif invaziv meme karsinomu olgusu kullanıldı. ER (-) olguların %’78’i invaziv duktal karsinom NOS, %6,3’ü metaplastik karsinom, %'6,3’ü myoepitelial diferansiasyon gösteren nvaziv duktal karsinom, %2,2’si nöroendokrin diferansiasyon gösteren nvaziv duktal karsinom, % 2,2'si Apokrin diferansiasyon gösteren nvaziv duktal karsinom, %4,25'i invaziv lobüler karsinom, % 2,2’si’ mikst(müsinöz+ duktal) karsinom, % 2,2’si’mikst (lobuler+müsinöz) karsinomdu. En genç hasta 27, en ya lı hasta 79 ya ında olup, ortalama hasta ya ı 52’idi. Olguların %36’sı Tüm karsinomlara nükleer grade’leme yapıldı. nükleer grade (NG)II, %64’ü nükleer grade (NG)III olarak de erlendirildi. Tümör çapları TNM klasifikasyonuna göre gruplandırıldı. Olguların ortalama tumor çapı 3,6 cm olup %14’ü T1(0-2 cm), %.86.'sı T2(2-5 cm) ve T3 (5 cm üzeri)'dü. Olguların %64’ünde anjiolenfatik invazyon tespit edilmedi; % 36’sında anjiolenfatik invazyon mevcuttu. %36,5’inde iltihabi stromal yanıt hafif, %29,5’inde orta, %39,5’inde belirgindi.(Resim: 2). %27,65’inde pushing margin (Resim1 ) , %42,5’inde santral fibroznekroz mevcuttu. Tümör nekrozu 41 (%87,23) olguda mevcut olup 6 (%12,77) olguda izlenmedi. 38 Aksiller lenf bezi metastazı sınıflandırılması TNM klasifikasyonuna göre yapıldı. ER(-) olguların %41,2’sinde aksiller lenf bezi metastazı saptanmadı (N0), %58,8’inde aksiller lenf bezi metastazı mevcuttu. %25,6’sı N1(1-3), %7,6’sı N2(4-9), %25,6’sı N3(10 ve üzeri) olarak saptandı (Tablo14). Kontrol grubu olan ER (+) olguların %81,25’ NOS nvaziv Duktal Karsinom, %6,25’i mikst( lobüler+ duktal) karsinom, %12,25'i lobuler karsinomdu. En genç hasta 22, en ya lı hasta 70ya ında olup, ortalama hasta ya 53’dü. %18,5’i nükleer grade (NG)I, %68,5'i nükleer grade (NG)II, %13'ü nükleer grade (NG)III olarak de erlendirildi. Tümör çapları ortalama 3,4 cm olup, TNM’e göre %33,5’i’ T1(0-2 cm), %66,5’i T2(2-5 cm) ve T3(5 cm üzeri)’ dü. %87,5’inde anjiolenfatik invazyon tespit edilmedi; %12,5’inde anjiolenfatik invazyon mevcuttu. %64,5’inde iltahabi stromal yanıt hafif, %23,5’inda orta, %12'sinde belirgindi. . Olguların hepsi infiltratif karakterde olup santral fibrozis-nekroz izlenmedi. Tümör nekrozu %37,5 olguda mevcut olup %62 olguda izlenmedi (Tablo15). ER negatif olgularında yapılan immunhistokimyasal boyanma sonuçlarına göre; CerbB-2 ile %21.2, CK5/6 ile %42.4, CK14 ile %38.3, CK17 ile %36.2, CK18 ile %63.6, SMA ile %21.2, Calponin ile %21.2, p63 ile %14.9, BRCA1 ile %.55.3 pozitif boyanma izlendi (Tablo:16,18). Kontrol grubu olan ER pozitif olguların immunhistokimyasal boyanma sonuçlarına göre; CerbB-2 ile %.25, CK5/6 ile %6.25, CK14 ile %6.25, CK17 ile %6.25, CK18 ile %100, BRCA1 ile %31.25 pozitif boyanma izlendi. SMA, Calponin, p63 ile boyanma izlenmedi (Tablo17,18). HK analiz sonucunda ER negatif tümörlerde 6 olguda( %12,76 ) sadece bazal sitokeratinlerle ( CK5/6, CK17, CK 14) pozitif boyanma izlendi. 10 Olguda( %21,7 ) bazal sitokeratin ve luminal sitokeratin( CK18) ile pozitif boyanma izlendi. 10 olguda (%21) myoepitel markerler ( SMA, Calponin, p63) , ve veya CK14, CK18 ile pozitif boyanma izlendi. 4 olguda (%8,5) luminal sitokeratin, bazal sitokeratin ve miyoepitel markerlerle boyanma izlenmedi. 17 olguda(%36,17) sadece luminal sitokeratin(CK18)'le pozitif boyanma izlendi (Tablo:16,19). ER(-) tumor grubunda CerbB-2 ile 10 olguda overekspresyon izlendi.(resim8). Bunlardan bir olguda skor:2, di erlerin skor:3’dü. HER-2 pozitif 10 olgunun 6’sı sadece luminal sitokeratin(CK18) ile , 3 tanesi bazal ve luminal sitokeratinlerle, 1 olguda sadece bazal sitokeratinlerle pozitif boyanma izlendi (Tablo16). 39 Triple negatif 37 olgu saptandı. Bunlardan 11 olguda sadece luminal sitokeratinlerle, 5 olguda sadece bazal sitokeratinlerle, 7 olguda bazal ve luminal sitokeratinlerle pozitif boyanma izlendi. 4 olguda hiçbir antikorla boyanma izlenmedi. (Tablo:16,25) ER (+) tümörlerin HK analiz sonuçlarına göre bir olguda (%6,25) bazal CK+luminal CK ile pozitif boyanma ve CerbB-2 ile overekspresyon izlendi. 16 olguda da luminal sitokeratin(CK18)'le pozitif boyanma mevcuttu (tablo19). Çalı mamızdaki verilerin de erlendirilmesinde tanımlayıcı istatistiksel metotların (ortalama,standart sapma) yanı sıra nitel verilerin kar ıla tırmalarında ki-kare gerçeklik testi ve Fisher’in kesin olasılık testi kullanıldı. TABLO 6: ER NEGAT FL VE HASTA YA I L K S HASTA YA I ER POZ T F ER NEGAT F (kontrol grup) Hasta ya ı N:16 N:47 50 Ya altı 4 %25 23 49 50 Ya üzeri 12 %75 24 51 ER negatifli i ile hasta ya ları ²:1,9 P=0,169 kar ıla tırıldı ında ER negatif olguların ya ortalaması 52, ER pozitif olguların ya ortalaması 53 bulunmu ; ER negatifli i ve ya arasında istatistiksel bir anlam elde edilememi tir. (p>0,05) ER negatifli i ve hasta ya ı 80 70 60 50 50 ta altı 40 50 ya üstü 30 20 10 0 ER(+) ER(-) Grafik 2: ER negatifli i ve hasta ya ı. 40 TABLO 7: ER NEGAT FL VE TÜMÖR ÇAPI L K S TÜMÖR ER POZ T F ER NEGAT F (kontrol grup) N:16 % N:47 % Ki-kare TÜMÖR ÇAPI ²:0,57 0-2 CM 4 %33.5 6 %14.6 2 CM ÜZER 12 %66.5 41 %85.4 P P=0,446 ER negatifli i ile tumor çapları kar ıla tırıldı ında ER (-) olguların tumor çapı ortalaması 3.6 cm , ER pozitif olguların tumor çapı ortalaması 3.4 cm bulunmu ve ER negatifli i ile tümör çapı arasında istatistiksel bir anlam elde edilememi tir. (p>0,05) TÜMÖR ÇAPI 90 80 70 60 50 0-2 CM 40 2 CM ÜZER 30 20 10 0 ER POZ T F ER NEGAT F Grafik 3:ER negatifli i ve tümör çapı TABLO 8: ER (-) GRUBUN MORFOLOJ K ÖZELL KLER - Morfolojik özellikler olgu sayısı - Pushing margin 13 %27,6 - Lymphoid stroma (belirgin) 16 %34 - Berrak hücreli de i iklik 9 %19,15 - I si hücreli de i iklik 9 %19,15 - Komedo-tip nekroz 17 %36,2 - Skuamoid de i iklik 6 %12,75 - Undiferansiye/küçük hücre 2 %4,25 - Tumöral dev hücre 15 %32 - Santral nekroz/fibroz 20 %42 41 (%) TABLO 9: ER NEGAT FL VE LT HAB STROMAL YANIT ER POZ T F ER NEGAT F N:16 % N:47 % HAF F 11 %64,5 17 %36.5 ORTA 4 %23.5 14 %29.5 1 %12 16 %34 ltihabi yanıt DDETL ²:6,3 P=0,041 ER negatifli i ile iltihabi stromal yanıt kar ıla tırıldı ında ER negative olguların % 34’ünde belirgin iltihabi yanıt varken , ER pozitif olguların %12’sinde belirgin iltihabi yanıt gözlenmi tir ve ER negatifli i ile iltihabi stromal cevap arasında istatiksel olarak belirgin anlamda ili ki elde edilmi tir. (p<0,05). TABLO 10: ER NEGAT FL ER POZ T F VE NÜKLEER GRADE ER NEGAT F (kontrol grup) ²:17,85 N:16 % N:47 % NG1 3 % 18.5 0 0 NG2 11 %68.5 17 %36 NG3 2 %13 30 %64 Nükleer grade ER negatifli i ile P=0,0001 nükleer grade kar ıla tırıldı ında ER negatif olguların % 64’ünde NG3 iken , ER pozitif olguların %13’ünde NG3 gözlenmi tir . ER negatifli i ile NG arasında istatiksel olarak belirgin anlamda ili ki elde edilmi tir. (p<0,05) NÜKLEER GRADE 80 70 60 50 ER POZ T F 40 ER NEGAT F 30 20 10 0 NG1 NG2 NG3 Grafik 4: ER negatifli i ve nükleer grade. 42 TABLO 11: ER NEGAT FL VE DAMAR NVAZYONU ER POZ T F ER NEGAT F (kontrol grup) DAMAR N:16 % N:47 % ²:2,15 NVAZYONU P=0,142 VAR 2 %12,5 17 %36,17 YOK 14 %87,5 30 %63,83 ER negatifli i ile anjiolenfatik invazyon kar ıla tırıldı ında ER negative olguların %36,17’sinde anjiolenfatik invazyon varken, ER pozitif olguların %12,5’inde anjiolenfatik invazyon saptanmı tır. ER negatifli i ile anjiolenfatik invazyon arasında istatistiksel bir anlam elde edilememi tir. (p>0,05). DAMAR NVAZYONU 100 90 80 70 60 VAR 50 YOK 40 30 20 10 0 ER POZ T F ER NEGAT F Grafik 5: ER negatifli i ve anjiolenfatik invazyon. 43 TABLO 12: ER NEGAT FL ER POZ T F VE TÜMÖR NEKROZU ER NEGAT F (kontrol grup) Tümör nekrozu N:16 % N:47 % VAR 6 %37,5 41 %87,23 YOK 10 %62,5 6 %12,77 ²:13,06 P=0,0003 ER negatifli i ile tümör nekrozu kar ıla tırıldı ında ER (-) olguların % 87,23’ünde nekroz mevcut iken, ER(+) olguların %37,5’inde nekroz gözlenmi tir .ER negatifli i ile tumor nekrozu arasında istatiksel olarak belirgin anlamda ili ki elde edilmi tir (p<0,05). TÜMÖR NEKROZU 100 90 80 70 60 Tümör nekrozu var 50 Tümör nekrozu yok 40 30 20 10 0 ER pozitif ER negat,f Grafik 6: ER negatifli i ve tümör nekrozu ili kisi. 44 TABLO 13: ER NEGAT FL VE NODAL STATÜ ER NEGAT F ER POZ T F (kontrol grup) Nodal statü N:16 % N:39 % Ki-kare ²:4,3 pN0 4 %30,7 16 41,2 pN1 5 %38,4 10 25,6 pN2 3 %23.3 3 7,6 pN3 1 %7.6 10 25,6 P=0,230 ER (-)’li i ile nodal statü kar ıla tırıldı ında ER (-)’li i ile nodal statü arasında istatistiksel bir anlam elde edilememi tir. (P>0.05) ER NEGAT FL VE NODAL STATÜ 45 40 35 30 25 ER POZ T F ER NEGAT F 20 15 10 5 0 N0 N1 N2 N3 Grafik 7:ER negatifli i ve nodal statü. 45 TABLO 14:ER (-) GRUPTAK H STOLOJ K TÜMÖR T PLER VE D ER K N K PARAMETRELER Histolojik tumor tipi Olgu sayısı:47 NOS. nvaziv Duktal Karsinom ( DC) yüzde 37 %78,7 Metaplastik karsinom 3 %6.3 Mikst(müsinöz+ duktal ) karsinom 1 %2,12 Nöroendokrin diferansiasyon gösteren DC 1 %2,12 Myoepitel diferansiasyon gösteren DC 3 %6.3 Mikst (lobuler+müsinöz) karsinom 1 %2,12 Lobular karsinom. 2 %4.25 Hasta ya ı 27–79 (ortalama ya :52 ) Tumor çapı (cm) 2cm’den küçük 6 %12.7 2cm’den büyük 41 %87.3 Staga 0: (node negative) 16 % 33,2 Stage 1( 1–3 nodes positive) 10 % 25,6 Stage 2 ( 4 or more nodespositive) 3 % 7,6 Stage 3 (4 or more nodespositive) 10 %25,6 2 17 % 36 3 30 %64 Nodal statü Vasküler invazyon 17/47 ER(-) GRUPTAK H STOLOJ K TÜMÖR T PLER DC.NOS METAPLAST K CA Myoepitel dif.. gösteren DC. Nöröendokrin dif. gösteren DC LOBÜLER CA. M KST(Lobüler+ Duktal) M KST(Müsinöz+Duktal) Grafik 8:ER negatif olguların histoloik tümör tipleri. 46 %36.1 TABLO 15:ER (+) GRUPTAK H STOLOJ K TÜMÖR T PLER VE D ER K N K PARAMETRELER Histolojik tumor tipi Olgu sayısı:16 NOS. nvaziv Duktal Karsinom ( DC) yüzde (%) 13 %81,25 Mikst(lobüler + duktal ) karsinom 1 %6,25 Lobular karsinom 2 %12,25 Hasta ya ı 22–70 (ortalama ya : 53) Tumor çapı (cm) 2 cm’den küçük 4 %25 2 cm’den büyük 12 %75 Stage0: (node negatif) 4 %25 Stage 1( 1–3 nodes positif) 5 %31,25 Stage 2 ( 4 or more nodespositif) 3 %18,25 Stage 3 (4 or more nodespositif) 1 %6,25 Nodal statü Nükleer Grade 1 3 %18,25 2 11 %68,75 3 2 %12,25 Vasküler invazyon 2/16 %12,25 ER(+) GRUPTAK H STOLOJ K TÜMÖR T PLER DC.NOS LOBÜLER CA. M KST(lObüler+ Duktal) Grafik 9: ER pozitif olguların histoloik tümör tipleri. 47 TABLO 16: ER(-) ÇALI MA GRUBU HK BOYANMA SONUÇLARI Bp no ER PR her-2 ck5/6 ck14 Ck17 Ck18 sma calponin P63 Brca1 1229/03 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 1338/03 (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) 2390/03 (-) (-) (-) (+) (-) (+) (-) (++) (++) (+) (++) 2579/03 (-) (-) (-) (+) (+) (-) (+) (-) (-) (-) (++) 5069/03 (-) (-) (-) (+) (+) (-) (-) (-) (-) (-) (-) 8366/03 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 10513/03 (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (+) 12880/03 (-) (-) (-) (-) (-) (-) (++) (-) (-) (-) (++) 12169/03 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 1816/03 (-) (-) (-) (+) (-) (+) (+++) (-) (-) (-) (+) 5096/04 (-) (-) (-) (-) (-) (-) (++) (-) (-) (-) (-) 8703/05 (-) (-) (+++) (++) (++) (+) (++) (-) (-) (+) (-) 7244/04 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (++) 8608/04 (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) 10969/04 (-) (-) (+++) (-) (-) (+) (++) (-) (-) (-) (++) 10011/06 (-) (-) (-) (+) (+) (+) (+) (+) (+) (+) (++) 10478/04 (-) (-) (+++) (-) (-) (-) (+++) (-) (-) (-) (-) 11573/04 (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) 8444/06 (-) (-) (-) (+) (-) (+) (-) (-) (-) (-) (+) 5087/06 (-) (-) (-) (+) (+) (+) (-) (++) (++) (-) (++) 19270/06 (-) (-) (+++) (-) (-) (-) (-) (-) (-) (-) (-) 8436/06 (-) (-) (-) (-) (-) (-) (++) (++) (++) (+) (++) 6028/07 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (+) 20091/06 (-) (-) (-) (++) (+) (+) (-) (++) (++) (+) (-) 23062/06 (-) (-) (-) (-) (-) (-) (+++) (-) (-) (-) (++) 1020/07 (-) (-) (-) (+) (-) (-) (-) (++) (++) (+) (++) 19718/06 (-) (-) (-) (++) (++) (+) (-) (-) (-) (-) (++) 10792/ (-) (-) (-) (+) (+) (+) (-) (++) (++) (+) (+) 527/07 (-) (-) (-) (++) (++ (+) (+) (+) (+) (-) (-) 48 TABLO 16: ER(-) ÇALI MA GRUBU HK BOYANMA SONUÇLARI Bp no 1899/07 3956/07 4068/07 20046/06 18390/07 19339/07 20516/07 21481/07 26233/07 22144/07 7573/04 25942/07 14254/07 5937/07 27053/07 16773/07 22437/07 27720/07 ER PR her-2 Ck 5/6 Ck 14 Ck 17 Ck18 sma Calponin P63 Brca1 (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (+++) (+++) (-) (+++) (-) (-) (-) (-) (+++) (-) (-) (+++) (+++) (-) (-) (-) (-) (-) (-) (-) (-) (-) (+) (-) (-) (-) (-) (++) (+) (-) (-) (++) (++) (++) (+) (-) (-) (-) (++) (-) (-) (+) (+) (-) (-) (+) (+) (+) (+) (-) (++) (++) (-) (-) (-) (-) (-) (-) (+) (+) (-) (-) (-) (+) (-) (-) (+) (+) (+) (-) (-) (+++) (++) (+++) (-) (++) (++) (+) (++) (+++) (++) (-) (+++) (-) (++) (++) (-) (++) (+) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (++) (++) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (++) (++) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) (-) 49 (-) (++) (-) (-) (+) (++) (++) (-) (-) (-) (++) (-) (++) (++) (++) (++) (+) (-) TABLO 17: ER(+) KONTROL GRUBU HK BOYANMA SONUÇLARI Bp no ER PR her-2 Ck Ck Ck 5/6 14 17 Ck18 sma calponin P63 Brca1 8044/05 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 13051/07 (+++) (++) (-) (-) (-) (-) (+++) (-) (-) (-) (+) 2179/04 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 2169/03 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 530/07 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 12816/04 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 12405/04 (++) ++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 14620/05 (+++) (++) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 2373/07 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (++) 14634/06 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (++) 4480/07 (+++) (++) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 8072/04 (++) (++) (+++) (+) (+) (-) (++) (-) (-) (-) (++) 5554/04 (+++) (++) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 2817/03 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (++) 5978/03 (+++) (++) (-) (-) (-) (-) (+++) (-) (-) (-) (-) 11869/05 (++) (++) (-) (-) (-) (-) (++) (-) (-) (-) (-) 50 TABLO18: MMUNH STOK MYA SONUÇ ANAL Z ER NEGAT F GRUP ER POZ T F GRUP Antikor Negatif Pozitif % Negative Pozitif % CerbB-2 37 10 %21,2 15 1 6,25 SMA 37 10 %21,2 15 1 %0 P63 40 7 %14,9 16 0 %0 CALPON N 37 10 %21,2 16 0 %0 CK5/6 27 20 %42,4 16 1 %6,25 CK14 29 18 %38,3 16 1 %6,25 CK17 31 17 %36,2 16 1 %6,25 CK18 17 30 %63,6 0 16 %100 BRCA1 21 26 %55,3 11 5 %31,25 TABLO 19: HK BOYAMA SONUCU OLU AN GRUPLAR TÜMÖR T PLER ER(-) ER(+) n:47 % n:16 % Bazal benzeri 6 %12,76 O %0 Bazoluminal 10 %21,27 1 %6,25 Luminal 17 %36,17 15 %93,75 Myoepitelial 10 %21,27 0 %0 4 %8,5 0 %0 simlendirilemeyen Ki kare P=0,002 ER(-) olgularda olu an gruplar ER(+) olgulardaki gruplarla kar ıla tırıldı ında ER(-) tümörlerde bazal benzeri, bazaluminal ve myoepitelial gruplar ER pozitiflere göre belirgin anlamda daha yüksek saptanmı tır. (p<0,05). 51 100 90 80 70 60 ER pozitif 50 ER negatif 40 30 20 10 f le nd ir i He r-2 po zit i le m ey en Lu m in al yo ep it e lia l sim M Ba za l Ba za l um be nz er i in al 0 Grafik 10: ER (-) tümörlerde HK boyanma sonucuna göre olu an subgruplar. TABLO 20: ER NEGAT F TÜMÖR SUBGRUPLARININ LT HAB STROMAL YANITI LT HAB HAF F ORTA BEL RG N STROMAL YANIT % N % N % Bazal benzeri(6) 1 %16,6 1 %16,65 4 66,65 Bazaluminal(10) 3 %30 2 %20 5 %50 Luminal(17) 11 %65 4 %23,5 2 11,5 Myoepitelial(10) 2 %20 3 %30 5 %50 2 %50 2 %50 0 %0 simlendirilemeyen(4) 52 TABLO 21: ER NEGAT F TÜMÖR SUBGRUPLARININ NF LTRASYON PATERN NF LTRAN EKSPANS L TÜMÖR SUBGRUPLARI N:47 % N:47 % Bazal benzeri(6) 3 %50 3 %50 Bazaluminal(10) 5 %50 5 %50 Luminal(17) 17 %100 0 %0 Myoepitelial(10) 5 %50 5 %50 4 %100 0 %0 simlendirilemeyen(4) BRCA1 EKSPRESYON ORANLARI 80 70 60 50 40 BRCA1 EKSPRESYONU VAR BRCA1 EKSPRESYONU YOK 30 20 10 0 ER POZ T F ER NEGAT F Grafik 11:ER negatifli i ve BRCA1 ili kisi. TABLO 22: ER(-) NEGAT FL LE BRCA1 EKSPRESYON KAYBI BRCA1 BRCA1 EKSPRESYONU VAR EKSPRESYONU YOK Östrojen N % Negatif 26 Pozitif 5 ER(-)’li i ile N % N %55,31 21 %44,6 47 %31,25 11 68,75 16 BRCA1 ekspresyon oranı %55,31’inde, ER(+) olgularında %31,25’inde % kar ıla tırıldı ında ²:1,88i P=0,169 ER(-) olguların BRCA1 ekspresyonu izlendi. ER(-) tümörlerde brca1 ekspresyon kaybı %44 olup ER negatifli i ile ile BRCA1 ekspresyonu kaybı arasında istatistiksel bir anlam elde edilememi tir. (p>0,05). 53 ERnegatifli i ve bazal fenotip ili kisi 100 90 80 70 60 Bazal fenotip var 50 Bazal fenotip yok 40 30 20 10 0 ER pozitif ER negatif Grafik 12: ER negatifli i ve bazal fenotip. TABLO 23:ER NEGAT F TÜMÖRLERDE BAZAL FENOT P L K S Bazal fenotip Var Yok Östrojen N:63 % N:63 Negatif:n:47 26 %55,31 21 Pozitif:n:16 1 6,25 % Ki-kare P: 11,74 0,0006 ** %44,69 15 93,75 ER negatifli i ile bazal fenotip izlenme oranı kar ıla tırıldı ında ER negatif olguların %55,31’inde, ER pozitif olguların da %6,25’inde negatifli i ile bazal fenotip varlı ı arasında bazal fenotip izlendi. ER istatistiksel bir anlam elde edilmi tir. (p<0,05). (Not:bazal fenotip olarak:bazal benzeri+bazaluminal+myopitelial grup birlikte de erlendirilmi tir). TABLO 24:ER NEGAT FlL VE M YOEP TEL D FERANS ASYON L K S Var Östrojen N Yok % N % N % Ki-kare P:0,106 ²:2,61 Negatif 10 % 21,3 37 %78,7 47 Kontrol grubu(er pozif 0 %0 16 %100 16 grup) ER(-)’li i ve miyoepitelial diferansiasyon ili kisi kar ıla tırıldı ında ER(-)’li i ile miyoepitelial diferansiasyon arasında istatistiksel bir anlam elde edilememi tir. (p>0,05). 54 TABLO25: TR PLE NEGAT FL K VE BAZAL FENOT P L K S Bazal fenotip Triple Var Yok N % N % ²: negatif 22 %59,4 15 %40,6 neg 4 %40 6 %60 P= grupn:37 Triple 0,229 olmayan n:10 Triple negatiflik ve bazal fenotip ili kisi kar ıla tırıldı ında triple negatif olguların %59.4’ünde bazal fenotip izlendi. Triple negatif olmayan olgularında %40’ında bazal fenotip izlendi. Triple negatiflik ile bazal fenotip arasında istatistiksel bir anlam elde edilememi tir. (p>0,05). ²:26,88 p: 0,008 TABLO 26:ER(-) TÜMÖR SUBGRUPLARININ NODAL STATÜSÜ TÜMÖR Pno GRUPLARI Pn1 pN2 pN3 Bazal benzeri(6) 2 %33,3 3 %50 0 %0 1 %16,6 Bazaluminal(9) 3 %33,3 5 %55,5 0 %0 1 %11,1 Luminal(14) 3 %21,4 0 %0 3 %21,4 8 %57,1 Myoepitelial(8) 6 %75 2 %25 0 %0 0 %0 2 %66,6 0 %0 O %0 1 %33,3 simlendirilemeyen(3) ER negative gruplar ve nodal statü ²:26,88 p: 0,008 ili kisi kar ıla tırıldı ında bazal benzeri, bazaluminal ve myoepitelal grupların nodal statü olarak N0 ve N1 düzeyinde kaldı ı izlenmi tir. Bazal fenotip ve nodal statü arasında istatistiksel edilebilmi tir.(p<0.05). 55 bir anlam elde TABLO 27: ER (-) TÜMÖR SUBGRUPLARININ NÜKLEER GRADE ORANLARI NÜKLEER GRADE NG1 N NG2 NG3 % N % N % Bazal benzeri 0 %0 2 %33,5 4 %66,5 Bazaluminal 0 %0 4 %40 6 %60 Luminal 0 %0 10 %58,8 7 %41,2 Myoepitelial 0 %0 0 %0 10 %100 0 %0 2 %50 2 %50 simlendirilemeyen ²:9,54 P=0,04 ER negatif gruplar ve nükleer grade ili kisi kar ıla tırıldı ında bazal benzeri, bazaluminal ve myoepitelial subgruplarında yüksek nükleer grade izlenmi ve istatiksel olarakta anlamlı bulunmu tur.(p<0.05). TABLO 28: ER (-) TÜMÖR SUBGRUPLARININ BRCA1 EKSPRESYON ORANLARI BRCA1 Pozitif BRC A1 negatif N % N % Bazal benzeri(6) 5 %83,3 1 %16,7 Bazaluminal 8 %80 2 %20 Myoepitelial 6 %60 4 %40 Luminal 6 %35,3 11 %64,7 1 %25 3 %75 E(-)TÜMÖR GRUPLARI simendirilemeyen ER negatif tumor gruplarında BRCA1 ekspresyon oranlarına bakıldı ve en yüksek Ekspresyon kaybı myoepitelial ve luminal fenotipte izlendi. 56 90 80 70 60 50 brca1 poziitif 40 brca1 negatif 30 20 10 ey en in al le nd i ril em lu m isi m m yo ep it e li a l in al ba za lu m ba za lb en ze ri 0 Grafik 13:ER(-) tümör grupları ve BRCA1 ekspresyon oranları. TABLO 29:BAZAL FENOT P VE BRCA1 EKSPRESYONU BRCA1 POZ T F BRCA1 NEGAT F % E(-)TÜMÖR % ²: P= 7,42 0,006** GRUPLARI n:47 Bazal fenotip(bazal 19 %83,3 7 %16,7 7 %35,3 14 %64,7 benzeri+bazaluminal+myo epitelial) N:26 Luminal fenotip ve isimlendirilemeyen N:21 ER negative tumor gruplarında bazal fenotip( bazal benzeri+bazaluminal+luminal) ile BRCA1 ekspresyon kaybı kar ıla tırılmı ve bazal fenotip te %16 , di er grupta(luminal ve isimlendirilemeyen) ise %64 ekspresyon kaybı izlenmi tir. 57 5) TARTI MA Meme kanseri, kadınlarda en sık görülen kanser olup, tanı ve tedavi yöntemleri alanındaki tüm geli melere ra men ölüm nedenleri arasında akci er karsinomundan sonra 2. sırada yer alır (11). Morfolojik, klinik, hormon reseptör düzeyi, tedaviye yanıtlarına göre farklı özellikleri olan, heterojenöz gruplara sahip tümörlerdir (9). Cerrahi tedaviden sonra dü ük ve yüksek riskli grupları belirlemek için kullanılan ve prognostik açıdan de erli olan; histolojik tip, histolojik grade, hormon reseptörü varlı ı, HER-2 amplifikasyonu, tümör boyutu, proliferasyon indeksi, nekroz, anjiolenfatik invazyon, meme ba ı tutulumu, intraduktal tümöral komponent varlı ı ve aksiller lenf bezi tutulumu gibi pek çok parametre vardır (11,15). Ancak aynı kategoriye sokulan tümör gruplarının klinik olarak çok farklı seyretmesi bazı parametrelerinde ilave edilmesi gerekti ini akla getirmektedir (9). Günümüzde bu tümörlere yapılan medikal tedavilerde önemlidir. ER (+) meme karsinomlarında ER düzeyi oldukça antiöströjen tedavisi (Tamoxifene ve Raloxifene) yıllardır kullanılan primer medikal tedavi yöntemidir.Yakla ık meme karsinomlarının % 60-65’i ER (+) dir (6). Histolojik olarak iyi diferansiye tümörler genelde ER (+) olup bu tümörlerin büyük bir kısmı iyi prognoza sahiptirler(6). Buna kar ılık meme karsinomlarının %20’si ER negatiftir ve bu grup tümörler daha kötü prognozlu, genelde yüksek histolojik grade’ye sahip tümörlerdir. Teorik olarak bu negatifli in sebebi 2 ekilde açıklanmaktadır. 58 Teorilerden biri; tümör hücrelerindeki ER ekspresyonunun downregülasyonu, di eride tümör hücrelerinin normalde hiç ER ekspresse etmeyen hücrelere diferansiasyonudur (44). Bilindi i üzere normalde memede duktus ve asinüslerde, bazal tabakada bulunan myoepitelial hücrelerde ER ekspresse etmezler ( 44). Bazı kaynaklarda ER (-)’ li ini tümör hücrelerinin myoepitelial diferansiasyonu ile ili kilendirmektedir (44). Putti.T.C ve arkada ları 291 ER (-) meme karsinomu olgusunu morfolojik ve immunhistokimyasal olarak incelemi ler. Olguların büyük bir ço unlu unu (%85) invaziv duktal karsinom, ikinci sıklıkta ise (%8) atipik medüller karsinom olu turmu . Sık görülen morfolojik parametreler; yüksek histolojik grade, komedo nekroz, lenfoid stroma, santral nekroz ve fibroz olup; pushing marjin aksiller lenf nodu negatifli i ile korelasyon gösteriyormu . HK olarak tümör hücrelerinde prognostik marker olarak bilinen; p53 ve HER-2, ekspresyonları yüksek bulunmu . HK çalı maları sonucunda : p53 ie %60, HER-2 ile %32, BRCA1 ile %68, CK5/6 ile %45, CK18 ile %69, SMAile %26 oranında pozitif boyanma saptanmı . Ck5/6 ile basal fenotip, Ck 18 ile luminal fenotip, SMA ile myoepitelial fenotip incelenmi . Bazal CK luminal CK ekspresyonu kar ıla tırılmı ve gösteren ekspresyonu gösteren ER(-) tümörler ile ER(-) bazal fenotip arttıkça tümörlerin prognostik parametreleri kötü prognoz gözlenmi tir. Ayrıca ER(-) tümörlerde herediter meme kanserinde rol oynayan BRCA1 gen mutasyonuda anlamlı olarak yüksek bulunmu tur. BRCA1 ekspresyon kaybı %32 olup genelde grade3 morfolojidekilerde saptanmı . ER(-) meme kanserleri morfolojik, fenotipik ve genotipik farklı bir antitedir sonucuna varılmı tır (6). Bizim çalı mamızda ise; 47 ER(-) meme kanseri olgusunun büyük ço unlu unu (%78,7) NOS invaziv duktal karsinom, ikinci sıklıkta (%6,7) metaplastik karsinom ve myoepitelial diferansiasyon gösteren invaziv duktal karsinom olu turmaktaydı. HK çalı maları sonucu: CerbB-2: %21.2, CK5/6: %42.4, CK18:%63,6, SMA:%21. BRCA1 ekspresyon kaybı %44.7 bulundu (Tablo:18). HK sonuçları literatürlerle uyumlu bulundu. Histolojik tanı olarak metaplastik karsinom ve myoepitelial diferansiasyon gösteren karsinom olguları HK analizine göre en çok bazal fenotip gösteren gruplardı. Rutin çalı ma esnasında bu tanılara sahip karsinomlarda bazal fenotip açısından daha ayrıntılı inceleyip bazal CK ekspresyonlarına bakılması gerekti i kanısına varıldı. 59 Rakha ve Putti; Bazal benzeri ve myoepitelial fenotip gösteren meme karsinomlarını klinik ve morfolojik olarak kıyaslamı lardır. Bazal benzeri karsinomlar tüm meme karsinomları içinde % 18,6 oranda bulunmu . Bazal benzeri 2 grupta incelenmi . Dominant bazal patern (> %50 bazal CK ekspresyonu). Ve bazal karakteristik (%10-50 bazal CK ekspresyonu). Myoepitel fenotip içinde SMA, p63, calponin ekspresyonu de erlendirilmi . Bazalfenotipte: grade 3 morfoloji, büyük tümör çapı, hormonreseptör negatifli i, luminal keratin negatifli i, p53, EGFR, Pcadherin pozitifli i, BRCA1 ekspresyon kaybı gözlenmi .. .NPI(Nothingam Prognostik ndeks) kötü, bununla ili kili olarakda uzak metastaz ve rekürrensi yüksek olup, komedo nekroz, lenf nodu negatili i, il kili bulunmu . Hasta ya ı, vaskuler invazyon, GCDFP ve HER-2 pozitifli i ile ili ki saptanmamı . Hastalıksız sa kalım ve tümörlü sa kalım kısa izlenmi . Sonuç olarak; bazal fenotipli meme karsinomlar ba ımsız survey belirleyicisidir denilmi (27). Bizim çalı mamızdada bazal benzeri olarak isimlendirdi imiz grupta grade3 morfoloji (resim5 ), belirgin iltihabi stromal yanıt( resim2 ), itici invazyon sınırı (resim 1 ), büyük tümör çapı, bazal CK pozitifli i, anlamlı bulunmu tur . BRCA1 kaybı, hasta ya ı ve anjiolenfatik invazyon ili kisi saptanmamı tır (Tablo21,27,28,29). Myoepitel fenotipte ise: genç ya , grade3 tümör, kötü NPI, hormon reseptör negatifli i, luminal CK negatif; p53, EGFR, P-cadherin, E-cadherin, pozitif bulunmu . Tm çapı, lenf nodu tutulumu, vasküler invazyon, HER-2, GCDFP ve nöroendokrin marker pozitifli i ile korelasyon saptanmamı . En sık görülen histolojik tip NOS invaziv duktal karsinom olup, tubuler mikst, medüller karsinom da sık görülen histolojik tiplermi . Ayrıca i si, berrak, bazaloid hücreli de i ikliklerde saptanmı . Tümörlü sa kalım kısa izlenmi , hastalıksız sa kalım survey belirleyicisi olarak kabul edilmemi . Sonuç olarak bazal fenotipin prognoz açısından myoepitel fenotipten daha kötü oldu u, herediter BRCA1 mutasyonunun daha sık gözlendi i, fenotip olarak benzer özellikler olsada iki grup arasında farklı özeliklerin oldu u belirtilmi tir (27). Bizim çalı mamızdaki myoepitel fenotip gösteren 10 olgu saptandı (%21.27). Olgular garde3, luminal CK ekspresyonu dü ük, nodal statü olarak büyük bir kısmı NO olan, ekspansil büyüme paternine sahip tümörlerdi.(tablo:26,27).Tümör çapı , anjiovasküler invazyon ile korelasyon saptanmadı. Ensık görülen histolojik tip, NOS invaziv duktal karsinom olup, ikinci sıklıkta myoepitelial diferansiasyon gösteren invaziv duktal karsinom saptandı.. si, bazaloid, berrak hücreli de i iklikler (resim4) bu grupta daha sık izlendi. HER-2 pozitifli i saptanmadı. 60 Kesse-Adu.R ve arkada larınının yaptı ı bir çalı mada; 117 Meme karsinomlu (77 ER pozitif,47 ER negatif ) olguda myoepitel diferansiasyonu ara tırılmı . Sonuç olarak ER (-) tümör grubunda %29, ER (+) tümör grubunda ise %2.5 myoepitelial diferansiasyon saptanmı (44). Bizim çalı mamızda ise 47 ER(-) olgunun 10'unda (%21,27) myoepitelial diferansiasyon izlendi. 16 ER(+) olguda hiç miyoepitelial diferansiasyon saptanmadı. statiksel olarak (p:0.106>0.05 ) ER negatifli i ile miyoepitelial diferansiasyon ili kisi anlamlı bulunmadı (Tablo:24). Son yıllarda meme karsinomlarında HER-2 overexpresyonu düzeyide dikkate alınmakta ekspresyon düzeyine göre Trastuzumab (Herceptin) tedavisi prosedüre eklenmektedir. HER-2 gen amplifikasyonu veya overekspresyonu meme karsinomlarının %15-25’inde izlenmektedir (26).Ancak ER (-) olan antiöstrojen tedaviden faydalanamayan tümör grubu HER-2 overekspresyonu da gösteremeyebilir. Bu grup tümörler Tamoksifen ve veya Herceptin tedavisinden faydalanamamaktadır, çünkü tümörler tarafından bu proteinler ekspresse edilmememektedir (10). Bu gruba bazı kaynaklarda triple negatif meme karsinomları denmektedir (5). Rakha.A.E ve arkada ları 1986-1998 yılları arasında tanı alan 1994 invaziv meme karsinomu olgusunda %16.3’ünde triple negatif fenotipli ( ER(-), PGR(-), HER.2(-) ) tümör grubunun morfolojik ve kilnik özelliklerini incelemi ler. IHK olarak: ER, PR, HER-2, AR, EGFR, P.cadherin, E.cadherin, CK5/6, CK14, p53 çalı mı lar. Tümörlerin ço u invaziv duktal karsinom (NOS), büyük çaplı, ekspansil büyüme paterni gösteren, prognostik indeksi kötü, rekürrens ve uzak metastaz oranı yüksek , hastalıksız sa kalım ve tüm sa kalım açsından kötü klinik gidi li tümörlermi . Bu tümörlerde: AR(-), E.cadherin(-), bazal CK(+), p.cadherin (+), p.53(+), EGFR(+) saptanmı . Sonuç olarak lenf nodları negatif olan tümör gruplarında bazal fenotip tek prognostik markerdir denilmi tir. Triple(-) karsinomlarda bazal CK oranı: %55,7 bulunmu ; meme kanserleri biolojik davranı ve tedaviye yanıt açısından heterojen bir hastalık grubudur denmi (5). Bizim çalı ma grubumuzda toplam 47 ER(-) meme karsinomu olgusunun 37'si triple negatifti.(%78,7) Tümörlerin ço u invaziv duktal karsinom olup ikinci sıklıkta metaplastik karsinom ve myoepitelial diferansiasyon gösteren invaziv duktal karsinom yer alıyordu. Triple negatif olgulardaki bazal CK ekspresyon oranlarına bakıldı. Sonuç olarak bazal CK pozitifli i %59.4 bulundu. Bazal CK ekspresyonu literatürde bahsedildi i oranda saptandı ancak kontrol grubunda %40 bazal CK pozitifli i saptandı ı için istatiksel olarakta triple negatiflikle bazal CK pozitifli i anlamlı bulunmadı (Tablo:25). 61 1987’de Dairkee ve ark memede bazal CK(+) karsinomların daha erken rekürrens yaptı ını ve prognostik öneme sahip olabilece ini belirttiler (35). 1990 da Domagala ve arkada ları Vimentin ekpresse eden, lenf nodu negatif olan, fakat 5 yıl içinde kötü gidi gösteren bir grup tümör tanımladılar. Bunlar aynı zamanda geni santral nekrozlu, yüksek gradeli, mitozu yüksek, ER(-) tümörlerdi. Bizim çalı mamızdada tümör gruplarındaki nodal statü de erlendirildi ve bazal fenotip gösteren grupta N0 yüksek saptandı.Ayrıca bazal fenotipli tümör grubu yüksek nükleer grade(resim4 ) ve geni santral nekroz ve komedo nekroz (resim3 ) varlı ı di er gruplara oranla belirgin anlamda yüksekti. Santini ve arkada larıda yine benzer morfolojik özellikte ve EGFR(+), CK14/17(+), SMA(+) tümörler tanımladılar.(36) 1998’de Malzahn ve arkada ları CK5/6-14-17 vimentin(+), grade3 ve ER(-) tümörler içinde pozitifli i gösteren küçük bir alt grubun tümörlü sa kalım ve hastalıksız sa kalım açısından kısa surveye sahip olabilece ini ileri sürdüler (37). Günümüzde klasik olarak hastaya adjuvan kemoterapi, radyoterapi ya da hormonal terapi verilip verimeyece ini gösteren bazı faktörler belirlenmi tir. Bunlar; ya , tümör çapı, grade, lenf nodu ve hormon reseptör durumu vb. Bazal fenotip gösteren hastalar genelde klinisyen için adjuvan tedavi açısından karar vermesi zor olan gruplar olmu tur. Tanı olarak net bir konsensus olu madı ı gibi tedavi protokolleri de henüz belirli de ildir. Fakat LN(-) 10 hastadan 2-3 ü adjuvan tedavi verilmesine bakmaksızın exitus, 7’si adjuvan tedavi. verilmese de ya amakta ve sonuçta yalnız 1 hastada adjuvan kemoterapi ile kanser ile ili kili ölümün gerçekten önlenebildi i anla ılmaktadır. Özet olarak, klinikopatolojik özellikleri benzer gibi gözükse de farklı davranı ların temeli meme kanserlerindeki farklı genetik özelliklerde yatmaktadır. Son 10 yılda moleküler çalı maların geli mesi ile binlerce genin e zamanlı olarak çalı ılması imkanı do mu tur. Tümör dokusu örneklerinden gen ekspresyon profili (GEP) çıkarılarak tümörlerde yeni moleküler klasifikasyonu getirmi tir (40). Nielsen ve Hsu 300 meme karsinomunun Gen ekspresyon profilini çıkardılar. %19 bazal benzeri fenotip saptandı. Bazal benzeri olan gruba HK olarak CK5/6, EGFR, c.kit, ER ve CerbB-2 çalı ıldı. Sonuç olarak: CK5/6 : % 62, EGFR: %57, c.kit: %29, ER (-) ve ERB.B2 (-) ekspresyon göstermi ler. Bazal fenotip için HK paneli: Sensitivite % 76 Spesifite %100 bulundu. Bazal benzeri meme kanserleri için tam anlamı ile güvenilir IHK belirleyiciler ya da IHK seti yoktur ancak az sayıda dar bir HK paneli kullanılırsa bir kısım bazal benzeri meme kanserleri gözden kaçabilir denildi. En azından duktal tip 62 morfolojideki karsinomlar için CK5/6 ( +), EGFR(+), ER(-), HER2(-)/dü ük olma durumu BLBC(basal like breast cancer) için oldukça diagnostik olabilece i belirtildi. Tedavisi güç olan BLBC grubunun EGFR ve c.kit ekspresyonunun anlamlı olması yeni medikal tedavi ajanlarına olanak sa layabilece i belirtildi (40). Sorlie T ve Perau CM sporadik meme karsinomları ile herediter BRCA1 gen mutasyonu ili kili meme karsinomlarında Gen Ekspresyon analizi çalı mı lar. Herediter BRCA1 mutasyonuna ba lı olan meme karsinomu gruplarında bazal fenotipin anlamlı olarak yüksek oldu u gözlenmi (35). Bizim çalı mamızda ise bazal fenotip gösteren grupta BRCA1 ekspresyonu %83, olup (resim11 ) literatürlerde bahsedildi i gibi bazal fenotipteki ekspresyon kaybı yüksek bulunmadı aksine luminalfenotipte ekspresyon kaybı daha yüksek saptandı. Foulkes ise BRCA1 gen mutasyonu ile ili kili meme karsinomlarında bazal CK ekspresyonunu yüksek oldu unu gözlemlemi çalı ması sonucunda ‘BRCA1 stem cell regülatörüdür ’ hipotezini öne sürmü ( 41). Kusinska ve Potemski ER(-) meme karsinomlarında GEP çalı ması yapmı sonuç olarak ER (-) meme Ca’lar 3 subgruba ayrılmı . Basal benzeri, HER-2 (+), Normal meme benzeri subtip. HER-2 subtip: HER-2 amplifikasyon genleri (17q22-24’te amplifikasyon ); grb7 gen ekspresyonu gösterir. Normal meme benzeri: Adipöz doku ve non-epitelial di er hücrelerden salınan genleri(+) ve bazal epitel genleri kuvvetle eksprese olur. Luminal epitel genleri zayıftır. Bazal benzeri subtip: CK5/6, CK 14/17, laminin ve ya asidi ba layan proteinler (+) 195 olguluk Meme karsinomu serisinde IHK olarak CK5/6, ER ,PR, CK17, HER-.2 çalı ılmı . HER-2(+) subtip ve basal benzeri subtip gösteren hasta gruplarında tümöral sa kam ve hastalıksız sa kalım sürelerinin kısa oldu u gözlenmi . HK çalı ma sonucunda, CK 5/6 %36.9, CK17 %21 olguda (+) bulunmu (43). Bizim çalı mamızda CK5/6 %42.4, CK17 %36,2 (+) bulundu (resim13 ,14 ). Matos ve Dufloth Gen Ekspresyon profiline göre meme karsinomlarını 5 grupta topladılar.. 1:Bazal benzeri. 3:Luminal(A). 2:HER-2 (+) 4:Luminal(B). 5:Normal meme dokusu benzeri. GEP çalı ması sonunda TMA (Doku mikroarray ) tekni i kullanarak 168 invaziv meme karsinomu olgusuna subtiplerin karakterini belirlemek üzere HK olarak 7 moleküler marker çalı ılmı : ER, HER-2, Pcadherin, p63, CK5/6, Ki 67, Bcl2 (tablo 30) (45). 63 TABLO 30: GEP SONUCU OLU AN GRUPLARIN HK PANEL SUB T P ER HER-2 P-cad.ve veya p63 Ekspresyon ve/veya CK5/6 Yüzdesi% Luminal A Pozitif Negatif Pozitif/negative 89(56.3) Luminal B Pozitif Pozitif Pozitif/ negative 26(16.5) Bazal Negatif Negatif Pozitif 12(7.6) Her-2 overekspr. Negatif Pozitif Pozitif/ negative 28(17.7) Negative Negatif Negatif Negatif 3(1.9) Livas ve arkada larıda GEP ile BLBC olarak belirlenen 18 meme karsinomunda CK8/18 % 83, EGFR % 72, CK 5/6 % 61, ER: % 0, izlenmi . Kullanılan HER-2: % 0 pozitif boyanma HK panelinin bazal fenotipi belirlemede sensitivitesi %55 , spesifitesi %100’dür ve genetik olarak BLBC oldu u gösterilen meme karsinomlarında IHK panel olarak yalnız CK5/6 kullanılması %39 oranda underdiagnoza yol açıyor denildi (40). Bizim çalı mamızdada bazı olgular sadece CK5/6 ile pozitif boyanırken (resim13 ). bazı olgularda sadece CK14 veya CK17 ile (resim 12 , 14) pozitif boyanma gözlenmi tir. Bu nedenle bazal CK ekspresyon analizi için tek marker çalı manın yetersiz tanıya neden olabilece i kanısına varıldı. Reis-Filho .J ve Simpson.T.P meme karsinomlarının CHG (Comparative genomic hybridization) analizi sonucunda tümörün grade’sine göre farklı genetik de i iklikler gözlemlemi ler. Örne in: Grade1,iyi diferansiye karsinomlarda sıklıkla 1q ve 16q kaybı, grade2 ve grade3 karsinomlarda 8q,17q ve 20q kaybı gözlemlemi ler . Sonuç olarak farklı biolojik davranı ların temeli farklı genetik de i iklerde yatmaktadır denilmi moleküler çalı malar morfoloji esaslı çalı maların yerini almaya ba lamı tır (46,48). 64 6) RES MLER Resim 1: ER negatif tümörlerde itici invazyon sınırı (pushing border). Resim 2: ER negatif tümörlerde itici invazyon sınırı ve belirgin peritümöral iltihabi stromal yanıt. 65 Resim 3: ER negatif tümörlerde yaygın komedo nekroz varlı ı. Resim 4:ER negatif tümörlerde berrak hücreli de i iklikler. 66 Resim 5: ER negatif tümörlerde multinükleer tümöral dev hücreler. Resim 6: ER ile negatif boyanan histolojik grade’si yüksek tümör hücreleri. 67 Resim 7: ER ile pozitif boyanan tümör hücreleri. Resim 8: ER negatif tümörlerde CerbB-2 ile kuvvetli membranöz boyanma. 68 Resim 9: ER negatif tümörlerde SMA pozitifli i Resim 10: ER negatif tümörlerde Calponin pozitifli i 69 Resim 11: : ER negatif tümörlerde BRCA1 pozitifli i Resim 12. ER negatif tümörlerde CK14 pozitifli i 70 Resim 13: ER negatif tümörlerde CK5/6 pozitifli i. Resim 14: ER negatif tümörlerde CK17 pozitifli i. 71 Resim 15: ER pozitif tümörerde CK18 pozitifli i. 72 7) SONUÇLAR • Meme kadınlarda en sık görülen ancak; biolojik davranı olarak geni bir yelpazede da ılan; heterojenöz bir hastalık grubudur. • Son 10 yılda moleküler çalı maların geli mesi ile binlerce genin e zamanlı olarak çalı ılması imkanı do mu , Tümör dokusu örneklerinden gen ekspresyon profili (GEP) çıkarılarak meme kanserlerinde yeni moleküler klasifikasyonu getirmi tir. • Yeni moleküler klasifikasyona göre meme kanserleri 5 grupta toplanmı tır. Luminal A , Luminal B, HER2(+), Bazal benzeri ve Normal meme benzeri. Bazal benzeri ve HER-2 (+) grup klinik olarak kötü prognoza sahiptir. • Bazal benzeri grup; ER(-), Her-2(-) ekspresyonu dü ük, EGFR, ckit, bazal sitokeratin(CK5/6,CK14,CK17) ekspresyonu yüksek, kötü prognoz, genç ya , BRCA1 gen mutasyonu ile ili kili tümörlerdir. • ncelenen bazal benzeri tümörlerin morfolojik olarak genelde grade 3, Duktal/NOS veya metaplastik, co rafik nekrozu sık, pushing margin ve stromal lenfositik cevabı yüksek oldu u gözlenmi tir. • Bu çalı mada; triple negatif / bazal benzeri karsinom sıklı ının daha fazla olma olasılı ından hareketle ER (-) meme karsinomları çalı ma grubu olarak seçildi. 47 ER(-) invaziv meme karsinomu vakasında; ortak morfolojik prognostik parametreler, HER2 (+)grup ve bazal benzeri grup oranı, triple negatif tümörlerdeki bazal benzeri grubun oranı, benzeri bu iki subgrup arasındaki meme karsinomunun tanısında panel de erlendirilmi tir. 73 farklılıklar ve bazal kullanılabilecek immunhistokimyasal • Çalı ma grubumuzu olu turan ER(-) belirgin lenfoid stroma, meme karsinomlarında; yüksek grade, santral fibroz/nekroz, pushin margin gibi morfolojik bulgular daha sık izlendi , buna ilaveten skuamoid, berrak hücreli ve i si hücreli de i ikliklerde saptandı.. • Uygun bloklara HK olarak: ER, PR, HER-2, SMA, Calponin, p63, CK5/6, CK14, CK17, CK18, BRCA1 antikorları belirlemek için; çalı ıldı.. Miyoepitelyal diferansiasyonu Calponin , SMA, P63 ,Luminal diferansiasyon için; CK18, Bazaloid diferansiasyon için; CK5/6, CK14, CK17 kullanıldı.. • HK boyamalar sonucunda 47 ER(-) olgunun 37'si triple negatif (%78,7), 10’u HER-2 pozitifti (%21.2 ). ER(-) çalı ma grubunda toplam 26 olguda (%55.31), ER pozitif olguların da %6,25’inde bazal fenotip izlendi. Triple negative gruptaki bazal fenotip oranıda %59.4 bulundu.Literatürlerde bahsedildi i gibi bazal fenotip ER negatiflerde ve triple negatiflerde anlamlı olarak yüksek saptanmı tır. • Yapılan çalı malarda ER(-) tümörlerde herediter meme kanserinde rol oynayan BRCA1 gen mutasyonuda mmunhistokimyasal anlamlı olarak yüksek bulunmu tur. Bu mutasyon olarak BRCA1 ekspresyon kaybı ile paralellik göstermektedir. Bizim çalı mamızda ER(-) grupta BRCA1 ekspresyon kaybı %44 saptanmı tır. Sonuç literatür bilgileri ile uyumlu bulunmu tur. Ancak bazal fenotip ile BRCA1 ekspresyon kaybı arasında korelasyon izlenmemi tir. Luminal fenotipte BRCA1 ekspresyon kaybı daha yüksek saptanmı tır. • CK5/6, ER, HER-2, EGFR kombinasyonu Basal- benzeri meme karsinomlarını belirlemek için iyi bir kombinasyondur; ancak bazal sitokeratin olarak tek immunhistokimyasal marker kullanmak yetersiz tanıya neden olabilir. Bu nedenle bazal CK olarak CK5/6, CK14, CK17 birlikte kullanılırsa BLBC yakalama ansı daha yüksektir. • Sonuç olarak yeni fonksiyonel sınıflamaya göre bazal fenotip gösteren meme karsinomları hormon reseptörleri negatif, HER-2 overekspresyonu göstermeyen, yüksek grade’li, kötü prognozlu, tanı ve tedavi olarak net bir konsept olu mamı , ancak son zamanlardaki GEP çalı maları ile çok sık bahsedilen tümor grubu olmu tur. 74 8) KAYNAKLAR 1. Parkin DM, Bray F, Ferlay J, Pisani P. Estimating the world cancer burden: Globocan 2000. Int J Cancer. 2001; 94: 153-156. 2. Burget R, Tuncer , Bozdemi N. Türkiye’de kanser sıkılı ı. Çukurova Üniversitesi Tıp Fakültesi Dergisi.1994; 38-39. 3. Gusterson A.B,Ross T.D, Heath J.V,Stein T.Basal cytokeratins and their relationship to the cellular origin and functional classification of breast cancer.Breast cancer reseach 2005,7:143-148. 4. Rosai J. Ackerman’s Surgical Pathology, 8th ed. Vol II St. Louis, Mosby, 1996;565-1660 5. Rakha A.E, El Sayed E.A, Green R.A, Lee H.S.A .et al.Prognostic markers in Triple –Negative Breast Cancers.Cancer.January, 2007.Vol.109/number1. 6. Putti TC, Abd El-Rehim DM,A Rakha E et al. Etsrogen receptor- negative breast carcinomas :a review of morphology and immunophenotypical analysis.Modern pathology (2005) 18,26-35. 7. Gudjonsson T, Adriance C.M, Sternlicht M.D et al. Myoepithelial cells : Their origin and Function in Breast Morphogenesis and Neoplasia. Journal of Mammary gland biology and neoplasia, Vol.10, No.3, July 2005. 8. Hanneman J, Lee H.S, et al.Br J Cancer. 2006. Nov 20; 95(10). 1334-41 9. Fulford LG, Easton DF, Reis- Filho JS, et al. Specific morphological features predictive for the basal phenotype in grade 3 invasive ductal carcinoma of breast. Histopathology 2006, 49, 22-34. 75 10. Filho S.J, Path MRC.Basal like breast cancers: From pathology to mouse models and beyond. Breast Cancer Research Centre, London, UK 11. Kumar V, Cotran RS, Stanley L. Basic Pathology. 7th ed. Philadelphia,WB Saunders Company, 2003; 191-192. 12. Grassadonia A, Tinari N, Iurishi I, Piccola E, Cumassi A. Glyconj J. 2004; 19:551556. 13. Stenberg SS. Histology for Pathologists, New York, Raven Pres, 1992; 71-82. 14. Ünal H, Ünal G. Meme Hastalıkları, stanbul, Nobel Tıp Kitabevi Ltd ti, 2001. 15. Tavasolli FA. Pathology of the Breast. 2nd edition. Connecticut, Appelton and Lange, 1999 16. Tavasolli FA, Devilee P. World Health Organition Classification of Tumours. Pathology and Genetics of the Breast and Female Genital Organs. Lyon , IARC Press, 2003;9-113. 17. Deugnier MA,Teuliere J, Faraldo M, Thiery J P, Glukhova M.The importance of being a myoepithelial cells lack corresponding immuophenotypic markers .Breast Cancer Research 2003.5:151-156. 18. Boecker W. Prenoplasia of the breast, Munich, Elsevier GmbH pres, 2006, 1: 2-9. 19. Wohlfahrt J, Melby M. Age at any birth is associated with breast cancer risk. Epidemiology. 2004; 12:68-73. 20. Vogel PM, Georgiade NG, et al. The correlation of histologic changes in human breast with the menstrual cycle. Am J Pathol1981;104:23-24. 21. Stenberg SS. Diagnostic Surgical Pathology, 3rd ed. Vol I Philedelphia, Lippincot Williams and Wilkins,1999;319-379. 22. Elston CW, Ellis IO. Pathological prognostic factors in breast cancer.I. The value of histological grade in breast cancer: experience from a large study with long term follow up. Histopathology. 1991;19:403-410. 23. Rosen PP. Rosen’s Breast Pathology, New York, Raven Press, 1992;71-82. 24. Damjanov I, Linder J. Anderson’s Pathology. 10th ed. St Louis, Mosby,1996; 2354-2381 25. Shingleton WW, Mc Carty KS. Breast Carcinoma: An Overview. Gynecol Oncol 1987; 26:271-283. 26. Francis G, BeadletG, Thomas S, Mengersen K.Evalution of estrogen and progesterone receptor status in HER-2 positive breast carcinomas and correlation with outcome. Pathology(October 2006) 38(5), pp. 391-398 76 27. Rakha EA, Putti TC, Abd El Rehim DM, Paish C, et al. Morphological and immunophenotypic analysis of breast carcinomas with basal and myoepithelial differentiation. Journal of Pathology. 2006. 208: 495-506 28. Haber MH, Gattuso P, Spitz DJ, David O. Differential Diagnosis in Surgical Pathology, Philidelphia,WB Saunders Company, 2002; 591-631. 29. Clayton F, Hopkins CL. Pathologic corerelates of prognosis in lymph node positive breast carcinomas. Cancer. 1993; 71: 1780-1790 30. Bocker W, Moll R, Poremba C, et al. Common adult stem cells in the human breast give rise to glandular and myoepithelial cell lineages: a new cell biological concept. Lab Invest. 2002; 82: 737-746. 31. Gabriea Dontu, Dorraya E.A, et al. Breast cancer stem /progenitor cells and the estrogen receptor. Department of nt. Med. Endocrin and Metab. Vol.15 No.5 July 2004. 32. Barbareschi M, Pecciarini L, Cangi G.M, Macri E. P63, a p53 Homologue, Is a Selective Nuclear Marker of Myoepithelial Cells of The Human Breast. The American Journal of Surgical Pathology 25(8): 1054-1060, 2001. 33. Jungueria L.C, Carneiro J. Basic histology. 4th edition. 34. Moll R, Franke WW, Schiller DL: The catalog of human cytokeratins: patterns of expression in normal epithelia, tumors and cultured cells. Cell 1982, 31: 11-24. 35. Dairkee SH, Ljung BM, Smith H, Hackett A: Immunolocalization of a human basal epithelium specific keratin in benign and malignant breast disease. 36. Santini D, Ceccarelli C, Taffurelli M, Pileri S, Marrano D: Differentiation pathways in primary invasive breast carcinoma as suggested by intermediate filament and biopathological marker expression. J Pathol 1996, 179:386-391. 37. Malzahn K, Mitze M, Thoenes M, Moll R: Biological and prognostic significance of stratified epithelial cytokeratins in infiltrating ductal breast carcinomas. Virchows Arch 1998, 433:119-129. 38. Perou CM, Jeffrey SS, van de Rijn M, Rees CA, Eisen MB, Ross DT, Pergamenschikov A, Williams CF, Zhu SX, Lee JC, et al.: Distinctive gene expression patterns in human mammary epithelial cells and breast cancers. Proc Natl Acad Sci USA 1999, 96:9212-9217 39. Siziopikou L, Rees CA, et al.Breast. 2007 FEB; 16(1):104-7. 40. Nielsen TO, Hsu FD, Jensen K, Cheang M, Karaca G, Hu Z, Hernandex-Boussard T, Livasy C, Cowan D, Dressler L, et al.: Immunohistochemical and clinical 77 characterization of the basal-like subtype of invasive breast carcinoma. Clin Cancer Res 2004, 10:5367-5374. 41. Fulford G.L, Reis-Filho J.S, Ryder K, Jones C .et al. Basal-like Grade III Invasive Ductal Carcinoma of the Breast:Patterns of Metastasis and Long-Term Survival.Breast Cancer Research 2007;9(1) 42. Loakso M, Tanner M,Nilsson J, Wiklund T.Basoluminal carcinoma :A New Biologically and Prognostically Distinc Entity Between Basal and Luminal Breast Cancer.Clinical Cancer Research Vol.12,4185-4191,July 15,2006. 43. Kusinska R, Potemski P,JesioneKupnicka D,Kordek R.Immunohistochemical Identification of basal –type cytokeratins in anvasive ductal breast carcinomaRelation with grade, stage,Estrogen Receptor and HER2..Pol J Pathol 2005.56,3,107-110. 44. Kesse –Adu R, Shousha S. Myoepthelial markers are expressed in at least 29% of oestrogen receptor negative invasive breast carcinoma. Modern pathology (2004)17, 646-652. 45. Matos I, Dufloth R,Alveranga M,Zeferino L.C ,et al.p63,cytokeratin5,and pcadherin: three molecular markers to distinguish basal phenotype in breast carcinomas. Virchows Arch(2005) 447:668-694. 46. Filho.R.S.J,Simpson.T.P,Gale.T,Lakhani.S.R.The molecular genetics of breast cancer: The contribution of comparative genomic hybridization. PathologyResearch and practice 201(2005)713-725. 47. Pinilla.S.M,Honrado.E,Hardisson D.Caveolin1 expression is assocated with a basal like phenotype in sporadic and hereditary breast cancer.Breast cancer Research and Treatment (2006) 99:85-90 48. Simpson T.P, Filho.R.S, Gale T,Lakhani S.R.Molecular evalution of breast cancer.J.Pathol 2005;205:248-254. 78