ÇÖZELTİ
ÇÖZELTİ NASIL OLUŞUR?
Çözünen+Çözücü=Çözelti
Örneğin;
Şeker+Su=Şekerli Su
Çözeltiler çözünmenin şekline göre
ikiye ayrılır;
a. İyonlu çözeltiler
Çözünen madde iyonlarına ayrışarak
çözünüyorsa bu çözeltilere iyonlu çözeltiler
denir.
Asit, baz, tuz çözeltileri iyonlu çözeltilerdir.
Bu çözeltiler hareketli iyon bulundurdukları
için elektrik akımını iletirler.
b. Moleküllü çözeltiler
Çözünen madde moleküler olarak
çözünüyorsa bu çözeltilere moleküler çözelti
denir. Şekerin suda çözünmesi bu çözeltilere
örnek olarak verilebilir. Bu çözeltiler elektrik
akımını iletmezler.
Çözeltiler kendi aralarında üçe ayrılır;
a. Doygun çözelti
Çözebileceği maksimum maddeyi çözmüş olan
çözeltiye denir.
b. Doymamış çözelti
Çözebileceği kadar maddeyi çözmemiş olan
çözeltiye denir.
c. Aşırı doymuş çözelti
Bazı durumlarda çözeltinin derişikliği doygunluk
sınırını aşabilir. Bu gibi çözeltilere aşırı doymuş
çözeltiler denir. Bu çözeltiler oldukça kararsızdır.
Küçük bir etki ile fazlalıklar çöker ve doygun bir
çözelti elde edilir.
Çözeltiler çözünenin miktarına göre
ikiye ayrılırlar;
a. Derişik çözelti
Belli bir miktar çözücüde, fazla
miktarda çözünen içeren çözeltilere
derişik çözelti denir.
b. Seyreltik çözelti
Belli bir miktar çözücüde, az miktarda
çözünen içeren çözeltilere seyreltik
çözelti denir.
ÇÖZÜNÜRLÜK
Belli bir sıcaklıkta 100 gram çözücüde gram olarak çözünebilen maksimum
madde miktarına ÇÖZÜNÜRLÜK denir.
Çözgen H2O olduğunda 100 gram yerine 100 ml değeri ile de karşılaşabilirsiniz.
Örneğin,25°C’de KNO3'ün çözünürlüğü,
(60 gram/100 ml su’dur). Yani 25°C’de 100 ml su en fazla 60 gram KNO3
çözebilir.
Çözünürlük=Çözünenin kütlesi
100g su
Çözünürlüğe Etki Eden Faktörler
Çözünen cinsi
Çözücü cinsi
Basınç
Sıcaklık
Ortak iyon
ÇÖZELTİLER ARASI REAKSİYONLAR
İyon içeren iki çözelti karıştırıldığında bazen çökelme olmaz,
bazende iyonlar suda az çözünen bir katı oluşturuyorsa bir
çökelme olur. Yani iyonlar arasında bir tepkime gerçekleşir.
1A grubunun tuzları ve yapısında NO3- iyonu bulunduran tuzlar
suda çok iyi çözünür. Diger tuzlar için bir genelleme yapmak
mümkün degildir.
Örnegin : AgNO3 çözeltisi ile NaCl çözeltileri karıştırıldığında
bir çökelme gözlenir. Burada iyonlar yeniden düzenlenerek
AgCl ve NaNO3 bileşikleri oluştuğu düşünülebilir. NaNO3 suda
çok iyi çözündüğüne göre çöken tuz AgCl'dir.
İyon Denklemi: Ag+(aq) + Cl-(aq) ® AgCl(k)
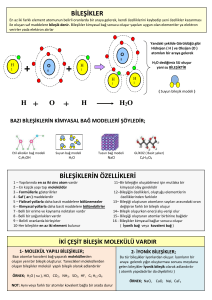
ÇÖZELTİLERİN ÖZELLİKLERİ
Çözeltinin kaynama noktası, saf maddenin
kaynama noktasından yüksektir.
Çözeltinin donma noktası, saf maddenin
donma noktasından düşüktür.
Çözeltinin buhar basıncı, saf maddenin buhar
basıncından düşüktür.
Çözeltilerin yoğunlukları çözeltilerde
çözünen madde miktarına göre değişir.
ÇÖZÜNÜRLÜK DENGESİ (Kç)
Çözeltilerde denge, kimyasal denge ile ilgili genel ilkelerin çözeltilere
uygulanışıdır.
Bu nedenle çözeltilerdeki dengeyi iyi anlayabilmenin yolu kimyasal
dengeyi iyi bilmeye bağlıdır.
Denge sabiti ancak, çok az çözünen iyonlu katılar için uygulanır.
Kç: Az çözünen iyonlu katıların, doygun çözeltisi içerisinde bulunan
iyon derişimlerinin çarpımıdır.
Kç bir denge sabiti olduğundan yalnız sıcaklıkla değişir.
Genel olarak 1A grubunun tuzları, NH4+ ve NO3– li bileşikler suda çok
iyi çözünür. Diğer tuzların suda iyi çözünüp çözünmediğini bilmemize
gerek yoktur.
Bir tuzun Kç sinden bahsediliyorsa suda iyi çözünmediğini
düşünebiliriz.
Mesela bir miktar su alınıp içerisine katı AgCl tuzundan azar azar
eklediğimizde ilk başlarda çözündüğünü gözleriz. Bir süre sonra kabın
dibinde AgCl katısının çözünmeden kaldığını görürüz. Bu noktadan
sonra ne kadar AgCl eklersek ekleyelim hepsi kabın dibine çöker.
Örneğin 25 °C de 1 lt su en fazla 1,6.10–5 mol AgCl çözebilir. 1 lt su
için AgCl miktarı bundan fazla olursa geri kalan kısım dibe çöker.
İlk çökelme olduktan sonra kimyasal olay durmuş değildir. Çözünme
olayı yine sürer fakat çözünmüş olarak bulunan AgCl miktarı
değişmez. Çünkü aynı süre içerisinde çökme olayı da devam
etmektedir. Bu olay bize denge olayını hatırlatır.