PEPTİD HARİTALAMA
4.Ders
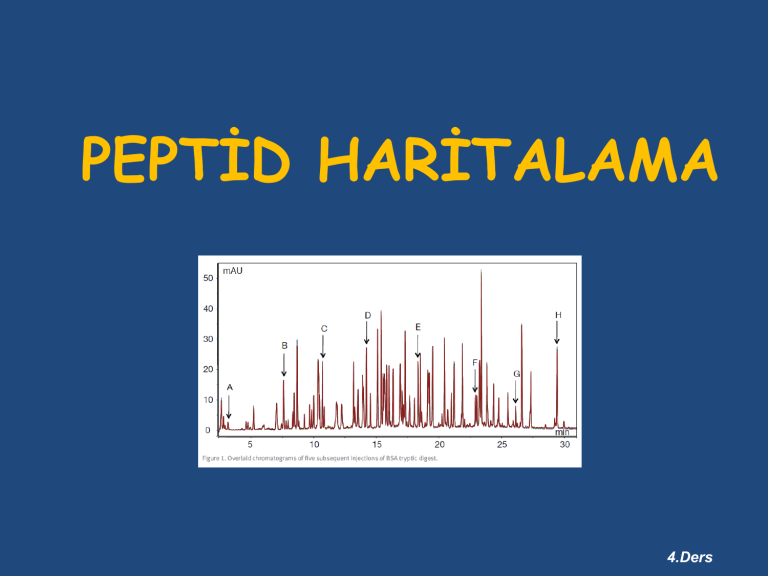
PEPTİD HARİTALAMA
Proteinleri;
• Enzimatik ajanlarla
• Kimyasal ajanlarla fragmentlere ayırma
Peptidleri oluşturan amino asitlerin
karakterizasyonu
Primer yapı
(analitik haritalama)
Diğer proteinlerle olan benzerlik
(karşılaştırmalı haritalama)
ANALİTİK PEPTİD HARİTALAMA
Niçin kullanılır?
Proteindeki posttranslasyonel modifikasyon yerleri
Aktif yerler
Ligand bağlama yerleri
İnternal dizi
Disülfit bağlarının yerleri
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
2. Proteinin indirgenmesi
3. Protein fragmentasyonu
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
a. Kromatografik metodlar
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
a. Kromatografik metodlar
b. Jel elektroforezi
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
a. Kromatografik metodlar
b. Jel elektroforezi
c. Elektroblotlama
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
2. Proteinin indirgenmesi
Birincil yapının kazandırılması
Denatüre edici koşullarda
Örn: 1- O2 ‘siz ortam ve pH8’de
8M üre 6M guanidin-HCl
2- Tiol ajanlarla: β-merkaptoetanol
3- Performik asitle (sisteinleri sisteik
asite dönüştürür)
HARİTALAMA ÖNCESİ HAZIRLIKLAR
1.
Proteinin saflaştırılması
2. Proteinin indirgenmesi
3. Protein fragmentasyonu
Enzimatik
(proteazlar)
Kimyasal
Önerilen 300 rezidülük kesimlerdir
PROTEİN FRAGMENTASYONU
ENZİMATİK FRAGMENTASYON
Seçilen enzim;
Spesifik olmalı
Diğer peptid bağlarına zarar vermemeli
Örn: TRİPSİN
Lizin ve arjinin rezidülerinden kesim yapar
PROTEİN FRAGMENTASYONU
KİMYASAL FRAGMENTASYON
Spesifik olmayan (6M HCl 110°C ‘da 24 saat)
Spesifik olan (JELDE AYRILAN PROTEİNLERDE)
• Siyanojen bromidle kesim
Metionin rezidülerinden kesim yapar
PROTOKOL: TRİPSİN KULLANARAK PROTEİNLERİN
FRAGMENTASYONU
Lizin ve arjinin rezidülerinden kesim yapar
METOD:
1. Protein substratı, yeterli konsantrasyon sağlanacak şekilde %1 amonyum
bikarbonatta çözdürülür.
2. Substrat:enzim oranı denatüre proteinler için 200:1 ila 50:1 arasında, doğal
proteinler için 1:1 oranında olacak şekilde tripsin eklenir.
3. 16 saat boyunca tripsin proteinle inkübe edilir.
4. Peptid haritalama için reaksiyon durdurulduktan sonra örnek RP-HPLC
kolonuna yüklenir.
JELDE AYRILAN PROTEİNLERDE UYGULAMALAR
1- JELDE PROTEİNLERİN GÖZLEMLENMESİ:
• Coomassie Blue
0.5-1 mg aralığındaki proteinler
• Negatif Boyama
Sodyum asetat, bakır klorid
• Gümüş Boyama
1-10 ng aralığındaki proteinler
JELDE AYRILAN PROTEİNLERİN DİZİLENMESİ
• Proteinlerin jelden geri kazanımı
• Proteinlerin PVDF yada nitroselüloz membrandan geri kazanımını gerektirir.
Ya da
Direkt olarak jelde peptid ayırım yapılır.
Proteinler inkübasyon süresi yada enzim konsantrasyonu giderek artan
kolonlardan geçirilir.
RP-HPLC (Reversed- Phase High Pressure liquid Chromatography)
KULLANARAK PEPTİD TAYİNİ:
RP-HPLC:
Apolar bir sabit faz polar hareketli faz içeren bir kolondan peptidlerin geçmesi
Farklı solüsyonlar kullanılır. Solvent A, B
A=sulu çözelti (trifluoroasetik asit) ,
B= organik (asetonitril)
Peptidlerin 214 nm UV absorbası alınır.
EDMAN DEGRADASYONU İLE HARİTALAMA METODU
• N-terminal uç (amino-ucu) işaretlenir ve peptidden kesilir.
• Tek tek tüm amino asitler elde edilir.
• Amino asitler kromotografi veya elektroforezle belirlenebilir.
• 20 amino asit kadarı belirlenmiştir.
AMİNOASİTLER
Apolar
Polar, asidik
Polar, nötral
Polar, bazik
KÜTLE SPEKTROMETRİSİ












