LYS KİMYA YT.indd
advertisement

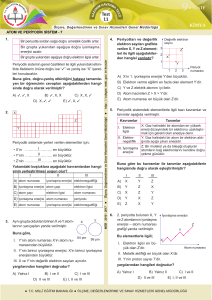
Modern Atom Teorisi – 4 1. Atom Blok I. 2He s II. 26Fe p III. 13Al d IV. 90Th f 12 - B KAVRAMA Test 4 STİ TE KAZ AN IM KİMYA 5. r1 r2 Xn X Yukarıdaki öncüllerin hangisilerinde atomların periyodik cetvelde ait oldukları bloklar doğru verilmiştir? X atomu ve iyonunun yarıçapları sırasıyla r1 ve r2 ile gösterilmiştir. A) Yalnız I Buna göre; B) I ve IV D) II, III ve IV C) I, II ve III E) I, II, III ve IV 2. Temel hâl elektron dağılımında s orbitallerinde toplam 7 elektron bulunduran atomların toplam proton sayısı kaçtır? A) 72 B) 68 C) 64 D) 60 I. n < 0 ise r2 > r1’dir. II. n > 0 ise r1 = r2 olabilir. III.r1 > r2 ise X metal olabilir. ifadelerinden hangileri yanlıştır? A) Yalnız I E) 56 B) Yalnız II D) II ve III C) Yalnız III E) I, II ve III I.Ametaldir. II. Küresel simetriktir. III. 16. grup üyesidir. ifadelerinden hangisi doğru olabilir? A) Yalnız II B) Yalnız III D) I ve III MEB 2016 - 2017 3. Temel hal elektron dağılımında 6 tane tam dolu orbitali bulunan elementle ilgili; C) I ve II E) I, II ve III 4. r1 r2 F r2 r1 6. F II Yukarıdaki şekilde iki tane F atomunun birbirine en yakın olabildiği konum modellenmiştir. Buna göre flor atomu için; I. Kovalent yarıçapı r2’dir. II. Van der Waals yarıçapı r1’dir. III. Çapı 2r1’dir. ifadelerinden hangileri doğrudur? A) Yalnız I B) Yalnız II D) I ve II I Yukarıda verilen periyodik cetvel şablonuna göre aşağıdakilerden hangisi yanlıştır? A) I yönünde oksitlerin asitlik kuvveti artar. B) II yönünde hidroksitlerin bazik karakteri artar. C) I yönünde atom çapı azalır. C) Yalnız III E) I, II ve III D) II yönünde metalik karakter azalır. E) Her iki yönde de atom numarası artar. 12 - B Test 4 KİMYA Modern Atom Teorisi – 4 7. 3. periyotta bulunan X, Y ve Z atomlarının proton sayıları arasındaki en büyük fark 2’dir. I1 I2 I3 I4 X 496 4560 6910 9540 Y 600 1150 4500 6500 Z 577 1820 2745 16600 11. Bu elementlerin 1. iyonlaşma enerjileri arasındaki ilişki X > Y > Z olduğuna göre X elementi periyodik cetvelin hangi gruplarında kesinlikle bulunamaz? A) 1., 13. ve 16. B) 2., 15. ve 18. C) 2., 13. ve 17. D) 1., 14. ve 16. Baş gruplarda olduğu bilinen X, Y ve Z elementleri için ilk dört iyonlaşma enerjisi değerleri kj/mol cinsinden verilmiştir. Buna göre; E) 1., 15. ve 17. 8. Bağ uzunluğu 230 pm olan X2 molekülündeki X atomunun Van der Waals yarıçapı pm cinsinden aşağıdakilerden hangisi olabilir? A) 100 B) 115 C) 130 D) 230 E) 250 I. X ve Y elementlerinin temel hâl e– dizilimleri küresel simetriktir. II. Z elementi p bloğundadır. III. Y’nin çapı X’ten küçüktür. ifadelerinden hangisi kesinlikle doğrudur? A) Yalnız I B) Yalnız II 9. Yusuf, 7N, 8O ve 9F elementleri ile ilgili aşağıdaki karşılaştırmaları yapıyor. I. Elektron ilgisi en büyük olan F’dir. II. Ametalik aktifliği en fazla olan N’dir. III. Hidrojenli bileşikleri içinde en bazik olanı NH3’tür. IV. 1. İyonlaşma enerjisi en küçük olanı oksijendir. V. Kovalent yarıçapı en küçük olan N’dir. Buna göre bu karşılaştırmalardan kaç tanesi doğrudur? A) 1 B) 2 10. C) 3 X D) 4 E) 5 Y E) II ve III MEB 2016 - 2017 D) I ve II C) Yalnız III 12. I. Gaz halindeki bir mol atoma bir mol elektron eklenmesi sırasında meydana gelen ısı değişimine ................. denir. II. Gaz halindeki bir mol atomdan bir mol elektron koparmak için gereken enerjiye ............................ denir. Z Yukarıda periyodik cetvelin baş gruplarından bir kesit verilmiştir. III. Bir elementin, bileşiklerindeki bağ elektronlarını çekebilme gücüne .................................... denir. Buna göre; IV. Komşu iki atom çekirdeği arasındaki uzaklığın yarısına .................... denir. I. I. iyonlaşma enerjisi en büyük olan X’tir. II. Elektronegatifliği en büyük olan Y’dir. III. Atom çapı en büyük olan Z’dir. Yukarıdaki tanımlamalarda boşluklar doğru bir şekilde doldurulursa aşağıdaki seçeneklerden hangisine gerek duyulmaz? ifadelerinden hangisi kesinlikle doğrudur? A) Aktiflik B) Elektron ilgisi A) Yalnız I C) Atom yarıçapı D) Elektronegatiflik B) Yalnız II KAVRAMA IM STİ TE KAZ AN D) II ve III C) Yalnız III E) İyonlaşma enerjisi E) I, II ve III 1 2 3 4 5 6 7 8 9 10 11 12 Adı :......................................................... Doğru :..................................... Soyadı :......................................................... Yanlış :..................................... Sınıf :......................................................... Boş No :......................................................... :..................................... Puan :..................................... E E E E E E E E E E E E