
Organik Bileşikler
• Kimya bilimi temelde organik kimya ve
anorganik kimya olarak ikiye ayrılır.
• Bu sunu süresince organik bileşiklerle ilgili
genel özellikleri anorganik bileşiklerden
farklarını ve bazı yaygın organik bileşikleri
öğreneceksiniz.
• Organik kimya yapısında C H N ve O
elementleri bulunduran maddeleri
inceler.Kısaca karbon kimyası olarak
adlandırılır.karbon kimyasına organik madde
denmesinin en önemli nedenlerinden biride
bu maddelerin genellikle canlı organizmaların
yapısında bulunmasıdır.
• Organik bileşiklerin bitki ve hayvanlardan elde
edilmesi çok eskilere dayanır.
• El-Razi 900 yıllarda ilk defa bitkilerden saf alkol
elde etmiştir.
• Aspirin söğüt yaprağından, penisilin ise ilk defa
küflü peynirden elde edilmiştir.
• Günümüzde kullanılan bir çok organik madde
yapay olarak elde edilmektedir.
• Kimyasal maddeler, 19. yüzyıl başlarında
organik ve anorganik maddeler olarak
sınıflandırılmıştır.
• Organik maddeler, büyük ve karışık yapılarda
maddeler oldukları ve genellikle canlı
organizmalarda bulundukları için bu
maddelere “hayatın gücü” denmiş ve uzun
yıllar boyunca laboratuar şartlarında elde
edilemeyecekleri düşünülmüştür.
• 1828 yılında alman kimyacı Friedrich Wöhler,
laboratuarda anorganik bir madde olan KCN
den organik bir madde olan üreyi elde etmiştir.
Wöhler böylece organik maddelerin
laboratuar şartlarında elde edilebileceğini
ispatlamıştır.
• Organik maddelerin bu şekilde elde
edilişinden sonra hızla yeni maddeler elde
edilmiş ve günümüzde milyonlarca çeşit
organik bileşik kullanılmaktadır.
• Organik bileşiklerin bu şekilde çok olmasının
nedeni C atomunun çok sayıda çeşitlilikte
bağlanabilme kabiliyeti ile ilgilidir.
ORGANİK VE ANORGANİK BİLEŞİKLER
• Organik hemen hemen tamamında C ve H
atomu vardır. Bu nedenle CO2, CO, CS’ gibi
bileşikler ve karbonat içeren bileşikler organik
bileşik sınıfına dahil edilmezler.
• Şimdi organik ve anorganik bileşikler
arasındaki farkları inceleyelim:
Organik ve anorganik bileşikler arası farklar
• 1. Organik bileşikler genellikle yanıcıdır. İnorganik bileşikler yanıcı
değildir.
2.Organik bileşiklerin erime noktaları genellikle düşüktür.(300 c nin
altındadır.) İnorganik bileşiklerin ise genellikle yüksektir.
3.Organik bileşikler genellikle suda çözünmezler,inorganiklerin çoğu suda
çözünürler.
4.Organik bileşikler çoğunun yapısı iyonik değildir. inorganikler ise iyonik
yapıdadır.
5.Organik bileşiklerin kendilerine özgü bir renk ve kokuları
vardır.Anorganik bileşiklerde ise bu oran daha azdır.
6. Organik bileşiklerin oluşumunda katalizörlerin rolü büyüktür.farklı
katalizörler kullanılarak aynı maddelerden farklı bileşikler oluşturulabilir.
7. Organik bileşiklerle yapılan reaksiyonlar fazla ısı ve zaman gerektirirler
,inorganik bileşiklerin reaksiyonları daha hızlıdır.
8. Organik bileşiklerin yoğunlukları genellikle düşüktür.
Organik Bileşiklerin Sınıflandırılması
Ornagik bileşikler fonksiyonal (işlevsel) gruplara göre sınıflandırılırlar.
Fonksiyonal Grup: Belirli kimyasal davranış gösteren atom grupları.
Bazı fonksiyonal
gruplar:
R
R
R
alkanlar
H
H
N
alkenler
R
R
aminler
O
H
R
organik asitler
H alkinler
R
R
OH
O
H
O
aldehitler
esterler
R
OR
O
R
O
ketonlar
R
R'
R amitler
R
N
R
R,R’: Hidrokarbon zinciri
Organik Bilesiklerin Islevsel Gruba Gore Siniflandirilmasi (I)
bilesigin sinifi
yapi
A- Molekul iskeletinin bir parcasi olanlar
B- Oksijen iceren islevsel gruplar
a- karbon oksijen tekli bagi olan
C C
alkan
C C
alken
C C
alkin
C
C
b-karbon oksijen ikili bagi olan
OH
O
C
alkol
eter
H
C
O
aldehit
C
keton
O
C
C
O
c- karbon oksijen hem tekli hem ikili
bag olan
C
OH
karboksilli asit
O
C
O
C
ester
Organik Bilesiklerin Islevsel Gruba Gore Siniflandirilmasi (II)
bilesigin sinifi
yapi
C-Azot iceren islevsel gruplar
C NH2
primer amin
C N
siyanur
(nitril)
D- Azot ve Oksijen iceren islevsel gruplar
O
C NH2
E- Kukurt iceren islevsel gruplar
C SH
C
S
C
primer amid
tiyol
(merkaptan)
tiyoeter
Soru: Asagidaki bilesiklerin yapisal formullerini cizelgeyi kullanarak yaziniz
C4H10O (alkol)
C3H8O (eter)
C3H6O2 (karboksilli asit)
C3H6O (aldehit)
C5H10O2 (ester)
C4H8O (keton)
C3H9N (amin)
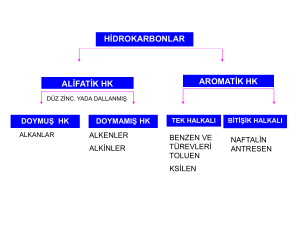
HİDROKARBONLAR
ALİFATİK HK
AROMATİK HK
DÜZ ZİNC. YADA DALLANMIŞ
DOYMUŞ HK
ALKANLAR
DOYMAMIŞ HK
ALKENLER
ALKİNLER
TEK HALKALI
BENZEN VE
TÜREVLERİ
TOLUEN
KSİLEN
BİTİŞİK HALKALI
NAFTALİN
ANTRESEN
Hidrokarbonlar
Alifatik
Aromatik
Hidrokarbonlar
Alifatik
Aromatik
Doymuş HK
Alkanlar
Doymamış HK
Alkenler
Alkinler
Hidrokarbonlar
•
Alifatik
Alkalar
Alkanlar yapı
içindeki bağların
tamamının tekli bağlar
olduğu
hidrokarbonlardır.
H
H
H
C
C
H
H
H
Hidrokarbonlar
•
Alifatik
Alkenler yapı
içinde karbon-karbon
çift bağı içeren
hidrokarbonlardır.
H
H
C
Alken
H
C
H
Hidrokarbonlar
•
Alifatik
Alkinler yapı içinde
karbon-karbon üçlü
bağı içeren
hidrokarbonlardır.
Alkinler
HC
CH
Hidrokarbonlar
•
En çok karşılaşılan
aromatik hidrokarbonlar
benzen halkası içeren
yapılardır.
Aromatik
H
H
H
H
H
H
FORMÜL VE FORMÜL ÇEŞİTLERİ
Bileşiklerin kısaca gösterilmelerine FORMÜL denir.
Organik Kimyada formüller Kapalı - Yarı Açık - Açık
olmak üzere 3 grupta ifade edilirler.
İsim
Kapalı
Yarı Açık
Açık
H H
Etan
C2H6
CH3-CH3
H
C C H
H H
Propan
C3H8
CH3-CH2-CH3
H H H
H C C C H
H H H
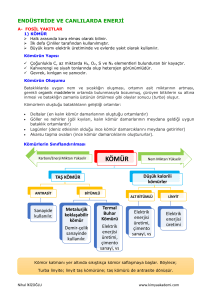
HİDROKARBONLAR
C ve H den oluşmuş organik
HİDROKARBONLAR denir.
bileşiklere
Hidrokarbonlar, ALİFATİK ve AROMATİK
hidrokarbonlar olmak üzere iki gruba ayrılırlar.
Aromatik olmayan hidrokarbonlara,
Hidrokarbonlar denir.
Alifatik
Alifatik Hidrokarbonlar, düz, zincirli ve dallanmış
yada halkalı biçimde olabilirler.
H H
Alifatik
Hidrokarbonlar,
doymuş ve doymamış biçimde
de sınıflandırılabilir.
H
C C H
H H
C-C tekli bağları,
C=C ikili bağları,
C≡C üçlü bağları
görülmektedir.
C
H
C
C≡C
H
Doymuş hidrokarbonlara ALKAN; ikili bağ içeren
doymamış hidrokarbonlara ALKEN, üçlü bağ içeren
doymamış hidrokarbonlara ALKİN denir.
H H
H
C C H
H H
C2H6 Etan
ALKAN
H
H
C
C
H
H
C2H6 Eten (Etilen)
ALKEN
H
C≡C
H
C2H2 Etin
(Asetilen) ALKİN
ALKAN
1. Genel formülü CnH2n+2 dir.
H H
H
C C H
H H
C2H6 Etan
ALKAN
2. C atomları arasındaki bütün bağlar
tekli bağdır.
3. İsimlendirme yapılırken sonu na -an
eki getirilir.
4. Doymuştur.
5. En küçük üyesi 1 karbon atomludur
ALKEN
1.Genel formülü CnH2n dir.
2. C atomları arasında en az bir
tane 2 li bağ vardır.
3. İsimlendirme yapılırken sonu
na -en eki ya da -ilen eki
getirilir.
4. Doymamıştır.
5. En küçük üyesi 2 karbonludur
H
H
C
C
H
H
C2H4 Eten (Etilen)
ALKEN
ALKİN
1. Genel formülü CnH2n–2 dir.
2. C atomları arasında en az
bir tane 3 lü bağ vardır
3. İsimlendirme yapılırken
sonu na -in eki getirilir.
4. Doymamıştır.
5. En küçük üyesi 2
karbonludur
H
C≡C
H
C2H2 Etin
(Asetilen) ALKİN
ALKAN
CH4
Metan
C2H6
Etan
C3H8
Propan
C4H10
Bütan
C5H12
Pentan
C6H14
Hegzan
C7H16
Heptan
C8H18
Oktan
C9H20
Nonan
C10H22 Dekan
ALKEN
—
C2H4
C3H6
C4H8
C5H10
C6H12
C7H14
C8H16
C9H18
C10H20
Eten(Etilen)
Propen
Büten
Penten
Hegzen
Hepten
Okten
Nonen
Deken
ALKİN
—
C2H2
C3H4
C4H6
C5H8
C6H10
C7H12
C8H14
C9H16
C10H18
Etin(Asetilen)
Propin
Bütin
Pentin
Hegzin
Heptin
Oktin
Nonin
Dekin
AROMATİK HİDROKARBONLAR
Aromatik Hidrokarbonlar denildiğinde;
1. Halkalı yapı gösterirler.
2. Halkadaki bağlar tek-çift-tek-çift şeklinde
sıralanmıştır ve Molekül tek düzlemlidir.
3. Aromatik hidrokarbonlar doymamış oldukları
halde, doymamış hidrokarbonların özellikleriniz
göstermezler.
4. En önemlisi benzen bileşiğidir.
AROMATİK HİDROKARBONLAR
Aromatik hidrokarbonların en basit örneği benzen dir.
CH
HC
CH
HC
CH
CH
BENZEN
(C6H6)
BENZEN;
1. Halkalı yapı gösterir
2. Halkadaki bağlar tek-çift-tek-çift
şeklinde sıralanmıştır.
3. Aromatik hidrokarbonlar doymamış
oldukları halde, doymamış
hidrokarbonların özellikleriniz
göstermezler.
AROMATİK HİDROKARBONLAR
Diğer bir üyesi naftalindir. (C10H8)
Diğer bir üyesi de antresendır. (C14 H10)
BENZEN
NAFTALİN
ANTRESEN
b. Fonksiyonel grupları farklıdır.
Örnek: Alkoller-eter
CH3-CH2-OH
CH3-O-CH3
Etil alkol
Di etil eter
c. Fonksiyonel grupların yerlerinde farklılık vardır.
Örnek: C5H10 da çift bağların yerleri farklıysa;
CH3-CH═CH-CH2-CH3
CH2═CH-CH2-CH2-CH3
2-penten
1-penten






![C Elementi [Slayt]](http://s1.studylibtr.com/store/data/000924935_1-effe9d67aa73b7116686c4c63d62e23f-300x300.png)



