BİY 315
PROTEİNLER
Yrd. Doç
Yrd
Doç. Dr
Dr. Ebru SAATÇİ
2008-2009 Güz Yarı Dönemi
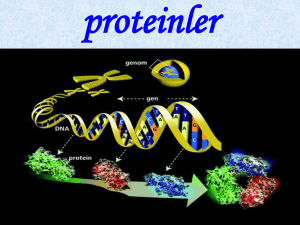
Pro ve Ökaryotlarda Translasyon
Prokaryotlarda transkripsiyon ve
t
translasyon
l
ardışıktır:
d kt
transkripsiyon bir yandan sürerken
translasyon 5’ ucunda başlar.
Ökaryotlarda ise hücrenin farklı
yerinde
i d olur
l transkript
ki ö
önce iişlenir
l i
sonra sitoplazmaya geçer.
Protein Yapısı
Proteinler 4 düzeyde organize olurlar
Primer yyapı,
p , düz lineer biçimde
ç
A.A. dizilimidir
Sekonder yapı polipeptit zincirinin katlanmasıyla oluşan özel bir
yapıdır bu yapı lineer yapıdaki yakın A.A. arasında bağ
güçlerinden oluşur: zayıf bağlar (H bağları,
bağları elektrostatik güçler
ve van der waals bağları). En genel tipleri ise alfa sarmal, beta
plakadır. Aynı protein bu yapılardan birini yada her ikisini
i
içerebilir.
bili
Tersiyer yapı sekonder yapının katlanmasıyla oluşur.
Quaterner yapı ise bir yada birkaç polipeptidin katlanarak
altbirimleriyle oluşturduğu kompleks yapıdır. Bu yapı farklı
polipeptidlerden oluşursa heterodimer, aynı tip polipeptidler
arasında olursa homodimer oluşturur.
oluşturur
Bazı proteinler kompakt yapıdadır enzim ve antikorlar globüler
yapıdadır lineer yapıdaki proteinlere ise fibröz proteinler denir.
Primer (Birincil) Yapı
Amino asitlerin polipeptit zinciri üzerinde nitel ve nicel
sıralanışlarını, protein molekülünün bir veya daha fazla
sayıda da polipeptit zincirinden oluşup oluşmadığı
hakkında bilgi veren yapıdır.
Proteinler,amino asit dizileri değişerek
ğ
farklılaşırlar.
Koruyucu (konservatif) değişimler: A.A. yan zincirinin
karakteri değişmez. Örneğin, Asp yerine Glu geçişi gibi.
Bazıları ise koruyucu olmayan (non-konservatif) tiptedir.
Bunlarda daha köklü bir değişim vardır. Örneğin, Asp
yerine
i Al
Ala geçer.
• Bazı proteinler kovalent veya kovalent olmayan bağlarla bir
arada
d tutulan
l
1d
1’den
f l sayıda
fazla
d polipeptit
li
i zinciri
i i i içerirler.
i il
İnsülin hormonu, kovalent bağlarla (disülfit bağları) bir arada
tutulan 2 polipeptit zinciri içerir.
içerir
Sekonder (İkincil) Yapı
İkincil yapıyı zincirdeki karbonil grubu ile imido grupları
arasında oluşan hidrojen bağları oluşturur.
Z f hidrojen
Zayıf
hid j bağları
b ğl
bi polipeptit
bir
li
tit zincirinin
i i i i içinde
i i d oluştuğu
l t ğ
gibi komşu polipeptit zincirleri arasında da oluşabilir.
İkincil yyapılar
p
α-heliks yyada yyada ββ-pilili
p
tabaka şşeklinde olabilir.
Alfa sarmal
Beta pilili tabaka
α-Helix
α-Heliks’te zayıf
hidrojen bağı
bağı,
bir peptit
bağındaki
g
elektronegatif
azot atomuna
bağlı H atomu
ile bu peptit
bağından
sonraki
dördüncü
amino asidin
karbonil
grubunun
oksijen atomu
arasında
oluşmaktadır.
(a) Sağ el dönüşlü αα-heliks
heliks oluşumu.
(b)Sağ el dönüşlü α-heliksin zinciriçi H-bağlarını gösteren top- ve
çubuk modeli. Tek bir dönüş 3.6 A.A. kalıntısı içerir.
Bir peptit zincirinin α-heliks oluşturabilmesi için ya sadece Lf
formundaki
d ki amino
i
asitleri
i l i veya sadece
d
Df
D-formundaki
d ki a.a. içermesi
i
i
gerekir.
Saç, kıl, tüy, yün, boynuz, tırnak, deri ve kuş tüyü gibi α-keratinlere dahil
proteinler genellikle soldan sağa dönüşlü α-heliks düzenlemesi gösterirler.
α-heliks Kararlılığını Etkileyen Faktörler:
1. Yüklü
kl R grupları
l olan
l ardışık
d kA
A.A.
A arasında
d oluşan
l
elektrostatik itme gücü,
2 Bitişik
2.
Bi i ik R gruplarının
l
hacmi,
h
i
3. Üç veya dört A.A. arayla yerleşmiş amino asitlerin yan
zincirleri
i i l i arasındaki
d ki etkileşim,
kil i
4. Pro ve Gly yapıdaki varlığı,
5. Heliks yapısının her iki ucunda bulunan A.A. arasındaki
etkileşim ve elektrik dipolü.
β-pilili tabaka
β tabaka yapıda polipeptit zinciri zig zag bir görünüm ortaya
k
koyar.
Yan
Y yana duran
d
zig
i zag polipeptit
li
i zincirleri
i i l i arasında
d H
Hbağları oluşur.
H b ğl rı karşı
H-bağları
k rşı karşıya
k rşı gelen petit bağlarının
b ğl rının amino
mino vee kkarbonil
rbonil
grupları arasında meydana gelir.
β tabaka yapıda komşu polipeptit zincirleri paralel ya da
antiparalel olabilir (amino ve karboksil uçları aynı veya zıt yönde
olabilir).
)
β-pilili tabaka konfigürasyonu, ipek lifi gibi gerilmiş protein
moleküllerinde görülmektedir.
α-heliks ısı ve nemin etkisiyle β-pilili tabakaya dönüşebilir.
Bitişik zincirler arasında oluşan H
H-bağının
bağının çapraz bağları da
görülmektedir.
((a)) Antiparalel
p
ββ-tabakada bitişik
ş zincirlerin amino ve karboksil uçları
ç
birbirine ters yöndedir.
(b)Paralel β-tabaka
• Gly
Gl ve P
Pro a.a.
kalıntıları betakıvrımlarının içinde
genellikle beraber
bulunur.
• Gly küçük ve
esnektir. Pro’nin imino
azotunu içeren peptit
b ğl cis
bağları
i
konfigürasyonuna
dönüşür.
• Tip I, Tip II den
daha sıklıkta bulunur.
Tip II kıvrım
yapısında 3. a.a. Gly
bulunur.
Tersiyer (Üçüncül) Yapı
Kuarterner (Dördüncül) Yapı
Tersiyer yapıya sahip
iki yada daha fazla
sayıda
d polipeptit
li
tit
zincirlerinin bir araya
gelmesiyle oluşur
oluşur.
Bu yapıda kovalent
bağlar rol oynamaz.
oynamaz
Proteinlerin Denatürasyonu
Denatüre edici etkenler:
Isı
pH
Organik
g
çözücüler
ç
Üre ve guanidin
bileşikleri
Ortama eklenmiş olan
üre ve merkaptoetanolün
uzaklaştırılması ile
proteinin (ribonükleaz)
renatürasyonu (disülfit
b ğl
bağlarının
yeniden
id
oluşumu)
gözlenmektedir.
Proteinlerin Biyolojik Fonksiyonları
Enzimler: Metabolizmayı düzenleyen ve etkileyen globuler proteinler ( geniş
bir protein sınıfı)
p
Biyokimyasal reaksiyonları katalizlerler
p
Substrat özgüllükleri vardır.
p
.... az şeklinde adlandırılır
p Eksiklikleri pek çok metabolik hastalıkla sonuçlanır.
Düzenleyici proteinler: Fizyolojik aktivitenin düzenlenmesinden sorumludurlar.
Örn: Hormonlar (insülin eksiklliği → diabet)
G-proteinler → Hücre içi haberleşme
Yapısal proteinler: Kas,
Kas, bağ dokusu proteinleri,
proteinleri membran proteinleri
Örn: Kollajen (tendon and ligamentlerde)
keratin ((saçç ve tırnakta))
Besin ve Depo proteinler: Ovalbumin, laktalbumin, kazein, ferritin
Transport proteinleri: Plazmada ve membranlarda spesifik maddelerin veya
i
iyonların
l
taşıyıcısıdırlar
d l
Örn: Hb-O2, miyoglobin-O2
Lipoprotein-lipid,
Lipoprotein
lipid, Transferrin
Transferrin-Fe
Fe
Seruloplazmin-Cu, vb
K
Kontraktil
k il proteinler:
i l Kasılmayı
K l
ve hareketi
h k i sağlayan
ğl
proteinler
i l
Ör:Miyozin - kalın filament
Aktin - İnce filament
Tübilin - membran iskeleti
Reseptörler:
R
tö l Hücre
Hü
i i haberleşmede
içi
h b l
d roll oynarlar
l
Örn: adrenalin için ß-adrenerjik reseptor
Savunma proteinleri: İmmünoglobülinler: Patojenlere karşı organizmayı
korurlar.
Fibrinojen: (Pıhtılaşma mekanizması)
Proteinlerin Sınıflandırılması
Fibröz Proteinler
Spiral
p
veya
y heliks şşeklinde kıvrılmış,(kovalent
ş,(
ve
H bağlarıyla çapraz bağlanmış) zincirlerden
oluşurlar
Bitkilerde bulunmazlar.
Bağ dokusu proteinleri
Kollajen, Elastin, Keratin
Miyozin: Kas proteini
Fibrinojen: pıhtılaşma proteini
Kollajen:
j
Birbirine sarılmışş 3 p
polipeptid
p p
zinciri (üçlü heliks)’nden oluşur.
Memelilerde total proteinin
%30’
%30’unu
teşkil
t kil eder.
d
Gl Al P L ’d zengindir.
Gly,Ala,Pro,Lys’den
i di
Proteolitik
P
li ik
enzimlere
karşı dirençlidir.
Keratin
İki zincirli
helezonik
sarmal
Globüler Proteinler
Sıkıca katlanmış helezon şeklinde polipeptid zincirlerden oluşur. (Proteinlerin
büyük kısmı, bu gruptadır). Örn: Hemoglobin, Miyoglobin
Miyoglobin monomerik, hemoglobin oligomerik (tetramerik) proteindir.
MİYOGLOBİN
HEMOGLOBİN
Miyoglobin
İnsan ve balinanın miyoglobin
m l küll rind ki amino
moleküllerindeki
min asit
it
dizilerinin karşılaştırılması:
Bu örnekte verilen miyoglobin 153
amino asitten oluşur. Bu iki
miyoglobinin
i l bi i amino
i asit
i di
dizileri
il i
benzer olmakla beraber özdeş
değildir.
α-heliks bölgelerince zengin
tek zincirli bir polipeptittir.
%80’i 8 adet
d t α-sarmalından
α rm lınd n
(A-H) oluşur:
Hem grubu molekülün apolar özellikteki iç
kısmına (F ve E sarmalları arasındaki cebe)
yerleşmiştir. Bu cep apolar amino asitlerle
çevrilidir. Bunlardan 2 tane histidin kalıntısının çok
ö l ffonksiyonları
özel
k i l vardır:
d
PROKSİMAL HİSTİDİN : Doğrudan HEM’in
demirine bağlıdır.
DİSTAL HİSTİDİN : HEM ile doğrudan
etkileşmez Oksijenin +2 değerlikli demire
etkileşmez.
bağlanmasını stabilize eder. Böylece Fe+2 çok az
okside olarak oksijenin geri dönüşümlü bağlanması
sağlanır.
sağlanır
myo- Yunanca’da “kas”
hemo- ise “kan” anlamına gelir.
Hem
em grubu içerir
içerir, yani bileşik proteindir
proteindir. Oksijeni bağlayan
bu grup, protein kısmına (globin) kovalent olmayan
etkileşimlerle
ş
bağlı
ğ durumdadır.
Hem
(Demir protoporfirin)
Hemoglobin
Hemoglobin kırmızı kan
hücrelerinde (eritrositler) yer
alan oksijen taşıyıcı proteindir.
Omurgalıların hemoglobini
her biri bir molekül oksijen
bağlayan birer hem grubu
içeren ikişer alt birimden
((toplam
p
4 altbirimden)) oluşur.
ş
Erişkin insanlardaki
hemoglobinin büyük bir kısmı
2α+2β altbirimi içeren
Hemoglobin
l bi A ((HbA)’dır.
bA) d
Ayrıca %2 oranında
Hemoglobin A2 (HbA2)
(2α+2δ zinciri
i i i iiçerir)
i ) bulunur.
b l
Oksihemoglobin: Oksijen bağlı hemoglobin (Demir:
Fe2+ formda bulunur): Hemoglobin relaks (gevşek),
R durumundadır.
durumundadır
Deoksihemoglobin: Bağlı oksijenin Hb’den
ayrıldıktan sonra ki durumu (Demir: hala Fe2+
formdadır): Hemoglobin tense (gergin), T
durumundadır.
Methemoglobin: Demir,
Demir okside Fe3+ formundadır.
formundadır
Bu form oksijen bağlayamaz.
K b k ih
Karboksihemoglobin:
l bi Karbon
K b monoksit
k i (CO)
bağlanmış hem grubu içerir. O2 taşıyamaz.
Memelilerdeki Oksijen Transferi
Hemoglobinin T ve R durumu
Oksijenin bağlı olduğu (R durumu) ve oksijenin bağlı olmadığı
(T) durumu.
T durumunda çok sayıda iyon çifti kararlı halde bulunduğundan,
R durumuna göre daha kararlıdır. R durumunun oksijene
affinitesi, T’ye
y g
göre daha yyüksektir.
Hb’nin Oksijeni Bağlama Kinetiği
Hb’nin dört tane oksijen
b ğl
bağlama
böl
bölgesii vardır.
d B
Bu
bölgeler, oksijeni kooperatif
olarak bağlarlar
bağlarlar.
Hb allosterik bir proteindir.
Bir bağlanma bölgesine
oksijen (ligand) bağlandığı
zaman,, diğer
ğ bağlanma
ğ
bölgelerini etkileyerek, diğer
bölgelerinde O2 bağlama
kapasitesini arttırır.
Oksijen dissosiasyon eğrisi
Farklı parsiyel oksijen
basınçlarında (pO2) ölçülen
Y’lerin
Y
lerin grafiğine oksijen
dissosiasyon eğrisi denir.
Miyoglobin ve hemoglobinin
eğrileri önemli farklılıklar
gösterir. Bu grafik miyoglobinin
oksijene ilgisinin
hemoglobinden daha fazla
olduğunu göstermektedir
göstermektedir.
Bağlanma bölgelerinin yarısının
doyurulması için gereken
parsiyel oksijen basıncı (P50)
miyoglobin için ortalama
1mmHg ve hemoglobin için
26mmHg’dir. [Oksijene ilgi ne
kadar fazlaysa (yani
(yani, oksijen ne
kadar sıkı bağlanıyorsa) P50 o
kadar düşüktür.]
Bohr etkisi:
p düşürüldüğünde
pH
ş
ğ
veya
y hemoglobin
g
yyüksek CO2 p
parsiyel
y
basıncında bulunuyorsa oksijenin hemoglobinden ayrılması
kolaylaşır. Her iki halde de hemoglobinin oksijene ilgisi
azalır
l ve bu
b yüzden
d
oksijen
k ij
di
dissosiasyon
i
eğrisinde
i i d sağa
doğru kayma meydana gelir. Oksijen bağlanmasındaki bu
değişikliğe Bohr etkisi denir.
denir Tam tersine,
tersine pH
pH’nın
nın artması
veya CO2 konsantrasyonunun azalması oksijene ilginin
artmasına ve oksijen
j
dissosiasyon
y
eğrisinde
ğ
bir sola
kaymaya neden olur.
Hb-O2 Dissosiasyon Eğrisini Kayması
Yüksek İlgi
Düşük İlgi
Hb-O2 Dissosiasyon eğrisini sağa kaydıran nedenler ;
- H+ artışı
Vücut sıcaklığının artışı
pH düşmesi
Eritrositlerdeki
Ei
i l d ki 22,3-DPG
3 DPG artışı
Co2
Hb-O2 Dissosiasyon eğrisini sola kaydıran nedenler ;
Hb-O2 Dissosiasyon eğrisini sağa kaydıran nedenlerin tersi
durumları ve Fötal hemoglobin artışı
2,3-Bisfosfogliseratın, hemoglobinin oksijene ilgisi
üzerine
i etkisi:
ki i
2,3-Bisfosfogliserat (2,3-BPG) oksijenin hemoglobine
bağlanmasında
önemli
bir
düzenleyicidir.
Konsantrasyonunun kabaca hemoglobine eşit olduğu
alyuvarlarda miktarca en fazla bulunan organik fosfattır.
fosfattır 2,323
BPG glikoliz yolundaki bir ara üründen sentezlenir.
2,3-BPG deoksihemoglobine bağlanıp oksihemoglobine
bağlanmayarak hemoglobinin oksijene ilgisini azaltır.
Hemoglobinler
Hemoglobin A2 (HBA2): HbA2 normal erişkin
hemoglobinin doğumdan yaklaşık 12 hafta sonra ortaya
çıkan ve toplam hemoglobinin yaklaşık %2’sini
oluşturan
l
minör
i ö bir
bi bileşenidir.
bil
idi İki α- globin
l bi ve iki δ –
globin zincirinden meydana gelir.( normal erişkin
hemoglobinleri)
Hemoglobin
H
l bi A1c:
A1 Fizyolojik
Fi l jik şartlarda
tl d HbA yavaş ve
nonenzimatik olarak glikozillenir. Glikozillenmiş
hemoglobinlerin en sık rastlanan formu HbA1c dır.
dır
Glukoz kalıntıları esas olarak β- globülin zincirlerinin
N- terminal valinlerin NH2 ggruplarına
p
bağlı
ğ olarak
bulunur. HbA1c miktarlarındaki artış diabetes
mellitus hastalarında görülür.