MADDENİN HALLERİ
Boşlukta yer kaplayan, kütlesi ve eylemsizliği olan her
şey maddedir. Oturduğumuz sıralardan, yediğimiz
yiyeceklere ,dev yıldızlardan gezegenlere,
kullandığımız basit aletlerden bilgisayarlara,tek
hücreli canlılardan karmaşık yapılı canlılara,gözümüzle
görebildiğimiz bütün nesnelerden
göremediğimiz,atmosferdeki gazlara kadar her şey
maddedir. Yani kısaca uzayda yer kaplayan ve
kütlesi, hacmi, eylemsizliği olan duyu organlarımızla
algılayabildiğimiz her şeye madde denir.
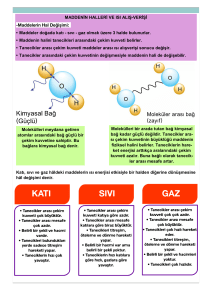
Maddenin katı, sıvı, gaz ve plazma olmak üzere dört hali vardır.
MADDENİN HALLERİ
KATI
SIVI
GAZ
PLAZMA
1. KATI HALİ
YEMEK TUZU ( NaCl )
ÇİNKO ( Zn )
GÖZ TAŞI ( CuSO4 )
Belirli bir şekli olan ve bu şeklin ortamlara göre değişmediği hale
katı hal denir.
Genel Özellikleri :
Katı halinde atomlar ve moleküller
birbirine oldukça yakındır.
Maddenin en düzenli (karalı ) halidir.
Tanecikler arasındaki çekim kuvveti
en fazladır.
Hacimleri ve şekilleri bellidir.
Sıkıştırılamazlar.
Akışkan değildir.
Tanecikler bulundukları yerde titreşim
hareketi yaparlar.
Fiziksel yollarla diğer üç hal olan sıvı,
gaz ve plazmaya dönüştürülebilirler.
2. SIVI HALİ
MEYVE SUYU
SU
SÜT
COLA
Maddenin bulundukları kabın şeklini alan haline sıvı hali denir.
Genel Özellikleri :
Kabın doldurduğu kısmın şeklini ve hacmini
alırlar.
Belirli bir şekilleri ve hacimleri yoktur.
Katılara göre daha düzensizdirler.
Akışkandır.
Sıvı tanecikleri birbiri üzerinde kayarak hareket
ederler.
Öteleme hareketi yaparlar.
Tanecikler arası boşluk fazladır.
Üzerine uygulanan basıncı her yöne aynen iletir.
Akmaya karşı direnç gösterirler.Buna viskozite
denir.
Açık kapta buharlaşırlar.
Yüzey gerilimleri vardır.Sıcaklık arttığında
hacimleri az da olsa artar.Böylelikle yoğunlukları
azalır.
Birbirleri içinde çözünebilen iki sıvı
karıştırıldığında birbirleri içinde yayılırlar.
Sıkıştırılamazlar.
3. GAZ HALİ
Boş bir kaba konulan bir madde o kabın her noktasına
yayılabiliyorsa bu haline gaz hali denir.
GENEL ÖZELLİKLERİ
Tanecikler arasında çekim yok denecek
kadar azdır.
Akışkandır.
Tanecikler arasında çok büyük boşluklar
vardır.Daima hareket halindedirler.
Maddenin en düzensiz halidir.
Belirli bir şekilleri ve hacimleri yoktur.
Bulundukları kabı doldururlar ve kabın her
yerine homojen olarak yayılırlar.
Sıkıştırılabilirler.
Sonsuz yayılma özelliğine sahiptir.
4. PLAZMA HALİ
KUTUP IŞIKLARI
Maddenin dördüncü hali plazmada ;
İyonlaşmış gaz
Elektronlar ve protonlar
Yüksüz atomlar ve moleküller
Uyarılmış atomlar
bulunur.
Normal bir gazla plazma arasındaki temel fark,
gazların yalnızca elektriksel olarak olarak nötr atom
veya moleküllerden oluşmasıdır.. Plazmada ise nötr
parçacıkların yanı sıra özgür elektron ve iyonlar da
bulunur. Burada özellikle içerisinde bulunan plazma ile
maddenin dördüncü hali olan plazma
karıştırılmamalıdır.
Plazma ortamında plazma titreşimleri ve plazma
dalgaları oldukça sık görülür. Normal gazda yalnızca
ses dalgaları üretilebilir.
GENEL ÖZELLİKLERİ
İyi bir iletkendir. Elektriği
ve ısıyı iletir.
Elektrik ve manyetik alanla
etkileşir.
Kimyasal reaksiyonları çok
hızlıdır.
Yüksek sıcaklık ve enerji
yoğunluğuna sahiptir.
HAL DEĞİŞİM OLAYLARI VE ISI
Sıcak bir cisimden soğuk bir cisme aktarılan enerjiye ısı
denir,yani ısı sıcaklık farkından ileri gelen enerjidir.
Erime ve Donma
• ERİME (ERGİME) : Katı maddeler
ısıtıldıklarında sıcaklıkları artar ve bir
noktaya gelindiğinde hal değiştirerek sıvı
hale geçerler. Bu olaya yani maddelerin
ergime sıcaklığında katı halden sıvı hale
geçmesine erime (ergime) denir. Erimenin
olduğu sıcaklığa da erime noktası denir.
• DONMA : Bir sıvının katıya dönüşmesine donma denir. Donmanın
olduğu sıcaklığa da donma noktası denir.
Saf maddeler için ,
Erime noktası = Donma noktası
Buharlaşma ve Yoğuşma
•
BUHARLAŞMA : Sıvıyı oluşturan tanecikler katılara
oranla birbirlerine daha uzak ve yapılarını oluşturan
tanecikler arasındaki çekim kuvvetleri daha zayıftır. Sıvıyı
buharlaştırmak (gaz hale getirmek) için tanecikleri
arasındaki çekim kuvvetlerini yenmek amacıyla enerji
vermek gerekir. Yeterli enerji ile tanecikler sıvı
yüzeyinden kurtularak gaz haline geçerler. Bu olaya
buharlaşma denir.
• YOĞUŞMA : Kaynayan suyun üzerine kapak
kapattığımızda kapakta su damlacıkları oluşur. Bu su
damlacıkları kaynama sırasında oluşan buharının tekrar
sıvı hale geçtiğini gösterir. Bir gaz ya da buharın sıvıya
dönüşmesine yoğuşma denir. Buhar sıvıya dönüşürken ısı
verir.
Süblimleşme
Maddenin katı halden sıvı hale dönüşmeden gaz hale
dönüşmesine süblimleşme denir. Katıdan gaz hale geçerken
madde ısı alır. Süblimleşmenin tersine maddenin gaz halden
doğrudan katı hale geçmesine geri süblimleşme denir. Su
moleküllerinin geri süblimleşmesine kırağılaşma denir.
KIRAĞILAŞMA
HAL DEĞİŞİM ISISI (L) : Maddenin 1 gramının bir halden
başka bir hale geçmesi sırasındaki ısı değişimidir. Hal değişim
ısısı madde eriyorsa, erime gizli ısı (Le) , madde buharlaşıyorsa
buharlaşma gizli ısısı (Lb) şeklinde ifade edilir. Erime
sıcaklığındaki bir mol katının erimesi için gerekli ısı molar erime
ısısı, kaynama noktasındaki bir mol sıvının buharlaşması için
gerekli ısı molar buharlaşma ısısıdır.
KÜTLE (m) : Hal değişimine uğrayan maddenin kütlesidir.
Birimi gram (g) ’ dır.
ÖZ ISI (c) : Bir maddenin 1 gramının sıcaklığını 1 santigrat
derece artırmak için gereken ısı miktarıdır. Birimi joule / gram
derece celcius ’ tur .
SICAKLIK FARKI : Son sıcaklık ile ilk sıcaklık arasındaki
farktır. Sıcaklık birimi celcius ’ tur.