Protein Analiz Yöntemleri
ve Proteomik
• Proteinler hücredeki tüm süreçlerde işlevseldir.
•22 farklı amino asitten oluşurlar
ve böylece hücreler,
dokular ve bireyler arasında çeşitliliği sağlarlar.
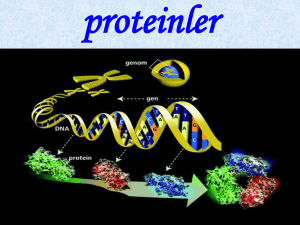
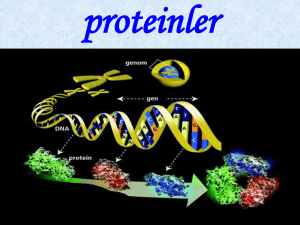
DNA
mRNA
Protein
Genom
Transkriptom
Proteom
•Hücrenin yaşamını sürdürebilmesi için sahip olduğu DNA bilgisini
protein ürününe dönüştürmesi gerekir.
• Proteom: Organizmanın tüm protein içeriğidir. Çevresel koşullardan
etkilenir ve değişkenlik gösterir.
Protein Karışımı
Ayırım
2D-PAGE
Proteinler
MALDI-TOF
Spot
Kesimi
Peptitler
Tripsin ile muamele
Peptit kütle
parmakizi
Veritabanı
Araştırmaları
ESI-MS/MS
Tandem
MS
Spektrumu
Proteinlerin
Tanımlanması ve
post translasyonal
modifikasyonlar
2D-Jel Temelli Yaklaşım
Kesim
Protein
karışımı
Peptit Karışımı
Ayırım
Peptitler
MS-MS
μHPLC, 2D-LC,
AffiniteKromatografisi
Ayırım 2D- HPLC
Veritabanı
araştırmaları
Peptit fraksiyonları
Protein
Tripsin uygulaması
fraksiyonları
Jel Temelli Olmayan Yaklaşım
LC-MS/MS
Tandem
MS
spektrum
Proteinlerin
Tanımlanması
2D Gel Software
Protein analizi için kullanılan yöntemler:
•Elektroforez
•Kromatografi
•Protein parmakizi
•ELISA “Enzyme-linked immunosorbent assay”
•X-Işını Kristalografisi
•Nüklear Manyetik Rezonans (NMR)
•Kütle spektrometresi (Mass spectrometry, MS)
•Protein mikroarray
Kromatografik Yöntemler
İnce Tabaka Kromatografisi
•Proteinlerin çözünme yeteneklerine göre ayrışım yapılır.
•Katı bir yüzeye (selüloz) emdirilen
örnek çözücü yüzey içine
yerleştirilir. Çözücü solüsyonun yüzeyde ilerlemesiyle, örnekteki
proteinler çözünme yeteneklerine göre ayrılırlar.
Kolon Kromatografisi
• Porlu katı bir yüzeyden geçirilen proteinler, yüzeyle olan
etkileşimlerine göre ayrılırlar.
– İyon değişim kromatografisi: Proteinlerin iyonik yüklerine göre
– Afinite kromatografisi: Proteinlerin kimyasal gruplara bağlanma
özelliklerine göre
– Jel filtrasyon kromatografisi: Proteinlerin büyüklüklerine göre
Kolon kromatografisi çeşitleri
Yüksek Basınç Sıvı Kromatografisi (HPLC)
Proteinlere çok daha kuvvetli bağlanan yüzeye yüksek basınç
uygulanarak proteinlerin yüzeyden çok daha hızlı geçmesi sağlanır.
Yüksek Basınç Sıvı Kromatografisi (HPLC)
• HPLC’nin en önemli üstünlüğü ayırma gücü, duyarlılığı ve
geri kazanımın yüksek, hızlı bir yöntem olmasıdır. Bu
yöntemde hareketli faz 10-400 atm. basınç altında
kolondan 0.1-5 cm/s gibi yüksek bir hızla geçirilir.
Bunun sonucu ayırma hızı çok daha düşük olan ve
hidrostatik
basınçla
çalışan
açık
sıvı
kolon
kromotografisine göre çok daha yüksek olur. Böylece
günler süren bir ayırma işlemi HPLC’de birkaç saatte
tamamlanabilir. Bu yöntem saflaştırmanın yanı sıra
protein çözeltilerinin tuzunu gidermek amacıyla da
kullanılabilir.
Protein Parmakizi Yöntemi
• Protein
yapısı
bozularak
çeşitli
boylarda peptidler oluşturulur (Tripsin +
siyanojen bromür).
•Jel elektroforezi veya kromatografik
yöntemlerle protein parmakizi çıkarılır.
ELISA Yöntemi
•“ELISA plate” antikor ile kaplanır. Antijen miktarı belirlenecek olan
örnek kuyulara yüklenir. Antijen ile antikorun bağlanması beklenir.
•Bağlanmamış veya özgün olmayan proteinler yıkama ile uzaklaştırılır.
•Enzim bağlı ikincil antikorlar eklenir ve bunlarda antijen-antikor
yapısına bağlanır (sandviç yapısı).
•Enzimle etkileşecek substrat eklenerek oluşan ışıma ile protein miktarı
spektrofotometrik olarak ölçülür.
X-Işını Kristalografisi (proteinlerin üç boyutlu
yapısını araştırmada kullanılır)
• X-ışınlarının
dalga
boyları
küçük
olduğundan moleküllerdeki atomlar arası
boşlukları araştırmada kullanılabilir.
• Bir solüsyon içinde hazırlanan kristaller
aynı
maddenin
düzenli
tekrarıyla
oluşurlar. Kristallere gönderilen X-ışını
kırınımlarının filme yansımasıyla pek
çok molekülün yapısı tayin edilebilir.
• Filme yansıyan noktaların şekli kristal
içindeki molekül yapısını gösterir.
Maurice Wilkins ve Rosalind Franklin tarafından incelenen
DNA X-ışını Kristalografisi ve DNA modeli
X-Işını Kristalografisi
• Buna göre proteinin içerebileceği α sarmal ve
β tabaka motifleri belirlenebilir.
• Protein içi kimyasal bağlar hakkında bilgi
edinilebilir.
• Tüm verilerin toplanmasıyla proteinin üç
boyutlu yapısı anlaşılabilir.
• Bazı proteinlerin kristalize olmaması bu
yöntemin kullanımını kısıtlar.
NMR Spektroskopisi (proteinlerin üç boyutlu
yapısını araştırmada kullanılır)
• NMR için yüksek saflıkta
protein örneği kullanılır.
• Doğal veya rekombinant
proteinler için uygulanabilir.
• Küçük proteinlerin (35kDa) yapı
analizi için uygundur.
NMR örnek tüpü
Yüksek manyetik alana (800MHz) sahip bir NMR spektrometresi
NMR Spektroskopisi
• Elektromanyetik bir alana konulan yüklü bir çekirdek α (düşük
enerjili pozisyon) ve β olmak üzere iki şekilde hareket edebilir.
• NMR spektrometresi çekirdeğin α dönüşünden β dönüşüne
(düşük enerji seviyesinden yüksek enerji seviyesine ) geçmesi
için gereken elektromanyetik radyasyonun frekansını ölçer.
• Bu değer kullanılan çekirdek tipine (1H,
13C, 15N)
göre değişir.
• Deney sonucunda alınan değer ile teoride olması gereken değer
arasında fark vardır ve bu fark bize çekirdeğin çevresindeki
elektron yoğunluğu hakkında bilgi verir.
• Böylece çekirdeğin ilişkide olduğu veya çevresindeki atomlar
belirlenebilir.
Dengedeki
Örnek
uyarılma
gevşeme
Uyarılma
durumu
Gözlem
Spektrum
NMR Spektroskopisi
• Kimyasal olarak indüklenmiş dinamik nuklear
polarizasyon (CIDNP): Proteinlerin gerçek zamanlı
katlanmalarıyla yapılarındaki değişimleri takip etmeyi
sağlayan bir NMR yöntemidir.
Olumlu ve Olumsuz Yönleri
• NMR kristal oluşumu gerektirmediği için kimi durumlarda üstünlük
sağlayabilir.Ancak büyük proteinlerde NMR yöntemi verimli sonuç
vermez.
• Büyük moleküllerin NMR spektroskopisinde piklerin çakışması sorunu
isotopik etiketleme ve çok boyutlu deneyler ile aşılmıştır.
• Büyük moleküllerin analizi ile ilgili diğer bir sorun ise mıknatıslanmanın
daha hızlı gevşemesidir.
• Pikler daha geniş, güçsüz ve sonuçta görünmez olur.
• Bu durum daha kısa sürede sinyal yakalanmasını gerektirir.
• Bu gevşemeyi azaltmak için “Transverse relaxation optimized
spektroscopy (TROSY)” yöntemi geliştirilmiştir.
Kütle Spektrometresi (MS)
•Kütle spektrometresi “Mass spectrometry” MS, bir örnekteki iyonik
maddeleri kütle farklılıklarına göre ayrırır.
• Kütle spektrometresi 3 kısımdan oluşur.
•İyon kaynağı
•Kütle analizörü
•Detektör sistem
Kütle Spektrometresi (MS)
• Aşamalar:
– Örneklerden iyonların
elde edilmesi
– Farklı kütlelerdeki
iyonların ayrışımı
– Kütle spektrumunun
oluşması için verilerin
biriktirilmesi
Protein analizinde “top-down” stratejisi:
• Kütle spektrometresinde proteinlerin
iyonizasyonu için kullanılan iki yöntem vardır.
– Elektrospray iyonizasyonu (ESI)
– “Matrix-assisted laser desorption/ionization”
(MALDI)
• Proteinler öncelikle bu yöntemlerden biriyle
iyonize edilir ve daha sonra bir kütle
analizörüne girer.
MALDI-ToF
Timed ion selector
Laser
Sample
plate
+
+
+
+
Reflector
+
+ +
Flight tube
Accelerating
field
Detectors
Protein analizinde “bottom-up” stratejisi:
• Proteinler elektroforetik ayrışımdan sonra enzimatik
olarak kesilir (tripsin veya pepsin) ve daha küçük
peptidler oluşur.
• Biriken peptid ürünleri daha sonra kütle analizörüne
girer.
• Bu yönteme peptid kütle parmakizi (PMF) denir.
Kütle Spektrometresi (MS)
• “Time-of-flight” (TOF) analizöründe iyonları
hızlandırmak için elektrik alan kullanılır ve sonra
iyonların dedektöre ulaşmasıyla ölçüm alınır.
• İyonların dedektörde toplanma süreleri (“Time-offlight”) iyonik yükleri ile doğru; molekül ağırlıkları ile
ters orantılıdır. Yani daha hafif iyonlar dedektöre
daha hızlı ulaşır.
Protein Mikroarray
• Protein moleküllerinin, belli bir düzende cam bir yüzeye
bağlanmalarıyla oluşturulur.
• Kullanım alanları
–
–
–
–
proteinlerin varlığının ve miktarının belirlenmesi
protein-protein etkileşimi
protein-nükleik asit etkileşimi
enzimlerin substratlarının bulunması