25.01.2007 tarihinde yayınlanan tebliğ değişikliklerini gösteren bölümler mavi ile
gösterilmiştir.
01.03.2007 tarihinde yayınlanan ve 06.03.2007 tarihinde yürürlüğe giren değişikliklikler
ise kırmızı ile gösterilmiştir.
11. Reçetelerin Düzenlenmesi ve İlaç Kullanım İlkeleri
11.1. Ayakta veya Evde Tedavilerde Reçetelerin Düzenlenmesi
Ayakta veya evde tedavi sırasında gerekli görülen ilaçlar için sağlık karnelerinde
bulunan kendinden kopyalı reçeteler kullanılacaktır. (Sosyal Güvenlik Kurumlarının bu
konudaki özel uygulamaları saklıdır)
11.2. Yatarak Tedavilerde Reçetelerin Düzenlenmesi
Yatarak tedavilerde hastanede kullanılan ilaçların hastane eczanelerinden temini zorunludur.
Dışardan alınması gereken ilaçlar, hak sahiplerinin sağlık karnelerine, üzerinde yer alan
bilgiler tam ve eksiksiz olarak kendinden kopyalı reçetelere yazılacak, “ECZANEMİZDE
YOKTUR, YATAN HASTA” kaşesi vurularak başhekimlik tarafından onaylanacaktır.
Hastanelerde bu şekilde düzenlenen reçeteler beş günlük maksimum tedavi dozunu
geçemeyecektir. Bilahare ilacın hastane eczanesince temin edilememesi ve tedavinin devam
ettiği durumlarda “doz” bitiminde yeniden reçete yazılması mümkündür.
Yukarıda belirtilen esaslara göre, hastanelerde yatan hastalar için düzenlenen reçete
muhteviyatı ilaçların, rasyonel kullanımını sağlamak amacıyla, eczanelerden dönüşümlü
olarak temini hususunda, hastaneler, Türk Eczacıları Birliği Merkez Heyeti ile işbirliği
yapabilir. Bu uygulamaya ilişkin usul ve esaslar, Maliye Bakanlığı, Sağlık Bakanlığı ve
Çalışma ve Sosyal Güvenlik Bakanlığı ile Türk Eczacıları Birliği Merkez Heyeti tarafından
müştereken belirlenir.
Yatan hastalar taburcu edilirken idame tedavileri için reçete edilen ilaçlar, SSK hastanelerinin
Sağlık Bakanlığına devri nedeniyle hastane stoklarında kayıtlı ve üzerlerinde “SSK
MALIDIR SATILAMAZ” veya “SSK’DAN DEVİR İLAÇTIR” ibaresi bulunan ilaçlarla
sınırlı olmak üzere, hastane eczanesinden verilebilir ve hastanın kurumuna tedavisine ait diğer
işlemlerle birlikte fatura edilir. Bu ilaçlar SSK mensubu hastalara verildiği takdirde provizyon
sistemine girilir. Hasta katılım payı peşin alınan hak sahiplerinden, hastane tarafından tahsil
edilir, maaşından kesilen hak sahipleri için ise kurumlarınca ilgili hastanelere ödenir. Bu
uygulamada, Tebliğ’de belirtilen reçete yazım kuralları ile indirim oranları dikkate alınır.
Ayrıca, SSK ilaç ve tıbbi malzeme sanayi müessesesinde üretilmiş olan ilaçlar,
miadları içerisinde Sağlık Bakanlığı sağlık tesislerinde SSK sigortalısının ayaktan/yatarak
tedavilerinde kurum mevzuatı doğrultusunda verilir.
12. Reçete Yazımı, Rapor Düzenlenmesi ve İlaç Kullanım İlkeleri
İlaç kullanımında ve rapor düzenlenmesinde aşağıda belirtilen hususlar temel alınacaktır.
a) Tüm reçetelere mutlaka teşhis yazılacaktır. Ayaktan hastalar için yazılan reçetelerde,
reçeteyi yazan hekimin imza ve kaşesi bulunacak (kaşede kurumun adı, hekimin ana uzmanlık
dalı ile birlikte var ise yan uzmanlık dalı ve diploma numarası mutlaka yer alacaktır) ayrıca,
kurum başhekiminin onayı ve mühür aranmayacaktır. Teşhisi yazılmayan, ilgili hekimin imza
ve kaşesi bulunmayan reçeteler resmi ve özel eczaneler tarafından kabul edilmeyecektir.
Üniversite hastaneleri ile eğitim ve araştırma hastanelerinde ihtisas yapan asistanlar, eğitim
aldıkları branş uzman hekiminin yazması gereken ilaçlar ile Tebliğ’de uzman hekimlerce
yazılabileceği belirtilen ilaçları yazabilir. Herhangi bir uzman hekim tarafından reçete
edilebilen tüm ilaçlar, aynı uzmanlık eğitimi üzerine yan dal uzmanlığı yapmış olan
hekimlerce de reçete edilebilecektir. Aile hekimliği yapan hekimler, aile hekimliği uzmanının
yazabildiği tüm ilaçları reçete edebilirler.
b) Sağlık Kurulu raporlarından, aslına sadık kalmak kaydıyla Tebliğ hükümlerine göre
eksikliği bulunan raporlar (doz, ilaç yazılım kurallarına ait tıbbi bilgiler) raporun çıktığı
hastanede raporu düzenleyen ilgili dal uzmanı tarafından kaşeli ve imzalı düzeltmesi ve bunun
Başhekimlik tarafından onaylanmak koşuluyla süresinin sonuna kadar geçerlidir. Raporlarda
yapılan düzeltmeler düzeltme tarihinden itibaren geçerlidir.
12.1. Reçetelere Yazılabilecek İlaç Miktarı
Ayaktan yapılan tedavilerde aşağıda 12.4 üncü maddede belirtilen durumlar dışında; bir
reçetede en fazla dört kalem ilaç ve her kalem ilaçtan bir kutunun (Parenteral ve topikal
formları hariç) bedeli ödenir.
Tetrasiklinler (doksisiklin ve tetrasiklin)(Doksin, Monodoks, Tetra kapsül ve Tetra,
Tetralet, Tetramine kapsül), Amfenikoller (kloramfenikol ve tiamfenikol) (Armisetin
kapsül,süspansiyon;Kemicetine kapsül,süspansiyon; Tiofen tablet, Urfamycin kapsül ve
süspansiyon) , Ampisilin (kombine preparatlar hariç) (Alfasilin, Ampisina, Silina tablet ve
süspansiyon) , Amoksisilin (kombine preparatlar hariç) ( Alfoxil , Largopen, Remoxil,
Demoksil tablet ve süspansiyon, fenoksimetil penisilin ( Cliacil,Pen-Os tablet ve süsp.)
Eritromisin (Eritro tablet, Erythrocin tablet ve süspansiyon), klindamisin (Cleocin,Klindan
kapsül ve süspansiyon) , sülfonamid ve trimetoprim kombinasyonlarını (Bactrim, Bakton,
Kemoprim, Metoprim, Trimoks tablet ve süsp.) içeren antibiyotikler on güne kadar tedaviyi
sağlayacak miktarda reçete edildiğinde ödenecektir.
İlacın enjektabl formlarının reçeteye yazılması durumunda, en fazla beş günlük tedavi
dozuna uygun olacak şekilde olan ambalajının ödemesi yapılır.
Reçetede mutlak surette günlük kullanım dozu belirtilecektir.
“Aynı eşdeğer gruptaki ilaçların piyasadaki en küçük ambalaj formlarından bir tanesinin bir
kutu olarak verilmesi uygulamasına en geç 01/01/2007 tarihinde geçilecektir. Geçiş süreci, bu
tebliğin yayım tarihinden itibaren, Sağlık Bakanlığınca ilaç veya ilaç grupları için en az 15
gün önceden genelge ile duyuru yapılmak kaydıyla, 01/01/2007 tarihine kadar
tamamlanacaktır.” (03.10.2006 tarih 26308 sayılı Resmi Gazete’ de yayımlanan Tedavi
Yardımına İlişkin Uygulama Tebliği Sıra no:10’ da yayımlanan şekli ile.)
a)İlacın reçete edilmesindeki özel düzenlemeler saklı kalmak kaydıyla, Hasta Katılım
Payından Muaf İlaçlar listesinde (EK–2) yer almamakla birlikte, uzun süreli kullanımı sağlık
kurulu raporu ile belgelendirilen ilaçlarda (hasta katılım payı alınmak kaydıyla), tüm
hekimlerce,
b)Menopoz (Kadın hastalıkları ve doğum, iç hastalıkları, ortopedi, fizik tedavi ve
rehabilitasyon ve aile hekimi uzmanları tarafından ve sağlık kurulu raporuna istinaden tüm
hekimlerce) ve disfonksiyonel uterin kanamalarda (kadın hastalıkları ve doğum ve aile
hekimliği uzmanı tarafından ve sağlık kurulu raporuna istinaden tüm hekimlerce) rapor
aranmaksızın,
en fazla üç aylık tedavi dozu yazılabilir.
c) 1.Yanık tedavilerinde, anemilerde, reflüde ve GIS ülserlerinde,
2. Yalnız dermatoloji uzmanlarınca reçete edilebilen oral retinoidlerde (izotretionin,
asitretin),
3. Yatış sonrasında taburcu edilen hastaların idame tedavisi için düzenlenen reçetelere,
hekim tarafından tedavi süresi belirtilmek kaydıyla,
en fazla bir aylık dozda ilaç yazılabilir.
Yatarak tedavi edilen hastalar için gerekli olan ve hastane eczanesinde bulunmayan ilaçlar en
fazla beş günlük tedavi dozunu geçmeyecek şekilde reçeteye yazılabilir. Bu reçetelerde
mutlak surette günlük tedavi dozu da yazılacak, beş günlük tedavi dozunu aşan ilaç eczane
tarafından kesinlikle verilmeyecektir. Ancak, sağlık kurumlarında uzun süre yatarak tedavi
gören tüberküloz hastalarına, kullanım dozu belgelenmek kaydıyla l aylık miktarda tüberküloz
ilaçları yazılabilir.
Bir ilacın Sağlık Bakanlığınca izin verilen endikasyon ve kullanım dozu dışında kullanımı
ancak Sağlık Bakanlığınca verilen onayla mümkün olacaktır.
12.2. Hasta Katılım Payından Muaf İlaçlar
Bu Tebliğ’e ekli Hasta Katılım Payından Muaf İlaçlar Listesinde (EK–2) yer alan
hastalıklarda kullanılacak ilaçlar sağlık kurulu raporuna istinaden en fazla 3 aylık miktarda
yazılabilecektir.
Hasta Katılım Payından Muaf İlaçlar Listesinde (EK–2) bulunan hastalıklarda rapora
istinaden bir reçetede 4 kalem sınırlaması bulunmamaktadır.
a) İlacın reçete edilmesindeki özel düzenlemeler (Tebliğin 12.7 bölümü ve EK-2/C
hükümleri) saklı kalmak kaydıyla, Hasta Katılım Payından Muaf İlaçlar Listesinde (EK–2)
yer alan ilaçlar, ilacın reçete edilme koşulunda belirtilmiş olan uzman hekimlerden birinin yer
aldığı sağlık kurulu raporuna dayanılarak reçete tekrarında diğer hekimlerce de
yazılabilecektir.
b) Ayaktan yapılan I.V.P. ve HSG tetkiklerinde kullanılacak non-iyonik radyo-opak
maddelerden 50 ml.lik bir kutu kullanılması halinde yalnızca tetkiki isteyen uzman hekim
veya radyoloji uzmanı tarafından reçete düzenlenecek, reçeteye radyo-opak madde ve
yapılacak tetkikin ne olduğu açıkça yazılacaktır. 50 ml.yi aşan dozda non-iyonik radyo-opak
madde kullanılması halinde ise ayrıca kullanılma gerekçesi reçeteye yazılacaktır.
c) Ayaktan yapılacak radyolojik tetkikler için kullanılacak tüm iyonik ve non-iyonik radyoopak maddelerden katkı payı alınmayacaktır. Reçeteye ön tanı ve istenilen tetkik, ilgili hekim
tarafından yazılıp imzalanacaktır.
Tedavi için yurtdışından getirtilecek ilaçlar, reçeteye sağlık kurulu raporuna dayanılarak
uzman hekim veya ilgili uzman hekim tarafından 3 aylık doza kadar yazılabilecektir. Onkoloji
ilaçları en fazla 3 aydaki kür sayısı kadar dozda getirtilebilecektir.
12.3. Hastanede Yatan Hastalarda Kullanılabilecek İlaçlar
Bu Tebliğe ekli (EK–2/B) sayılı listede yazılan anestezikler ve ilaçların bedelleri,
sadece hastanede yatan hastalarda ve/veya tedavisi klinik şartlarında yapılabilen hastalarda
kullanımı halinde ödenecektir.
Listede yer alan ilaçların kullanımı için reçeteler bu Tebliğin 11.2 nci bölümündeki
esas ve usullere uyularak düzenlenecektir. Bu ilaçların ayakta tedavilerde reçetelere yazılması
durumunda ödeme yapılmayacaktır.
Sağlık kurulu raporu ile tevsik edilen ve sürekli periton diyalizi tedavisinde kullanılması
zorunlu görülen diyaliz solüsyonu ile sarf malzemeleri ayakta tedavide de yazılabilir.
12.4. Ayakta Tedavide Kullanımı Sağlık Kurulu Raporuna Bağlı İlaçlar
Bu Tebliğ’e ekli (EK–2/C) sayılı listede yer alan ilaçların, ayakta tedavilerde kullanımı
durumunda reçetelere yazımı sağlık kurulu raporuna bağlıdır. Bu sağlık kurulu raporu,
hastanın adı, teşhis (kısaltma yapılmadan), etken madde adı ve dozu, uygulama planı ve
süresi ile hastayı tedavi eden birimin ve uzman hekimin adını da ayrıca kapsayacaktır.
Preparatın maksimum dozu belirtilerek maksimum dozu aşmamak kaydıyla düzenlenen rapor
tedavi süresi boyunca geçerlidir. Bu süre her hal ve takdirde iki yılı geçemez.
Yukarıda belirtilen listede yer almakla birlikte (EK–2) sayılı Hasta Katılım
Payından Muaf İlaçlar Listesinde yer almayan ilaçlardan hasta katılım payı alınacak, (EK–2)
liste kapsamında olanlardan ise sağlık kurulu raporunda belirtilmesi kaydıyla hasta katılım
payı alınmayacaktır.
12.5. Bedeli Ödenecek İlaçlar
Kurum ve kuruluşlarca bedeli ödenecek olan ilaçlar bu Tebliğ’e ekli Bedeli Ödenecek İlaçlar
Listesinde (EK–2/D) belirtilmiştir. Bu listede ticari isimleri ve barkod numaraları ile birlikte
yer alan ilaçlar dışındakilerin bedelleri, reçeteye yazılsa dahi kurumlarca hiçbir şekilde
ödenmeyecektir.
Bedeli Ödenecek İlaçlar Listesinde (EK–2/D) yer alacak veya bu listeden çıkarılacak ilaçların
saptanmasına ilişkin değerlendirmeler, 14/02/2004 tarih ve 25373 sayılı Resmi Gazetede
yayımlanan, 06/02/2004 tarih ve 2004/6781 sayılı Bakanlar Kurulu Kararı ile oluşturulan
“Geri Ödeme Komisyonu” tarafından yapılır. Etken maddesi geri ödeme listesinde olan bir
ilacın eşdeğeri olanlar en ucuz eşdeğerinin altında fiyat taşıması halinde “Geri Ödeme
Komisyonu” tarafından ivedilikle değerlendirilir. Geri ödeme komisyonunun çalışma usul ve
esaslarına ilişkin karar Maliye Bakanlığının web sayfasında duyurulmuştur.
12.6. İntravenöz İlaç Tedavisi
Üniversite hastaneleri ve eğitim hastaneleri ile Sağlık Bakanlığınca uygun görülen
resmi ve özel hastanelerde,
a) Kanser, kronik osteomiyelit, infektif endokardit vb. hastalıklarda ve/veya,
b) Kan ürünleri ile damar yoluyla kullanılan antibiyotikler gibi ürün ve ilaçların
kullanımı,
gereken hallerde hastanın hastaneye yatışı yapılmadan intravenöz tedavi/kemoterapi
uygulanabilir. Bu uygulama için tedavide kullanılacak ilaçlar ve sarf malzemelerinin tedaviyi
yapan sağlık kurumu tarafından temin edilmesi halinde ilgili kuruma fatura edilir ve
provizyon sistemine girilir.
Uzun süreli intravenöz ilaç tedavisi (kemoterapi vb) uygulamaları sonucunda hasta
adına düzenlenecek faturaya, hastalığın adını, uygulanan tedavi planını, verilen ilacın günlük
dozunu ve miktarını belirten ve ilgili uzman hekimin imzası ile başhekimin onayını içeren
tedavi planı eklenmesi gerekmektedir.
12.7. Bazı Özel Hastalıklara ve İlaç kullanımına İlişkin Düzenlemeler
12.7.1. Altın Preparatları, Biyolojik Ajanlar, Leflunomid ve Subkütan Metotreksat
Kullanım İlkeleri
a) Altın preparatları kullanımından önce diğer antiromatizmal ilaçlar ile tedavi yapılacaktır.
Bu tedaviye cevap alınamaması durumunda ve tedavinin devamı gerektiğinde; yapılan
tedaviden alınan sonuçlar, tedavinin ne kadar süredir devam ettiği, ilacın adı, dozu ve
kullanım süresi ile ayrıntılı tedavi şemasını belirten sağlık kurulu raporu düzenlenecektir.
b) Romatolojide biyolojik ajanlardan Anti TNF ilaçların (infliksimab, etanarsept, adalimumab
gibi) kullanım ilkeleri; en az 2 farklı hastalık modifiye edici antiromatizmal ilacı, en az 3’er
ay olmak üzere kullanmış olmasına rağmen hastalık aktivitesinin kontrol altına alınamadığı
(Hastalık Aktivite Skoru DAS 28 > 5.1) veya yan etki nedeniyle bu ilaçların kullanılamadığı
resmi sağlık kurulu raporunda belirtilen romatoid artritli hastalarda, biri maksimum doz
indometazin olmak üzere en az 2 nonsteroid antiinflamatuar ilacı maksimum dozunda
kullanmasına rağmen yeterli cevap alınamayan veya yan etkileri nedeniyle bu ilaçların
kullanılamadığı aksiyel tutulumlu ankilozan spondilitli hastalarda, sulfasalazin veya
metotreksat kullanılmasına rağmen cevap alınamayan veya yan etkileri nedeniyle bu ilaçların
kullanılamadığı periferik eklem tutulumlu ankilozan spondilitli hastalarda (Bath Ankilozan
Spondilit Hastalık Aktivite İndeksi BASDAİ > 4, Visual Analog Skoru VAS 0-10cm),
Hastalık modifiye edici ajanlardan en az ikisi (tek tek veya kombinasyon şeklinde) standart
dozda en az altı ay kullanılmışsa ve yanıt alınmamışsa (bir ay arayla yapılmış iki ayrı
muayenede en az üç hassas eklem ve en az üç şiş eklem olması) veya toksisiteden dolayı altı
aydan daha kısa sürede yukarıdaki ilaçlar kesilmek zorunda kalmışsa psöriatik artrit
tedavisinde, Anti TNF ilaçlar kullanılabilecektir.
c) Bu maddenin (a) ve (b) bentlerinde belirtilen ilaçlar; üniversite hastaneleri ile eğitim ve araştırma
hastanelerinde fizik tedavi ve rehabilitasyon, erişkin ve pediatrik romatoloji ve immünoloji uzman
hekimlerinden biri tarafından düzenlenecek ilaç kullanım raporuna dayanılarak, bu uzman
hekimlerden biri veya iç hastalıkları uzman hekimi tarafından reçete edilebilir. İntravenöz formları,
mutlaka ilacın başlandığı üniversite hastaneleri ile eğitim ve araştırma hastanelerinde veya immünoloji
veya romatoloji veya fizik tedavi ve rehabilitasyon veya iç hastalıkları uzman hekiminin bulunduğu
sağlık tesisinde uygulanır. Subkütan formlarının ilk dozları ilacın başlandığı üniversite hastaneleri ile
eğitim ve araştırma hastanelerinde veya immünoloji veya romatoloji veya fizik tedavi ve
rehabilitasyon veya iç hastalıkları uzman hekiminin bulunduğu sağlık tesisinde hekim gözetiminde
yapılır, uygun enjeksiyon tekniği konusunda hastaya veya hasta yakınına eğitim verildikten sonra ilgili
uzman hekim uygun gördüğü ve ilaç kullanım raporunda “Mahallinde tedavisi sürdürülebilir”
ibaresine yer verdiği taktirde hastane dışında uygulanmak üzere iki aylık dozlar halinde reçete
edilebilir. Hastalar iki ayda bir üniversite hastaneleri ile eğitim ve araştırma hastanelerinde veya
immünoloji ve/veya romatoloji uzman hekiminin bulunduğu resmi sağlık tesisinde muayene edilecek,
ilk ilaç etkinliği iki ay sonunda değerlendirilecek, yeterli cevap alınamamışsa (Romatoid artrit için,
DAS 28’de 0.6 puandan, ankilozan spondilit için, BASDAİ’de 2 birimden daha az düzelme olması,
psöriatik artrit için, psöriatik artrit yanıt kriterlerine “PSARC” göre yanıt alınamaması durumunda)
ilaca devam edilmeyecektir.
Bu ürünler raporda belirtilmek koşuluyla, yukarıda belirtilen şartlarda kombine olarak da
kullanılabilir.”
d) Psoriyazis vulgariste üniversite hastaneleri ve eğitim ve araştırma hastanelerinde cilt
hastalıkları uzman hekiminin yer aldığı diğer hastalık modifiye edici ilaçlara dirençli
olduğunu, kullanılacak ilacın miktar ve süresini belirten sağlık kurulu raporuna dayanılarak
cilt hastalıkları uzman hekimlerince yazılabilecektir.
e) Crohn hastalığında; diğer tedavilere cevap vermeyen fistülize vakalarda hastalığın teşhisi,
kullanılan ilacın ismi, günlük kullanım dozu ve kullanım süresini belirten iç hastalıkları veya
genel cerrahi, uzmanlarının bulunduğu sağlık kurulu raporuna dayanılarak sağlık tesislerinde
klinik koşullarda uygulanacaktır. Bu grup ilaçlar sağlık kurulu raporuna dayanılarak iç
hastalıkları, genel cerrahi uzmanlarınca reçete edilir.
f) Leflunomid Kullanım İlkeleri; diğer hastalık modifiye edici ilaçlarla kontrol altına
alınamadığı veya bu ilaçlara kontrendikasyonu olduğu belgelenmiş romatoid artritli hastalarda
iç hastalıkları, romatoloji, immünoloji veya fizik tedavi ve rehabilitasyon uzman
hekimlerinden birinin yer aldığı sağlık kurulu raporu ile verilebilir. Tedavinin devamında
reçete bu uzman hekimler tarafından düzenlenir. Raporda tedavinin ne kadar süre devam
edeceği, ilacın adı, dozu ve kullanım süresi belirtilecektir.
g) Subkütan Metotreksat Kullanım İlkeleri; romatoid artrit tanısında fizik tedavi ve
rehabilitasyon, romatoloji veya immünoloji (erişkin veya pediatrik) uzman hekimlerinin en az
birinin bulunduğu resmi sağlık kurumlarında düzenlenecek sağlık kurulu raporuna
dayanılarak, tüm hekimlerce reçete edilebilecektir.
12.7.2. Antidepresanlar ve Antipsikotiklerin Kullanım İlkeleri
a) Trisiklik ve tetrasiklik antidepresanlar tüm hekimlerce yazılabilir.
Yeni nesil (SSRI, SNRI, SSRE, RIMA, NASSA gibi gruplara giren) antidepresanlar,
psikiyatri (erişkin ve çocuk), nöroloji (erişkin ve çocuk), üroloji, kadın hastalıkları ve doğum,
dahiliye fizik tedavi ve rehabilitasyon veya aile hekimliği (aile hekimliği yapan pratisyen
hekimler dahil) uzman hekimleri tarafından veya bu hekimlerden birinin çıkardığı ilaç
kullanım raporuna dayanılarak pratisyen hekimler dahil tarafından yazılacaktır. Yatan
hastalarda, yatışı yapan ilgili uzman hekim tarafından da tek kutu olarak reçete edilebilecektir.
b) Yeni nesil (atipik) antipsikotiklerin (klozapin, olanzapin, zotepine, risperidon, amisülpirid,
ketiapin, ziprosidon, aripiprazol) oral formları psikiyatri (erişkin ve çocuk) veya nöroloji
(erişkin ve çocuk) uzman hekimlerince, paranteral formları ise yalnızca psikiyatri (erişkin ve
çocuk) uzman hekimlerince yazılır.
Yeni nesil (Atipik) antipsikotikler, en az bir psikiyatri (erişkin ve çocuk) veya nöroloji
(erişkin ve çocuk) uzman hekiminin yer aldığı sağlık kurulu raporuna dayanılarak, diğer
hekimler tarafından da yazılabilir.
Yeni nesil (Atipik) antipsikotikler dışındaki antipsikotik ilaçlar diğer hekimlerce de
yukarıdaki kısıtlamalar olmaksızın yazılabilir.
Acil hallerde, acil servislerde yeni nesil (atipik) antipsikotiklerin parenteral formları (uzun
salınımlı/depo etkili formları hariç) tek doz olarak diğer hekimlerce klinik şartlarda
kullanılabilir.
Demansta, atipik antipsikotik ilaçlar, psikiyatri, nöroloji veya geriatri uzman hekimi
tarafından veya bu hekimlerden birinin bulunduğu resmi sağlık kurulu raporuna dayanılarak
diğer hekimlerce yazılacaktır.
c) Antidepresanlar ve antipsikotikler için düzenlenecek raporda, hastanın tedavisinde
kullanılacak ilaç veya ilaçların; etken madde ismi, günlük kullanım dozu, ilacın kullanılacağı
süre belirtilecektir. Bu süre bir yılı aşamayacaktır.
12.7.3. Aşı Uygulaması
Hayati önemi haiz olan zehirlenmelerde kullanılan antidotlar (panzehirler) hekim tarafından
hastanın reçetesine yazıldığında, sağlık kurulu raporu aranmaksızın, bedellerinin tamamı
hastanın kurumunca ödenecektir.
Böbrek yetmezliği, kistik fibrozis, KOAH, kanser, HIV/AIDS enfeksiyonu, splenektomi
olanlar ve immünsupresif tedavi alan, bağışıklık durumu olumsuz etkilendiği için enfeksiyon
hastalıklarının daha ağır seyrettiği yüksek riskli kişilerin bu durumlarını belgeleyen sağlık
kurulu raporu bulunması halinde reçete edilen aşıların (Sağlık Bakanlığı Genişletilmiş
Bağışıklama Programı kapsamına dahil olan; kızamık, difteri, boğmaca, tetanoz, hepatit B,
polio ve BCG aşıları hariç (MMR ve HİB, Sağlık Bakanlığı tarafından kapsama dahil
edildiğinde hariç tutulacak) bedeli kurumunca ödenir.
Bronşiyal astma, alerjik rinit, alerjik konjonktivit ve benzeri atopik (akar) duyarlılığı olan
hastaların tedavisinde kullanılması immünoloji, çocuk hastalıkları, kulak burun boğaz, göz
hastalıkları veya göğüs hastalıkları uzman hekimlerinden birinin bulunduğu sağlık kurulu
raporu ile belgelendirilen hastalara bu uzmanlar ve bunların bulunmadığı yerlerde dahiliye
uzmanı veya aile hekimince reçete edilen enjektabl yolla alınan alerji aşısı bedeli, hasta
katılım payı alınması kaydıyla ödenir. Alerji aşılarının oral formları ödenmez. Medikal tedavi
ve izlemin 3 ay yapılması sonrası laboratuar testlerine göre aşı uygulaması tam teşekküllü
resmi sağlık tesisinde ve öncelikle hastayı alerji yönünden izleyen uzman hekimin kontrol ve
sorumluluğunda, bu hekimin bulunmaması durumunda yukarıda belirtilen branş
uzmanlarından biri tarafından yapılacaktır. Tedavi arı venom alerjisi hariç 5 yılı geçemez. Arı
venomları sağlık kurulu raporu ile yukarıda belirtilen şartlardaki hekimler tarafından reçete
edilebilir.
Grip aşıları için; 65 yaş ve üzerindeki kişiler ile yaşlı bakımevi ve huzurevinde kalan kişilerin
durumlarını belgelendirmeleri halinde sağlık kurulu raporu aranmaksızın, astım dahil kronik pulmoner
ve kardiyovasküler sistem hastalığı olan erişkin ve çocuklar, diabetes mellitus dahil herhangi bir kronik
metabolik hastalığı, renal disfonksiyonu, hemoglobinopatisi veya immünsupresif olan erişkin ve
çocuklar ile 6 ay 18 yaş arasında olan ve uzun süreli aspirin tedavisi alan çocuk ve adolesanların
hastalıklarını belirten heyet raporuna istinaden, tüm hekimlerce reçete edildiğinde aşıların bedelleri
kurumlarınca yılda bir defaya mahsus olmak üzere ödenir.
Pnömokok aşısı 2 yaş üstü çocuklarda ve erişkinlerde astım dahil kronik pulmoner ve
kardiyovasküler sistem hastalığı olan erişkin ve çocuklar, diabetes mellitus dahil herhangi bir
kronik metabolik hastalığı, renal disfonksiyonu, hemoglobinopatisi, splenektomisi olan veya
splenektomi planlanan olgularda proflaksi amacıyla veya immünsupresif olan erişkin ve
çocuklar ile 6 ay–18 yaş arasında olan ve uzun süreli aspirin tedavisi alan çocuk ve
adolesanların hastalıklarını belirten heyet raporuna istinaden tüm hekimlerce reçete
edildiğinde aşıların bedelleri kurumlarınca 5 yılda bir ödenir.
Yukarıda belirtilenlerin dışında kalan aşı bedelleri ödenmeyecektir. Sağlık Bakanlığı,
UNICEF ile yapacağı protokol kapsamında aşı ve serum temin edebilir, bu aşı ve serumları
ücretsiz olarak halka uygular.
Bu maddede bahsi geçen splenektomiler medikal, cerrahi ve otosplenektomileri
kapsamaktadır.
12.7.4. Rasburicase Kullanım İlkeleri
Myeloablatif dozda çoklu ajanlı kemoterapi uygulanan, tümör yükü olan
hematolojik maligniteli, urikoliz ve hidrasyon tedavisine rağmen böbrek fonksiyonları
bozulmuş (kreatin > 2 mg/dl, kreatin klerensi < 50 ml/dakika) ve urikolizin kontrendike
olduğu hastalarda prospektüs şartlarına (en fazla 5 günlük tedavi) göre yatan hastalarda
kullanılır. Pediatrik veya erişkin hematoloji, onkoloji veya nefroloji uzman hekimleri
tarafından çıkartılmış ilaç raporu doğrultusunda bu uzmanlardan birinin yazdığı reçeteye göre,
raporda laboratuar sonuçlarının yer alması kaydıyla geri ödenir.
12.7.5. Botulismus Toksini Tip A
a) Botulismus toksini, ancak organik nedenleri ekarte edilmiş ve tıbbi tedaviye
cevap vermeyen olgularda, bu durumu belirten ve kullanılacak ilacın dozuyla, kullanım
süresini içeren üniversite hastaneleri, eğitim ve araştırma hastanelerinde düzenlenmiş sağlık
kurulu raporuna dayanılarak aşağıda belirtilen branş uzmanlarınca;
- Göz adalesi fonksiyon felçleri bozuklukları
- Blefarospazm
- Hemifasiyal spazm
- Servikal distoni (spazmodik tortikollis)
- EMG esnasında uygulanacak fokal distoni
- Erişkinlerde inme sonrası gözlenen fokal spastisite
olgularında yalnızca üniversite hastaneleri, eğitim ve araştırma hastanelerinde ve belirtilen
uzmanların olduğu erişkin veya çocuk spastisite dal hastanelerinde kullanılabilecektir.
Reçeteler uygulamayı yapacak göz hastalıkları, nöroloji veya fizik tedavi ve rehabilitasyon
uzman hekimleri tarafından düzenlenecektir.
b) Pediatrik Serebral Palside Botulismus Toksini Kullanımı
- Yalnızca üniversite hastaneleri ile eğitim hastanelerinde ve belirtilen uzmanların
bulunduğu erişkin veya çocuk spastisite dal hastanelerinde araştırma hastanelerinde olmak
şartıyla,
- 10 yaşa kadar; sistemik hastalığı, kemiksel deformite, kanama diyatezi, fikst
kontroktür olmayan hastalarda en fazla iki adaleye uygulanmak üzere,
- Ortopedi, fizik tedavi ve rehabilitasyon, pediatrik nöroloji veya çocuk hastalıkları
uzmanı hekimlerinin katılımıyla oluşturulacak sağlık kurulu raporuna dayanılarak,
- Tedaviden yarar görüp tekrarı düşünülen hastalarda 6 ay sonra yeni bir rapor
düzenlenerek en fazla iki uygulama,
- Tek seansta botoks için toplam 300 üniteyi, dysport için 1000 üniteyi aşmamak
üzere,
yapılacaktır.
12.7.6. Büyüme Hormonu Kullanım Esasları
Büyüme hormonu ile tedaviye başlanabilmesi çocuk endokrinoloji/endokrinoloji dallarından
veya bu dalın uzmanları bulunan hastanelerin ilgili bölümlerinden alınacak sağlık kurulu
raporuna bağlıdır. Bu sağlık kurulu raporu, hastanın –hastalığın adı, ilacın adı ve dozu,
uygulama planı ve süresi ile hastayı tedavi eden birimin ve uzman hekimin adını da ayrıca
kapsar. Bu sağlık kurulu raporu, en fazla bir yıl süreyle geçerli olacak hastanın yaşı ve fiziki
boy uzunluğu bu rapora yazılacaktır.
İlaçlar ilgili uzman hekim (Endokrinoloji/çocuk endokrinoloji) tarafından günlük doz miktarı
ve bir kutunun kaç günlük doza tekabül ettiği belirtilmek suretiyle en fazla 3’er aylık dozlar
halinde reçeteye yazılır ve yazılan ilaç miktarı doktorun ismi, diploma numarası ve imzası ile
birlikte sağlık karnesine işlenir.
A) Çocuklarda;
Tedaviye başlanabilmesi için hastanın ilgili uzman hekim tarafından en az 6 ay süreyle
büyüme hızı izlendikten sonra; büyümeyi etkileyen sistematik bir hastalığı veya beslenme
bozukluğu olmayan hastalarda;
1- Yıllık büyüme hızı;
- 0-4 yaş 6 cm’nin altında,
- 4 yaş üzeri 4,5 cm’nin altında,
- Puberte’de; izleme süresi ve büyüme hızı hastanın diğer bulgularına göre endokrinoloji/
çocuk endokrinoloji uzman hekimince değerlendirilmesi;
2- Kemik yaşı;
- Puberte öncesi için kronolojik yaşa göre en az 2 yıl geri olması,
- Pubertal dönem için sadece epifizlerin açık olması,
(Puberte Kıstasları: Erkeklerde gonadarj (testis hacimlerinin) 4 ml. ve üzerine çıkması,
kızlarda T2 düzeyinde telarşın olması, kızlarda kemik yaşının 8'in, erkeklerde 10'un üzerine
çıkması, pubertenin başlangıcı olarak kabul edilecektir.)
3- Ötiroid hastalarda uygulanan büyüme hormonu uyarı testlerinden en az ikisine
(laboratuarın kriterlerine göre) yetersiz yanıt alınarak izole büyüme hormonu eksikliği veya
büyüme hormonunun diğer hipofiz hormonlarının eksikliği ile birlikte olması
(hipopituitarizm) tanılarının konması;
Hastanın yaş grubu ve pubertal bulguları gerektiriyorsa büyüme hormonu testleri
yapılmadan mutlaka priming yapılmalıdır.
4- Boy sapması patolojik olan (yani -2, 5 SD den daha kötü), yıllık uzama hızı yetersiz olan,
kemik yaşı takvim yaşına göre 2 yıldan daha fazla geri olan, ancak yapılan 2 farmakolojik
uyarı testine yeterli yanıt alınan hastalara uyku esnasında büyüme hormonu profili çıkartılmalı
ve hastada büyüme hormonu eksikliği olmamasına rağmen eğer büyüme hormonu salınımında
bir bozukluk söz konusu ise, yani nörosekretuar disfonksiyon söz konusu ise yada; hastada
biyoinaktif büyüme hormonu saptanmış ise (IGF 1 testi ile);
Bu hususların düzenlenecek sağlık kurulu raporu ile tevsik edilmesi halinde hastaya büyüme
hormonu tedavisi uygulanacaktır.
Büyüme hormonu ile tedavisine başlanan hastalar endokrinoloji/çocuk endokrinoloji hekimi
tarafından en az 6 aylık sürelerle izlenerek, radyolojik olarak epifiz hatlarının açık olduğunun
gösterilmesi kaydıyla hedeflenen yaş grubu ortalama boy skalasına göre 25 persentile ulaşana
kadar durum her yıl sağlık kurulu raporu ile tevsik edilecektir.
Sonlandırma Kıstasları:
1) Epifiz hattı kapandığında,
2) Yıllık büyüme hızı 5 cm ve altında olduğunda,
3) Boy uzunluğu kızlarda 155 cm ye erkeklerde 165 cm ye ulaştığında,
tedavi sonlandırılacaktır.
4) Tedavi esnasında boy 25 persentile ulaştığında tedavi sonlandırılacaktır.
B) Erişkinlerde;
1) Epifiz hatları açık olan erişkin yaştaki hastaların büyüme hormonu kullanım esasları, çocuk
yaş grubu ile aynıdır.
2) Epifiz hatları kapalı olan hastalarda:
a) Çocukluk yaş grubunda büyüme hormonu eksikliği tanısı konulup, büyüme
hormonu tedavisi verilen ve epifizleri kapandığı için tedavisi kesilen hastalarda tekrarlanan iki
adet büyüme hormonu uyarı testine yetersiz yanıt alınmışsa (kontrendikasyon yoksa testlerden
biri insülin tolerans testi olarak tercih edilmelidir) erişkin dozda büyüme hormonu tedavisi
başlanabilir.
b) Erişkin yaş grubunda hipotalamohipofizer hastalıklara bağlı büyüme hormonu
eksikliği düşünülen hastalarda, 2 adet büyüme hormonu uyarı testine yetersiz yanıt alınmışsa
(kontrendikasyon yoksa testlerden biri insülin tolerans testi olarak tercih edilmelidir) erişkin
dozda büyüme hormonu tedavisi başlanabilir.
3) Hipofiz hormonlarından (prolaktin ve büyüme hormonu dışında) bir veya daha
fazla ek ön hipofiz hormonu eksikliği varsa, bir adet büyüme hormonu uyarı testi
(kontrendikasyon yoksa insülin tolerans testi tercih edilmelidir) tanı için yeterlidir.
4) İnsülin tolerans testine göre büyüme hormonu eksikliği tanısı için pik büyüme
hormonu cevabının 3mcg/L’den küçük olduğunun raporda belirtilmesi gereklidir.
5) Büyüme hormonu, büyüme hormonu tedavisine karar verilen hastalara, üniversite
hastanesi ve eğitim ve araştırma hastanelerinin endokrinoloji bölümleri ile endokrinoloji
kliniği olan ihtisas hastanelerince hazırlanan resmi sağlık kurulu raporuna dayanılarak
başlanabilecektir. Rapora hastanın tanı ve tedavi şeması ile ilgili ayrıntılı bilgi yazılacaktır.
Bu rapor en fazla bir yıl süreyle geçerli olacaktır.
6) Reçeteler erişkin endokrinoloji uzman hekimince yazılacaktır.
12.7.7. Düşük Molekül Ağırlıklı Heparinlerin Kullanım İlkeleri
Bu ilaçlar rapor aranmaksızın uzman hekimler tarafından yazılabilecektir. Hastalığın tanısı,
günlük dozu, kullanılacak ilaç miktarını ve süresini gösteren sağlık kurumlarınca düzenlenen
sağlık kurulu raporuna dayanılarak diğer hekimlerce de yazılabilecektir.
Hastanede yatan hastalarda ve acil müdahale gerektiren durumlarda acil servislerde rapor
aranmaksızın bu ilaçlar diğer hekimlerce de yazılabilecektir.
12.7.8. Enteral ve Paranteral Beslenme Ürünleri Verilme İlkeleri
Enteral beslenme ürünleri, normal çocuk beslenmesinde kullanılanlar hariç olmak üzere
ayaktan tedavide malnütrisyonu olan, barsak operasyonuna bağlı malabsorpsiyon veya oral
beslenemeyen ancak enteral beslenmesi gereken tüm hastalara sağlık kurulu raporuyla
kullanılabilir.
Raporda, hastalığın tanısı, kullanılacak beslenme ürününün jenerik ismi, günlük kalori ihtiyacı
ve buna göre belirlenen günlük kullanım miktarı açıkça yazılıp, reçeteye en fazla üçer aylık
dozda yazılacaktır.
Malnütrisyon tanımı açısından;
-Son 3 ayda ağırlığında % 10 ve daha fazla kilo kaybı veya
-Kan albümin seviyesi 2.5 gram/desilitrenin altında olanlar kabul edilecektir.
Parenteral beslenme ürünleri yatan hastalar dışında resmi sağlık tesislerinde düzenlenmiş
sağlık kurulu raporu ile oral veya tüple beslenemeyen hastalara verilebilir.
12.7.9. Eritropoietin Alfa-Beta, Darbepoetin, Sevelamer ve Parikalsitol Kullanım
İlkeleri
a) Eritropoietin alfa-beta ve darbepoetin içeren ilaçların kronik böbrek yetmezliği tedavisi
gören hastalara kullanımı ve reçeteye yazımı aşağıda belirtilen esaslara göre yapılacaktır
Eritropoietin alfa-beta ve darbepoetin ile tedaviye başlamadan önce; hastanın ferritin ve/ veya
transferrin saturasyonu (TSAT) değerlerine bakılacaktır. Bu değerler TSAT < %20 ve/ veya
ferritin <100 µg/ L ise hastaya öncelikle oral veya intravenöz demir tedavisine başlanacaktır.
TSAT ≥ %20 ve/ veya ferritin ≥ 100 µg /L olduğunda hemoglobin değeri 10 (on) gr/dl
altında ise eritropoietin alfa-beta ve darbepoetin tedavisine başlanabilir. Hedef hemoglobin
değeri 11-12 gr/dl arasıdır. Hemoglobin değeri 11 (onbir) gr/dl'ye ulaşıncaya kadar başlangıç
dozunda eritropoietin alfa-beta ve darbepoetin ile tedaviye devam edilecek ve Hb seviyesini
11-12 gr/dl arasında tutabilmek için idame dozda tedaviye devam edilecektir. Hb seviyesi 12
(oniki) gr/dl'yi aşınca tedavi kesilecektir. Hasta Hb seviyesi için takibe alınacak ve Hb
seviyesi 11-12 gr/dl’nin arasına gelince hastaya idame dozda tedaviye tekrar
başlanabilecektir. İdame tedavi sırasında ve/veya tedaviye yeniden başlandığında TSAT
>%20 ve/veya ferritin >100 µg/ L olacaktır. Bu değerlere 3 ayda bir bakılacak ve tetkik sonuç
belgesi reçeteye eklenecektir.
Diyaliz Merkezleri Yönetmeliğine göre 3 ayda bir yapılan ferritin tetkiki esas alınarak
düzenlenen reçeteler, anılan yönetmeliğin yürürlük tarihi itibarı ile geriye dönük olarak
uygulanır.
Eritropoietin alfa-beta ve darbepoetin, nefroloji uzmanı veya diyaliz sertifikalı uzman
hekimlerden en az birinin bulunduğu sağlık kurulu raporu ile nefroloji uzmanı, diyaliz
sertifikalı uzman veya diyaliz sertifikalı hekimlerce yazılabilir.
Eritropoietin alfa-beta ile tedaviye başlangıç dozu 50- 150 IU/ kg/ hafta ve idame dozu 25- 75
IU/ kg/ haftadır. Darbepoetin ile tedaviye başlama dozu 0.25-0.75 mcg/kg/hafta ve idame
dozu 0.13-0.35 mcg/kg/haftadır.
b) Eritropoietin alfa-beta ve darbepoetin içeren ilaçların kronik böbrek yetmezliğinin dışında
kullanımı; eritropoietin türevlerini ve darbepoetin içeren ilaçların kronik böbrek yetmezliği
dışında kullanımında Sağlık Bakanlığınca belirlenen endikasyonlara ve kurallara uyulacaktır.
Yeni doğanda eritropoietin kullanımı: doğum ağırlığı 1500 gr’ın altında veya 32 gebelik
haftasından önce doğan bebeklere 200 İU/kg/hafta 3 kez 6 hafta süre ile uygulanabilir.
Bir defada en fazla 1 aylık ilaç verilebilecektir. Sağlık kurulu raporlarında ilacın adı, kullanım
dozu ve süresi belirtilecektir. Eritropoietin alfa-beta ve darbepoetin endikasyon muadili olarak
birbirlerinin yerine kullanılabilirler.
c) Sevelamer ile tedaviye başlamak için diğer fosfor düşürücü ilaçların 3 ay süreyle
kullanılmış olması gerekmektedir. Bu süre sonunda:
1) kalsiyum ve fosfor çarpımı 72 ve üzerinde olan veya kemik biyopsisi sonucuna göre
adinamik kemik hastalığı olduğu belgelenen,
2) hastanın Kt/V değeri 1.4’ün üzerinde olmasına rağmen düzeltilmiş kalsiyum ve fosfor
çarpımı 55’in üzerinde olan,
3) Kt/V 1.4'ün üzerinde olan hastanın PTH değeri 300 pmol/dl ve üzerinde ve D3 kullanma
endikasyonu olan,
hemodiyaliz tedavisi altındaki hastalara nefroloji veya diyaliz sertifikalı dahiliye/pediatri
uzman hekimlerinin düzenlediği sağlık kurulu raporu ile nefroloji veya diyaliz sertifikalı
dahiliye/pediatri uzman hekimleri tarafından reçete edilir. Fosfor düzeyi 3.5mg/dl'nin altında
olduğu durumlarda sevelamer tedavisi kesilir.
d) Parikalsitol ile tedaviye; hemodiyaliz tedavisi altındaki PTH düzeyleri 300-800 pg/ml
değerlerinin arasında olan hastalarda diyalizat kalsiyumunun 1.25 mmol/l ile kullanılmasına
rağmen albumin ile düzeltilmiş serum kalsiyumu 9,5 mg/dl ve serum P 4,5 mg/dl olduğu
belgelenen hastalarda başlanır. Aynı hasta grubunda düzeltilmiş serum kalsiyum düzeylerinin
10.2, serum P düzeylerinin 6mg/dl’yi geçtiği durumlarda kesilir. İlgili koşulların söz konusu
olduğu hastalarda hemodiyaliz raporuna istinaden 3 aylık dozla nefrolog veya diyaliz hekimi
tarafından reçete edilebilir. Tetkikler 3 ayda bir tekrarlanır ve tetkik sonucu reçeteye eklenir.
12.7.10. Lizozomal Hastalıklar için Tedavi Esasları
Hastalığın kesin teşhis ve tedavisinin sağlanması için hasta endokrinoloji ve metabolizma
veya gastroenteroloji (çocuk veya erişkin) uzmanı hekiminin bulunduğu eğitim ve araştırma
hastanelerine gönderilecektir. Bu hastanelerde, hastaya tanı konulacak, hastalığı ile ilgili
endokrinoloji ve metabolizma veya gastroenteroloji (çocuk veya erişkin) uzman hekiminin
bulunduğu, tanı-tedavi şemasını gösterir sağlık kurulu raporu düzenlenecektir.
Bu rapora dayanılarak hastanın tedavisi için gerekli ilaçlar endokrinoloji ve metabolizma veya
gastroenteroloji (çocuk veya erişkin) uzman hekimi tarafından 3 ayı aşmayacak miktarda
reçeteye yazılacaktır. Hastanın takip ve tedavi edildiği endokrinoloji ve metabolizma uzman
hekimi bulunan eğitim ve araştırma hastanelerinde hastalar adına dosyalar açılacak ve tüm
bilgiler bu dosyada muhafaza edilecektir.
Hastanın tedavisi sağlık kurulu raporunda belirtilen tedavi şemasına göre endokrinoloji ve
metabolizma veya gastroenteroloji (çocuk veya erişkin) uzman hekimi, bulunmadığı yerlerde
çocuk sağlığı ve hastalıkları veya iç hastalıkları uzman hekimlerince klinik koşullarda
uygulanacaktır.
Hasta 3 ayda bir endokrinoloji ve metabolizma uzman hekimi bulunan eğitim ve araştırma
hastanelerinde kontrol edilecektir.
A) Gaucher Hastalığı Tedavi Esasları
a) Tanı Kriterleri;
1- Hastanın enzim düzeyi (Glucocerebrosidase) belirlenerek, enzimatik tanı konulacaktır veya
2- Mutasyon analizi yapılacaktır.
b) Enzim tedavisine başlama kriterleri;
1- Tedavi endikasyonu olan hastalık tipleri
- Tip I (Non Nöropatik Form)
- Tip III (Kronik Nöropatik Form)’tür.
- Tip II (Akut Nöropatik Form) için enzim tedavisi yapılmayacaktır.
2- Hastalığın tanısı, bir eğitim hastanesinde ve gastroenteroloji (çocuk veya erişkin) veya
endokrinoloji ve metabolizma uzmanlarının da yer aldığı bir sağlık kurulu tarafından
konulacak ve hastaya tanı ve tedavi ile ilgili tüm bilgileri içeren bir rapor düzenlenecektir.
c) Tedavinin Kesilmesi;
1- Hasta 3 ayda bir tanı ve tedavi aldığı merkezde kontrol edilecektir. İzlemde karaciğer-dalak
boyutlarının değerlendirilmesi ve tam kan sayımı ile karaciğer enzimlerinin tayini, eğer gerek
görülür ise 1 yıllık periyotlar ile karaciğer-dalak boyutlarının volumetrik, kemik lezyonlarının
takibi uygundur.
2- Hastanın tedavisinin yapıldığı resmi sağlık tesisinde hastalar adına dosyalar açılacak ve
tüm bilgiler bu dosyada muhafaza edilecektir.
3- Tanıyı koyan resmi sağlık tesisi tarafından hastanın tedaviye başlama öncesi
kriter/kriterlerindeki düzelme durumu belgelenecektir.
4- Halen tedavi almakta olan hastaların tedaviye devam edip etmeyecekleri bu Tebliğ’de yer
alan tedavi kriterlerine göre değerlendirilecektir.
5- Tedaviye cevap alınamadığı belirlenen durumlarda tedavi kesilecektir (İzleme
parametrelerinde tedavi başlandıktan en az 6 ay sonra hiçbir düzelme meydana gelmez ise).
B) Fabry Hastalığı Tedavi Esasları
1- Hastanın enzim düzeyi (Galactosidase) belirlenerek enzimatik tanı konulacaktır.
2- Uygulanacak enzim dozu Sağlık Bakanlığı’nın belirleyeceği dozu geçmeyecektir. Bu doz 2
haftada bir 1mg/kg’dır.
Hastalığın teşhisi, bir eğitim hastanesinde ve gastroenteroloji (çocuk veya erişkin)
veya endokrinoloji ve metabolizma uzmanlarının da yer aldığı bir sağlık kurulu tarafından
konulacak ve hastaya tanı ve tedavi ile ilgili tüm bilgileri içeren bir rapor düzenlenecektir.
C) Mukopolisakkaridoz Tip I Hastalığı Tedavi Esasları
1- Hastanın enzim düzeyi (L-İduronidase) belirlenerek enzimatik tanı konulacak ve mutlaka
mutasyon analizi yapılacaktır.
2- Enzim tedavisi tek başına Hurler-Schie ve Schie formlarında haftada bir 0.58mg/kg’dır.
Hurler tipinde ise 3 aylık enzim tedavisinin ardından kemik iliği transplantasyonu yapıldıktan
sonra 3 ay daha enzim tedavisi devam edecek, klinik düzelme olduğu takdirde tedavi
sonlandırılacaktır.
D) Diğer Lizozomal Depo Hastalıklarının Tedavi Esasları
Pompe, mukopolisakkaridoz Tip II, VI, VII, niemann-pick, wolman hastalığı,
kolesterol ester depo hastalığı gibi hastalıkların tedavileri için bu maddede belirtilen esaslara
uyulacaktır.
12.7.11. Glokom İlaçları
Glokom ilaçları ile tedaviye göz hastalıkları uzmanı tarafından başlanacaktır. Göz
hastalıkları uzmanının bulunduğu, kullanılacak ilacın etken maddesini belirten bir sağlık
kurulu raporu mevcut ise, rapor süresince diğer hekimlerce de reçeteye yazılabilecektir.
12.7.12. İmmünglobulinlerin Kullanım İlkeleri
A) Spesifik/Hiperimmün İV İmmünglobulinlerin Kullanım İlkeleri
Ayaktan tedavide spesifik/hiperimmün immünglobulinlerin geri ödenmesinde, sadece Sağlık
Bakanlığının onay verdiği endikasyonlarda sağlık kurulu raporu şartı aranarak, bu ilaçlara ait
reçeteler uzman hekimlerce yazılacaktır. Hepatit B, tetanos ve kuduz immünglobulinlerinde
sağlık kurulu raporu şartı aranmayacaktır.
Anti-HEP B IG klinik uzmanlar tarafından ve vaka başına profilaktik olarak 0.02-0.06 ml/kg
/doz erişkinlerde maksimum 1600 ünite, çocuklarda maksimum 800 üniteyi aşmamak üzere
reçete edilmesi halinde ödenebilecektir
Hepatit B İmmunglobulinin Hepatit B virüs yüzey antijeni taşıyan (HbsAg) hastalarda karaciğer
transplantasyonu sonrası enfeksiyon profilaksisi endikasyonunda kullanımı, söz konusu ilaçların
prospektüsünde de belirtildiği gibi ameliyat süresince karaciğersiz fazda 10.000 IU, ameliyattan sonra
ise her gün (yedi gün boyunca) 2.000 IU şeklindedir. Takip eden uzun dönem tedavi süresince aylık
Anti HBs serum seviyesi kontrolleriyle, 100 IU/litre serum seviyesi olacak şekilde sürdürülmelidir. Bu
uzun dönem tedavi süresince aylık toplam 2000 IU dozuna kadar kullanılması uygundur."
B) Spesifik Olmayan/Gamma/Polivalan İmmünglobulinler
Gama globulin preparatları belirlenen endikasyonlarında hematoloji, onkoloji, immünoloji
uzmanları tarafından reçete edilebilir.
Ayrıca;
1) Pediatrik HIV enfeksiyonunda Pediatrik Enfeksiyon uzmanı,
2) Guillan-Barre sendromunda, bulber tutulumu olan myastenia graviste nöroloji (yetişkin ve
pediatrik) uzmanı,
3) Gebeliğe sekonder immün trombositopeni veya gebelik ve ITP beraberliğinde Kadın
Doğum uzmanı,
tarafından reçete edilebilir.
Tüm kullanımlar için hematoloji, onkoloji veya immünoloji uzmanlarının veya belirtilen
hastalıklarda, belirtilen uzmanın bulunduğu sağlık kurulu raporu ile uzman hekimlerce reçete
edilebilecektir.
12.7.13 İnterferon Kullanım İlkeleri
A) Kronik Viral Hepatitlerde Alfa İnterferon Kullanım İlkeleri
1) İnterferonlar, kronik hepatit tedavisinde çocuk veya erişkin gastroenteroloji veya
enfeksiyon hastalıkları uzmanları tarafından düzenlenen sağlık kurulu raporunda yer alması şartıyla,
yukarıda belirtilen uzmanlık dallarındaki hekimler veya iç hastalıkları uzmanlarınca da reçete edilir.
2) Kronik hepatit B'de 6 aydan fazla süredir ALT düzeyleri normalin en az 2 katından fazla
veya biyopsi ile tanı konmuş, HBV DNA pozitif olan ve kronik hepatit saptanmış kompanse kronik
hepatit-B’li hastalara uygulanır. Tedavi süresi 12 ayı, tedavi dozu haftada 35 milyon üniteyi geçemez.
3)Kronik hepatit C’de Anti HCV ve HCV RNA’sı pozitif, histolojik olarak kronik
hepatit saptanan, kompanse karaciğer hastalığı bulguları olan hastalara ribavirinle kombine
uygulanır.
Ancak, ribavirin kontrendikasyonu var ise interferon (klasik interferon veya pegil
interferonlar)
monoterapisi
uygulanacaktır.
Gerek monoterapide gerekse ribavirin + interferon (klasik interferon veya pegil interferonlar)
kombine tedavisinin en geç 6 ncı ayında tedaviye cevap alınamaması halinde, rapor üzerinde
belirtilerek tedavi sonlandırılacaktır (3 üncü ayda yapılan HCV RNA kontrolünde başlangıca
göre 2 log’dan küçük azalma) (ağır fibrozis veya kompanse sirozu olan hastalarda 3 üncü ve
6 ncı ay değerlerine bakılmaksızın tedavi süresine ilgili hekim tarafından karar verilir).
Tedavi süresi 12 ayı, tedavi dozu haftada 18 milyon üniteyi geçemez
4) Hepatit-D’de 6 aydan fazla süredir ALT düzeyi normalin en az 2 katından fazla veya
biyopsi ile tanı konmuş, anti deltası pozitif olan ve kronik hepatit saptanmış kompanse
karaciğer hastalığı bulguları olan hastalara uygulanır.”
5) 2 ve 3 üncü maddede belirtilen kronik hepatit B ve kronik hepatit C tedavisine başlama
kriterlerine uygun olarak 18 yaşın üzerindeki hastalarda veya klasik interferon tedavisinde
nüks
hastalarda
Pegil
İnterferonlar
kullanılır.
Tedavi süresi 12 ayı geçemeyecektir. 3 üncü veya 6 ıncı ayda tedaviye yanıt alınamaması
(Kronik hepatit C’de madde 3’de belirtildiği şekilde) durumunda tedavi kesilecektir.
6) Kronik hepatit-B’de (1)nci maddede yer alan uzman hekimlerce sağlık kurulu raporu ile
adefovir veya entakavir kullanılır.
7) Teşhise esas olan bulgular sağlık kurulu raporunda belirtilecektir.
B) Multipl Skleroz Hastalığında Beta İnterferon ve Copolymer-l Kullanım
İlkeleri
a) Disabilite skorunun (E.D.S.S.) 0–5,5 arasında olması, hastanın yardımsız olarak en az 100
m. yürüyebilmesi,
b) Olguların remitting-relapsing türü olması, (2 yıl içerisinde en az 2 atak geçirmesi, yeni
vaka’larda ise 1 yıl içerisinde 2 atak geçirmiş olması, gerekmektedir.)
Bu ilaçlar nöroloji uzmanının bulunduğu sağlık kurulu raporuna dayanılarak verilecektir.
Reçeteler yalnızca nöroloji uzman hekimlerince düzenlenecektir.
12.7.14. Kanser İlaçları Verilme İlkeleri
a) Ayaktan tedavide kemoterapi yapılacak kanserli hastalara kür tedavisi uygulanıyor ise kür
protokolünü gösterir sağlık kurulu raporuna dayanılarak bir kürlük, kür tedavisi
uygulanmayanlarda ise en fazla 3 aylık dozda ilaç verilebilir.
Ancak; hormonlar ve hormon antagonistleri ile maligniteye bağlı metastatik olgularda
kullanılan yardımcı ilaçlar, sağlık kurulu raporu ile 3 aylık dozlarda verilebilir.
b) Kanser ilaçları diğer ilaçlarda olduğu gibi Sağlık Bakanlığının izin verdiği endikasyonlarda
kullanılacaktır. Ruhsatlı endikasyonda kemoterapi seçeneğini kullanmış olan ve kemoterapi
dışında seçeneği olmayan kanserli hastalar için; cevap alınabilecek veya sağ kalım avantajı
sağlayabilecek kanser ilaçlarının bedeli, yeterli literatür desteği ile birlikte Sağlık
Bakanlığınca onaylandığı takdirde ödenir. Bu durumda sağlık kurulu raporunda ilk tedavi
veya tekrarlayan hastalıkta kullanım muhakkak belirtilecektir.
Ancak, klasik kemoteröpik İlaçlar (Adriamisin, dakarbazin, epirubisin, etoposid, fluorourasil,
ifosfamid, karboplatin, metotreksat, siklofosfamid, sisplatin, tamoksifen, vinblastin,
vinkristin, mitoksantron, klorambusil, melfalan, busulfan, merkaptourin, bleomisin, mitomisin
C, hidroksiüre ve mitotan) (a) bendindeki nitelikleri taşıyan sağlık kurulu raporu ile, tıbbi
sorumluluğu, tedaviyi planlayan uzman hekime ait olmak üzere, uygun görüldüğü durumlarda
kullanılabilir.
c) Aşağıda belirtilen ilaçların onkolojik tedavide kullanımında hastalığın teşhisi, teşhise esas
teşkil eden patoloji veya sitoloji raporunun merkezi, tarihi ve numarası, (patoloji veya
sitolojik inceleme yapılamamış ise teşhise esas teşkil eden bilgiler içeren bir epikriz) evre
veya risk grubu, varsa daha önce uygulanan kemoterapiler, planlanan kemoterapi ve planı
yapan ilgili uzman hekimin adı, unvanı ve imzasının bulunduğu sağlık kurulu raporuna
istinaden diğer hekimlerce de yazılabilecektir.
İnterferon alfa 2a-2b, eritropoietin alfa-beta, darbepoetin, trastuzumab, rituximab,
(rituximab; nükseden veya kemorezistan CD20 pozitif foliküler lenfoma, diffüz büyük B
hücreli lenfoma, mantle hücreli lenfoma tanılı hastaların tedavisinde, evre III veya evre IV
CD20 pozitif foliküler lenfomalı hastalarda CVP “siklofosfomid, vinkristin, prednisolon”
tedavisine ek olarak, CD20 pozitif diffüz büyük B hücreli lenfomada CHOP kemoterapi
şemasına ek olarak kullanımı endikedir. Yukarıda bahsedilen foliküler lenfoma ve mantle
hücreli lenfomada maksimum 8 dozda kullanımı geri ödenir. Bu iki durumda rituximab
kullanımına cevap veren ancak progresif hastalık gelişen olgularda ilave olarak 4 doz daha
kullanılabilir. CD20 pozitif diffüz büyük B hücreli lenfomada maksimum 8 doza kadar geri
ödenir. İbritumomab tiuxetan terapötik rejiminin bir parçası olarak kullanıldığında maksimum
iki doza kadar geri ödenir.), interleukin-2, bevacisumab, cetuximab, ibritumomab, imatinib
(Imatinib; onkoloji veya hematoloji uzmanının bulunduğu en fazla 6 ay süreli sağlık kurulu
raporu ile bu uzmanlar tarafından reçete edilir.), gefinitib, erlotinib, octreotid (Octreotid;
akromegali tedavisinde endokrinoloji uzmanlarınca reçete edilir.), bortezomib, talidomit,
docetaksel, paclitaxel, imiquimod, temozolomide etken maddelerini içeren ilaçlar tıbbi
onkoloji ile pediatrik onkoloji, hematoloji veya pediatrik hematoloji uzmanlarınca, ayrıca bu
uzmanların bulunduğu hastanelerde diğer hekimlerce tavsiye edildiğinde yukarıda sayılan
uzmanların uygun görüşüyle (raporda onay kaşe ve imzası ile), sayılan uzmanların
bulunmadığı hastanelerde ise hastalıkla ilgili branşlarda diğer uzmanlarca düzenlenmiş sağlık
kurulu raporlarına istinaden tüm hekimlerce yazılabilir. Bu ilaçların onkoloji dışı kullanımları
ilgili alanlarındaki uzman hekimler tarafından yapılabilir.
“Alemtuzumab: Kemik iliği tutulumu gösterir biyopsi sonucuyla, yeterli doz ve sürede
alkilleyici ajanlar alan ve fludarabin fosfat kürlerini tamamlayan ya da fludarabin temelli
kombinasyon rejimlerine kesin olarak dirençli hale gelmiş (Evre III veya Evre IV Kronik
Lenfoid Lösemi-KLL) hastalarında hematoloji uzmanının yer aldığı sağlık kurulu raporunda
belirtilmesi şartıyla, sekiz haftalık tedaviyle cevap alınması durumunda raporda belirtilmesi
koşuluyla tedavinin on iki haftaya kadar uzatılabilmesi, cevap alınamaması durumunda ise
tedavinin sekiz haftayla sınırlandırılması, bu rapora istinaden hematoloji veya tıbbi onkoloji
uzmanlarınca reçete edilebilir.
Vinorelbin tartarat: Vinorelbin tartaratın oral formları, kür protokolünde belirtilmek
şartı ve tedaviye enjektabl form ile başlanması koşuluyla tedavinin sekizinci günü oral
formları maksimum 120 mg/21 gün dozda kullanılanların bedeli ödenir.
Fulvestrant: Doğal veya yapay postmenapozal kadınlarda, lokal veya metastaz yapmış
hormon reseptör pozitif meme kanserinde, endokrin tedaviden (anastrozol, tamoksifen) sonra
ilerlemeye devam etmiş hastalarda, hazırlanan raporda bunların belirtilmesi koşuluyla reçete
edilebilir.”
12.7.15. Klopidogrel Kullanım İlkeleri
a) Koroner artere stent uygulanacak hastalarda kardiyoloji, iç hastalıkları veya kalp
damar cerrahisi uzman hekimleri tarafından rapor aranmaksızın bir defaya mahsus olmak
üzere 24 saat öncesinden başlanabilir. İlaç salınımsız stent takılan hastalarda hastanın taburcu
olmasından itibaren rapor aranmaksızın 4 haftalık doz bu hekimler tarafından reçete edilebilir.
Diğer (ilaç salınımlı) stentlerde ise stent uygulama tarihinden itibaren 6 ayı geçmeyecek
şekilde bu hekimlerden birinin bir defaya mahsus olmak üzere hazırladığı sağlık kurulu
raporu ile diğer hekimler tarafından da reçete edilebilir.
b) Akut koroner sendrom tanısıyla hastaneye yatırılan veya müşahedeye alınan
hastalarda EKG değişikliği veya troponin pozitifliği saptanmış ve belgelenmiş olan ST
yükselmesiz miyokard enfarktüsü veya anstabil anginalı hastalar ile ST yükselmeli miyokard
enfarktüsü hastalarında kardiyoloji, iç hastalıkları, kalp damar cerrahisi veya acil tıp uzman
hekimleri tarafından rapor aranmaksızın bir defaya mahsus olmak üzere kullanılabilir. Bu
durumlarda hasta taburcu olduktan sonra 4 haftayı geçmemek üzere bu hekimlerden birinin
hazırladığı sağlık kurulu raporu ile diğer hekimler tarafından da reçete edilebilir.
c) Kalp kapak biyoprotezi bulunanlarda, koroner arter hastalığı, tıkayıcı periferik
arter hastalığı veya serebral iskemik olay (iskemik inme) saptanan ve belgelenen hastalarda;
gastrointestinel entolerans veya diğer tıbbi nedenlerden dolayı asetilsalisilik asit ve diğer
antiagregan ilaçların kullanılamadığı durumlarda gerekçenin belirtilmesi halinde kardiyoloji,
iç hastalıkları, nöroloji, kalp damar cerrahisi veya acil tıp uzman hekimlerinden birinin
hazırladığı ve 12 ayı geçmemek üzere kullanım süresinin belirtildiği sağlık kurulu raporu ile
diğer hekimler tarafından da yazılabilir. Burada bahsedilen durumlarda rapor süresi
dolduğunda durumun devam ettiği belgelendiği taktirde hastaya tekrardan rapor çıkarılabilir.
d) Girişimsel periferik veya serebral işlemler sonucu, intrakraniyal de dahil olmak
üzere tüm intravasküler (intraarteriyel veya intravenöz) stent, stentgraft, kaplı stent veya tüm
intravasküler cihaz (koil, trispan, onyx veya benzeri) yerleştirilen hastalarda kardiyoloji, iç
hastalıkları, nöroloji, kalp damar cerrahisi uzman hekimleri veya girişimsel radyoloji işlemini
yapan radyolog tarafından rapor aranmaksızın bir defaya mahsus olmak üzere 24 saat
öncesinden başlanabilir. Bu işlemler ile ilaç salınımsız stent takılan hastalarda hastanın
taburcu olmasından itibaren rapor aranmaksızın 4 haftalık doz bu hekimler tarafından reçete
edilebilir. Diğer (ilaç salınımlı) stent takılan hastalarda girişimsel uygulama tarihinden
itibaren 6 ayı geçmeyecek şekilde bu hekimlerden birinin hazırladığı sağlık kurulu raporu ile
diğer hekimler tarafından da reçete edilebilir.
12.7.16. Metabolik Hastalıklar ile Enzim Bozukluğu Hastalıkları
a) Çocuk mamaları, gıda olması nedeniyle listeye dahil edilmemiştir. Ancak, doğuştan
metabolik hastalığı, enzim bozukluğu olan ve kistik fibrozisli hastalar için tedavi edici içerikli
olanlar ile malabsorbsiyona neden olan bir hastalığı olan hastaların ve iki yaşına kadar inek
sütü alerjisi olan bebeklerin kullandıkları özel mamalar, sağlık kurulu raporu alınması
(öncelikle pediatrik veya erişkin endokrinoloji ve metabolizma uzman hekimi tarafından,
onların yokluğunda çocuk hastalıkları veya iç hastalıkları uzman hekimleri tarafından
çıkarılmış rapor) koşuluyla tüm hekimler tarafından yazılabilir. Fenil ketonüri hastalarında da
glutensiz un ayda maksimum 5 kg’a kadar ödenecektir.
b) Çölyak hastalığında; özel formüllü un ve özel formüllü un içeren ürünler çocuk veya
erişkin gastroenteroloji uzmanının yer aldığı sağlık kurulu raporuna dayanılarak, 15 yaşın
altında olan hastalarda bir aylık 2 kg’ı mamul (makarna), 250 gramı (çikolata, gofret vb)
olmak üzere toplamda en fazla 5kg 250 gram olacak şekilde verilecektir. 15 yaş ve üzerinde
olan hastalara bir aylık 2 kg mamul olmak üzere toplamda en fazla 5 kg olacak şekilde
verilecektir. Sağlık kurulu raporunda bir aylık en fazla kullanım miktarı ve kullanım süresinin
un ve ürün olarak ayrı ayrı belirtilmesi zorunludur. Bu ürünler en fazla üçer aylık dozlar
halinde, sağlık kurulu raporunda belirtilen kullanım süresi ve miktarlara uygun olarak tüm
hekimlerce reçeteye yazılabilecek ve unun 1kg’ı için ödenecek azami tutar 5 YTL’yi
geçmeyecektir. Bu ürünlerin bedeli katkı payı alınmaksızın kurumlarca karşılanacaktır.
12.7.17. Osteoporoz İlaçları Kullanım İlkeleri
Senil ve postmenopozal osteoporoz tedavisinde
Aşağıdaki hasta gruplarında bifosfonatların veya diğer osteoporoz ilaçların (calcitonin,
raloksifen, stronsiyum ranelat) kullanımında raporda tedavi süresi belirtilecek, omurgadan ve
femurdan yapılan tetkiklerle ilgili KMY ölçümünün bir örneği reçeteye eklenecektir.
Bu grup ilaçlar;
1. Osteoporotik patolojik kırık bulunan ve lomber bölgeden posteroanterior veya lateral
yapılan kemik mineral yoğunluk (KMY) ölçümünde total L2-4 (veya total L1-4) veya femoral
bölgeden yapılan KMY ölçümünde total femur veya femur boynundan elde edilen “T”
değerlerinden herhangi birinin -1 veya daha düşük olduğu hastalarda,
2. Lomber bölgeden posteroanterior veya lateral yapılan KMY ölçümünde total L24 (veya total L1-4) veya femoral bölgeden yapılan KMY ölçümünde total femur veya femur
boynundan elde edilen “T” değerlerinden herhangi birinin -2,5 veya daha düşük olduğu
hastalarda,
sağlık kurulu raporuna dayanılarak tüm hekimlerce reçete edilir. Rapor süresi 1
yıldır. Rapor süresi bitiminde KMY ölçümü tekrarlanacaktır.
Sudek atrofisinde standart tedavilere (analjezik, fizyoterapi) rağmen yeterli cevap alınamadığının
(6 ay) ve lokal kırığın raporda belirtilmesi halinde”
Bu esaslar yatan hasta reçetelerinde de uygulanır.
12.7.18. Orlistat ve Sibutramin Etken Maddesi İçeren İlaçların Kullanım İlkeleri
Endokrinoloji ve metabolizma uzman hekiminin bulunduğu resmi sağlık kurumlarınca
düzenlenen en fazla üç aylık süreli sağlık kurulu raporuna dayanılarak yazılabilecek, raporun fotokopisi
reçeteye eklenecektir. Yazılan her reçeteye hastanın bir önceki reçeteye göre kaybettiği kilo, diyet ve
egzersize uyduğu, BMI değeri hekim tarafından yazılarak imza ve kaşe altına alınacaktır. Bu rapora
dayanılarak tüm hekimlerce reçete edilebilecektir.
- Daha önce dört ardışık hafta boyunca yalnızca diyetle en az 2,5 kg.lık bir kilo kaybı olmalıdır.
- Obez hastalarda vücut kitle indeksi (BMI) ≥ 40 kg/m2 olmalıdır.
- Bu grup ilaçlardan aynı anda sadece biri kullanılacaktır.
İlk üç ay hastaların kontrolü her ay yapılacaktır. İlaçlar birer aylık verilecektir.
Tedavinin 12 haftası sonunda hastalarda başlangıçtaki vücut ağırlığının en az %5'ini
kaybetmesi halinde tedavinin devamına karar verilirse, yeni bir rapor daha düzenlenerek tedavi üçer
aylık sürelerle uzatılabilecektir. 12 hafta sonunda vücut ağırlığının en az %5'inin kaybolmaması halinde
tedavi kesilecektir. Bu etkin maddelerin kullanımları hastanın hayatı boyunca her şartta 2 yılı
geçmeyecektir.
12.7.19. Migrende İlaç Kullanım İlkeleri
a) Triptanların oral formları nöroloji uzman hekimce reçete edilir. Sağlık kurulu
raporu varsa (nöroloji uzmanının bulunduğu) diğer hekimler tarafından da yazılabilir. Bu grup
ilaçlardan yalnız bir etken madde reçete edilebilir, ayda en fazla 6 doz/adet (tablet, sprey veya
kartuş) yazılabilir. Aynı ilacın farklı farmasötik formları aynı anda yazılamaz.
b) Topiramat diğer profilaktik migren ilaçların 6 ay süreyle kullanılıp etkisiz kaldığı
durumlarda nöroloji uzmanının yer aldığı sağlık kurulu raporunda belirtilerek tedaviye
başlanır.
Sağlık kurulu raporu 1 yıl süreyle geçerlidir ve raporla tüm hekimlerce yazılır.
12.7.20. Palivizumab Kullanım İlkeleri
Palivizumab etken maddesini taşıyan preparatın yenidoğan, alerji ve enfeksiyon üst ihtisası
yapmış çocuk hastalıkları uzmanları tarafından reçetelenmesi ve belirtilen koşullarda
kullanılması halinde bedelleri hasta katılım payı alınmadan ödenir.
Yüksek RSV riski taşıyan pediatrik hastalarda respiratuar sinsisyal virüsün (RSV)
neden olduğu ciddi alt solunum yolu hastalığının önlenmesinde;
a) 12 aylıktan küçük ve tıbbi destek alan (oksijen beraberinde diüretik, steroid ve
bronkodilatatör kullanılan) ve bronkopulmoner displazisi olanlarda,
b) Bronkopulmoner displazisi olmaksızın prematüre doğan ve yoğun bakımda
respiratuar tedavisi (solunum desteği) almış olan bebeklerde profilaktik olarak Ekim-Mart
ayları arasında, ayda bir kez ve en fazla 2 yaşına kadar mevsim başlangıcında kullanılmalıdır.
12.7.21. Anagrelid Kullanım İlkeleri
Hidroksiüre + asetil salisilik asit tedavisine dirençli olduğu yada hidroksiüre ile
dirençli sitopeni (anemi ve/veya lökopeni) geliştiği belgelenen, yüksek vasküler risk taşıyan
esansiyel trombositemi hastalıklarında erişkin/çocuk hematoloji veya onkoloji uzmanının
bulunduğu sağlık kurulu raporu mevcudiyetinde adı geçen branş uzmanları tarafından reçete
edilebilir.
12.7.22. Aktive Protein C (Xigris) Kullanım İlkeleri
Yoğun bakım ünitelerinde, en az üç uzman hekim (Anestezi ve reanimasyon,
enfeksiyon hastalıkları, iç hastalıkları, göğüs hastalıkları, genel cerrahi) onayı ile, en az iki
organ yetmezliği gelişmiş ağır sepsis hastalarının tedavisinde, ilk 48 saat içerisinde, hastalığın
teşhisi, günlük kullanım dozu ve süresini belirten onaylı epikriz raporuna dayanılarak
yazılabilecektir (24 µg/kg/saat IV x 96 saat). Yeniden kullanım gerektiğinde bir önceki
verilen ilacın kullanıldığının yeni düzenlenecek raporda belirtilmesi ve bu raporda da
hastalığın teşhisi, günlük kullanım dozu ve süresinin kayıtlı olması gereklidir.
12.7.23. Amfoterisin-B ve Kaspofungin ve Vorikanozol Kullanım İlkeleri
Hastanın böbrek ve karaciğer fonksiyonları normal ise ilk tercih klasik amfoterisinB veya fluconazol’dür.
Klasik amfoterisin-B'ye alerjik reaksiyon gösterdiğinin resmi sağlık kurulu
raporuyla belgelenmesi yada hastanın karaciğer veya böbrek fonksiyon testlerinin laboratuar
verileri ile bozuk olduğunun klinik olarak belgelenmesi hallerinde, raporda belirtilen
lipozomal veya lipid kompleks amfoterisin-B veya kaspofungin veya vorikanazol
kullanılabilecektir.
Kaspofungin, vorikanazol, lipozomal amfoterisin-B ve lipid kompleks amfoterisinB’nin parenteral formları EHU onayı ile mutlak surette yatarak tedavide kullanılabilir. Bu
ilaçların oral formları ise yine EHU onayı ile ayaktan tedavide de kullanılabilecektir.
12.7.24. Solunum Sistemi Hastalıkları İlaçları Kullanım İlkeleri
Bu grup ilaçların ayaktan tedavide kullanımı aşağıdaki ilkelere göre yapılacaktır.
1. Astım tedavisinde;
Formeterol, salmeterol ve kombinasyonları, reçeteye göğüs hastalıkları, göğüs
cerrahisi, alerji, iç hastalıkları, çocuk sağlığı ve hastalıkları uzman hekimleri tarafından
yazılacaktır. Bu uzman hekimlerden en az birinin bulunduğu resmi sağlık kurulu raporu
mevcut ise tedavinin devamı için diğer hekimlerce de yazılabilecektir.
Montelukast, zafirlukast, reçeteye iç hastalıkları, çocuk hastalıkları göğüs
hastalıkları ve alerji uzman hekimleri tarafından yazılacaktır. Bu uzman hekimlerden en az
birinin bulunduğu resmi sağlık kurulu raporu mevcut ise tedavinin devamı için diğer
hekimlerce de yazılabilecektir.
2. KOAH tedavisinde;
Formeterol, salmeterol ve tiotropium, reçeteye göğüs hastalıkları, göğüs cerrahisi, iç
hastalıkları, çocuk hastalıkları ve kardiyoloji uzman hekimleri tarafından yazılacaktır. Bu
uzman hekimlerden en az birinin bulunduğu resmi sağlık kurulu raporu mevcut ise tedavinin
devamı için diğer hekimlerce de yazılabilecektir.
Formeterol ve salmeterol’ün inhaler kortikosteroidlerle kombinasyonları, reçeteye
iç hastalıkları, çocuk hastalıkları, göğüs hastalıkları ve göğüs cerrahisi uzman hekimleri
tarafından yazılacaktır. Bu uzman hekimin bulunduğu resmi sağlık kurulu raporu mevcut ise
tedavinin devamı için diğer hekimlerce de yapılabilecektir.
3. Mevsimsel alerjik rinit tedavisinde:
Montelukast kulak burun boğaz uzman hekimleri tarafından yazılabilecektir.
12.7.25. Antiepileptik İlaçların Epilepside Kullanım İlkeleri:
Sağlık Bakanlığı tarafından psikiyatrik hastalıklarda onaylı endikasyonu olan antiepileptikler, bu
tanılarda psikiyatri uzmanları tarafından reçete edilebilir. Ayrıca psikiyatri uzmanının bulunduğu sağlık
kurulu raporu mevcudiyetinde tüm hekimler tarafından reçete edilebilir
Gabapentin, pregabalin, lamotrigin, topiramat, vigabatrin, levatirasetam, ve bunun gibi
yeni nesil antiepileptikler nöroloji (erişkin ve çocuk), fizik tedavi ve rehabilitasyon, çocuk
hastalıkları veya nöroşirurji uzman hekimleri tarafından yazılacaktır. Bu uzman hekimlerden
birinin bulunduğu, kullanılacak ilacın etken maddesi, kullanım dozu ve süresini belirten sağlık
kurulu raporu mevcut ise diğer hekimlerce de reçeteye yazılabilecektir.
12.7.26. Levosimendan Kullanım İlkeleri
Akut kalp yetmezliği, dekompanse kalp yetmezliğinin akut döneminde yatan
hastalara;
- Öncelikle hastane eczanesinden temin edilir. Hastane eczanesinden temini
mümkün olmazsa, sözleşmeli eczaneden yatan hasta reçetesiyle temin edilir ve mükerrer
ödeme yapılmaması için hastane faturasında bu ilacın olmadığının kontrolü gerekir.
- İnvaziv hemodinamik monitarizasyon yapılabildiği yoğun bakım ünitelerinde,
- Kardiyoloji, kalp damar cerrahisi, anestezi ve reanimasyon ile acil uzman
hekimleri tarafından,
kullanılabilecektir.
12.7.27. Faktör ve Diğer Kan Ürünlerinin Reçete Edilme İlkeleri
A ) Faktörler
Hastanın tanısı, faktör düzeyi, varsa inhibitör düzeyini belirten hematoloji uzman
hekiminin imzasının bulunduğu sağlık kurulu raporuna dayanılarak;
- Akut kanaması olduğu durumlarda yada cerrahi girişimler öncesi,
- Faktör düzeyi % l'in altında ve/veya ayda üçten fazla kanaması olan hastalarda
proflaksi endikasyonu konulduktan sonra haftalık faktör kullanım miktarı 4500 üniteyi
geçmediği taktirde Sağlık Bakanlığı tarafından verilen hastaya özel Hemofili Takip Karnesine
yazılarak verilecektir.
Haftalık faktör kullanımının 4500 üniteyi geçmesi gerektiği durumlarda ayrıca bu
durumu belirten yeni bir sağlık kurulu raporu düzenlenecektir.
Acil müracaatlarda; hastanın tam teşekküllü resmi sağlık kurumlarına başvurması
halinde, Hemofili Takip Karnesinin mevcut olmaması veya bu belge mevcut, ancak ilaçta doz
arttırılmasını gerektirecek yeni bir endikasyonun gelişmesi halinde ilk mesai gününde raporun
çıkarılması, reçete veya tabela üzerinde bu durumun hekimin el yazısı ile belirtilmesi
koşuluyla, hastanın tedavisi sağlanacaktır.
Acil durumlarda hastaya en fazla bir günlük dozda ilaç yazılarak hematoloji uzman
hekiminin bulunduğu tam teşekküllü bir hastaneye sevk edilecektir.
Faktör VIIa, hastanın tanısı, faktör düzeyi, varsa inhibitör düzeyini belirten
hematoloji uzman hekiminin imzasının bulunduğu sağlık kurulu raporuna dayanılarak; yatan
hastalarda endikasyonları belirtilen dozlar doğrultusunda günde 3 doz veya bu hastaların
opere edilmesi halinde ise 12 doza kadar uzman hekim tarafından reçete edildiği taktirde geri
ödenir.
B ) Anti Rh Kullanım İlkeleri
a) Doğum Sonu Kullanım;
Doğum belgesi, anne-bebek kan grubu belgesi, Direkt Coombs testi negatifliğini
gösteren belge ve Anti Rh reçetesine dayanılarak verilecektir.
b) Düşük veya küretaj sonrası kullanımı;
Resmi ve anlaşmalı sağlık tesisinde annenin ve babanın kan grubu belgesi, düşük
veya küretaj olduğuna dair bir sağlık kuruluşunun belgeleri ekinde Anti Rh reçetesine
dayanılarak verilecektir.
c) Antenatal Kullanım;
Anne-baba kan grubu belgeleri ve İndirekt Coombs testi negatifliğini gösteren belge
ile sağlık kurulu raporunda doz ve kullanım süresi belirtilerek verilecektir.
d) Idiopatik (İmmün) Trombositopeni’de Kullanımı:
İntravenöz formu Rh pozitif ve splenektomisiz hastalarda resmi sağlık kurulu
(erişkin veya pediatrik hematoloji uzman hekiminin bulunacağı) raporunda doz ve kullanım
süresi belirtilerek verilebilir. Reçeteler hematoloji uzman hekimince düzenlenecektir.
C ) Antitrombin III Kullanım İlkeleri
Hastalığın tanısı, günlük kullanım dozu ve süresini belirten resmi sağlık kurulu
(erişkin veya pediatrik hematoloji uzman hekiminin bulunacağı) raporuna dayanılarak en
fazla 3 günlük dozda verilebilecektir. Yeniden kullanımı gerektiğinde bir önce verilen ilacın
kullanıldığının yeni düzenlenecek raporda belirtilmesi ve bu raporda da hastalığın tanısı,
günlük kullanım dozu ve süresinin kayıtlı olması gereklidir.
D) Human Albumin kullanım İlkeleri
Human albümin preparatları yalnızca yatarak tedavi gören hastalara, albümin
düzeyi 2.5g/dl ve altında ise uzman hekimlerce yazılabilir, laboratuar sonuçları ve kullanılan
miktar epikrizde belirtilecektir. Hastane eczanesinde bulunmadığı durumlarda, günlük doz ve
tedavi protokolünü ve kan albümin düzeyinin 2.5g/dl ve altında olduğunu gösterir sağlık
kurulu raporuna dayanılarak en fazla 3 (üç) günlük dozda verilecektir. Plazmaferezde kan
albümin düzeyi şartı aranmaz.
E) Bu maddede yer alan faktörler ile diğer kan ürünlerinin reçetelenmesinde bu
Tebliğin 18.2 inci maddesinde belirtilen koşullara da uyulacaktır.
12.7.28. Viskosuplemantasyon Ürünleri Kullanım İlkeleri
Bu ürünler her bir diz eklemi için yılda bir kürden (1 kür tedavi birer hafta arayla 3
doz uygulamayı kapsar) fazla uygulanamaz. Ortopedi, fizik tedavi ve rehabilitasyon,
romatoloji ve immünoloji uzman hekimlerince reçete edilecektir. Aynı diz eklemi için 3
kürden fazla uygulama yapılmaz.
12.7.29. Kadın Cinsiyet Hormonları Kullanım İlkeleri
Bu grup ilaçların bütün formlarından;
1. Östrojenler ve hormon replasman tedavisinde kullanılanlar
- Östradiol yada konjüge östrojen ve progestojen kombinasyonları
- Yalnız östrojen içerenler
- Tibolon içerenler.
2. Progestojenler,
Kadın hastalıkları ve doğum, iç hastalıkları, ortopedi, fizik tedavi ve rehabilitasyon
ve aile hekimi uzmanları tarafından ve sağlık kurulu raporuna istinaden tüm hekimlerce
yazılabilir.
12.7.30. Pulmoner Hipertansiyonda Iloprost trometamol (İnhaler Formu) ve Bosentanın
Kullanım İlkeleri:
a) Hastaların fonksiyonel kapasiteleri NHYA sınıf III ve IV olmalı,
b) Kalsiyum kanal blokeri ile yapılan vazodilatasyon testi başarısız ( etkisiz olmalı),
c) Üçüncü aylık tedavi sonrası kontrolünde klinik efor kapasitesi (6 dakika yürüme
testi veya treadmil efor testi), hemodinami veya ekokardiyografik verilerinde düzelme olması
gerekmektedir. Ayrıca yine üçüncü ay kontrolünde PAB (Pulmoner arteryel basınç)'ta azalma
olmaması (PAB'ın değişmemesi veya artması) halinde ve yukarıdaki verilerde düzelme
olmaması halinde tedavi sonlandırılmalıdır. Uygulanacak tedavi 3'er aylık periyotlar halinde
yukarıda açıklanan hususlar doğrultusunda sağlık kurulu raporunda belgelenecektir.
d) İlgili ilaçlar kardiyoloji, kardiyovasküler cerrahi, göğüs hastalıkları, pediyatrik
kardiyoloji uzman hekimlerinden birinin düzenlediği sağlık kurulu raporu ile adı geçen
hekimlerce reçete edilebilecektir. Bu koşullar yatan hastalar için de geçerlidir.”
12.8. Sağlık Bakanlığı (İlaç ve Eczacılık Genel Müdürlüğü) Bilimsel Komisyonları tarafından
herhangi bir ilaçla ilgili “Güvenlik ve Endikasyon Formu” geliştirilmiş ise ilgili ilacın geri
ödenmesi için söz konusu formun doldurulması ve gereken imzaların tamamlanması ve bir
örneğinin reçeteye eklenmesi gerekmektedir.
EK-2
HASTA KATILIM PAYINDAN MUAF İLAÇLAR LİSTESİ
1. Tüberküloz
1.1. Anti-tüberküloz ilaçlar
1.2. Antibiyotikler (çoklu ilaç direnci olan tüberkülozlar)
1.2.1. Kanamisin
1.2.2. Amikasin
1.2.3. Siprofloksasin
1.2.4. Ofloksasin
1.2.5. Levofloksasin
1.2.6. Moksifloksasin
1.2.7. Gatifloksasin
1.2.8. Amoksisilin/klavunat
1.2.9. Klaritromisin
1.2.10. Rifapentin
1.2.11. Linezolid
1.2.12. Azitromisin
1.2.13. Roksitromisin
1.3. Kapreomisin
1.4. Klofazimin
1.5. Kortikosteroidler
1.6. Tiosemikarbazon ve Türevleri
1.7. Viomisin
2. Kanser
2.1. Analjezikler ve Narkotik Analjezikler
2.2. Antineoplastik İlaçlar
2.3. İmmünglobulin Preparatları
2.4. İmmünsupressifler
2.5. Kanser tedavisi sırasında ortaya çıkan yan etkileri önlemek amacıyla kullanılan ilaçlar
2.6. Oral ve Enteral Beslenme Ürünleri
2.7. Radyofarmasötik Müstahzarlar
2.8. Bunların Uygulanması ile İlgili Parenteral Sıvılar, Antidotlar, Antiemetikler ve Aşılar
2.9. Parenteral Beslenme Ürünleri
2.10. LH-RH analogları
3. Kronik Böbrek Hastalıkları, Organ ve Doku Nakli Nakli
3.1. Antiagreganlar
3.2. Antianemik İlaçlar
3.3. Antihipertansifler
3.4. Antimikotik
3.5. Antiviral İlaçlar
3.6. Asit, Baz, Elektrolit, Kalsiyum ve Fosfat Dengesini Sağlamaya Yönelik İlaçlar,
Parenteral Sıvılar
3.7. Diüretik İlaçlar
3.8. Esansiyel Amino Asitler
3.9. İmmünglobulinler
3.10. İmmünsupresif ilaçlar
3.11. Kolşisin
3.12. Kortikosteroidler
3.13. Kronik Böbrek Yetmezliğine Eklenen Piyelonefrit ve Peritonitte Kullanılan
Antibiyotikler
3.14. Periton Diyaliz Solüsyonları
3.15. Aktif D Vitaminleri ve Metabolitleri
3.16. Antikoagülanlar (sadece organ ve doku naklinde)
3.17. Oral, Enteral ve Parenteral Beslenme Solüsyonları
3.18. Karnitin (sadece hemodiyaliz uygulanan hastalarda)
4. Uzun Süreli Kalp ve Damar Hastalıkları
4.1. Kalp Yetmezliği
4.1.1. ACE İnhibitörleri ve Kombinasyonları
4.1.2. Digoxin
4.1.3. Angiotensin Reseptör Blokerleri ve Kombinasyonları
4.1.4. Antiagreganlar
4.1.5. Beta Blokerler
4.1.6. Diüretikler
4.1.7. Nitratlar
4.1.8. Vasodilatatörler
4.1.9. Alfa Beta Reseptör Blokerleri
4.2. Koroner Arter Hastalığı
4.2.1. ACE İnhibitörleri ve Kombinasyonları
4.2.2. Antiagregan İlaçlar
4.2.3. Beta Blokerler
4.2.4. Kalsiyum Kanal Blokerleri
4.2.5. Kolesterol ve Lipid Düşürücüler
4.2.6. Nitratlar (uzun ve kısa etkili)
4.2.7. Antikoagülanlar
4.2.8. Alfa Beta Reseptör Blokerleri
4.2.9. Anjiotensin Reseptör Blokerleri ve Kombinasyonları
4.2.10.Trimetazidin HCl
4.3. Disritmiler
4.3.1. Antiaritmik İlaçlar
4.3.2. Antiagreganlar
4.3.3. Antikoagülanlar
4.3.4. Digoxin
4.4. Periferik ve Serebral (Serebrovasküler) Damar Hastalıkları, Venöz yetmezlikler
4.4.1. Antiagreganlar
4.4.2. Antikoagülanlar
4.4.3. Periferik ve Serebral Damar Düzenleyiciler
4.5. Arteriyel Hipertansiyon
4.5.1. Adrenerjik Nöron Blokerleri
4.5.2. Alfa Adrenerjik Reseptör Blokerleri
4.5.3. Alfa - Beta Reseptör Blokerleri
4.5.4. Angiotensin Dönüştürücü Enzim İnhibitörleri ve Reseptör Blokerleri (Kombine
şekilleri dahil)
4.5.5. Antiagreganlar
4.5.6. Beta Adrenerjik Reseptör Blokerleri
4.5.7. Diüretikler
4.5.8. İmidazolin Reseptör Agonistleri
4.5.9. Kalsiyum Antagonistleri
4.5.10. Santral Etkili Vasodilatatörler
4.6. Doğuştan Kalp Hastalıkları
4.6.1. Antiagreganlar
4.6.2. Antikoagülanlar
4.7. Akut Romatizmal Ateş (ARA) ve Kapak Hastalıkları
4.7.1. Antiagreganlar
4.7.2. Asetil Salisilik Asit (pediatrik yaş grubunda efervesan formları dahil)
4.7.3. Kortikosteroidler
4.7.4. Antikoagülanlar
4.7.5. Antiaritmikler
4.7.6. Digoxin
4.7.7. Beta Blokerler
4.7.8. Angiotensin Reseptör Blokerleri ve Kombinasyonları
4.7.9. ACE İnhibitörleri ve Kombinasyonları
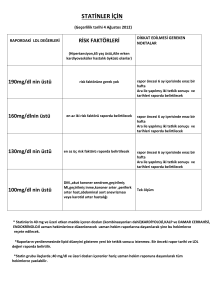
4.8. Hiperkolesterolemi, Hiperlipidemi
4.8.1. Fibrik Asit Türevleri
4.8.2. Niasin
4.8.3. Reçineler (Kolestramin)
4.8.4. Statinler
4.8.5. Ezetimib
4.9. Kardiyomiyopati
4.9.1. ACE İnhibitörleri ve Kombinasyonları
4.9.2. Angiotensin Reseptör Blokerleri ve Kombinasyonları
4.9.3. Antikoagülanlar
4.9.4. Antiagreganlar
4.9.5. Antiaritmikler
4.9.6. Beta Blokerler
4.9.7. Diüretikler
4.9.8. Nitratlar
4.9.9. Vasodilatatörler
4.9.10. Digoxin
4.9.11. Alfa Beta Reseptör Blokerleri
4.9.12. Kalsiyum Kanal Blokerleri
4.10. Pulmoner Hipertansiyon
4.10.1. Alfa Adrenerjik Blokerler
4.10.2. Antikoagülanlar
4.10.3. Vasodilatatörler
4.10.4. İloprost trometamol (sadece inhaler formu)
4.11. Reynaud Hastalığı
4.11.1. Alfa Adrenerjik Blokerler
4.11.2. Kalsiyum Kanal blokerleri
4.12. Pulmoner Tromboemboli
4.12.1. Antikoagülanlar
5. Solunum Sistemi Hastalıkları:
5.1. Astım
5.1.1. Antiastmatikler
5.1.2. Bronkodilatatör Ajanlar
5.1.2.1. Beta 2 Agonistler (kombinasyonları dahil)
5.1.2.2. Teofilin grubu (kombinasyonları dahil)
5.1.2.3. Antikolinerjikler (kombinasyonları dahil)
5.1.3. Antiinflamatuar Ajanlar
-Kromolin ve Tuzları
-Kortikosteroid Ajanlar
-Lökotrien Reseptör Antagonistleri
5.2. Kronik Obstrüktif Akciğer Hastalıkları
5.2.1. Bronkodilatatör Ajanlar
5.2.1.1. Beta 2 Agonistler (kombinasyonları dahil)
5.2.1.2. Teofilin grubu (kombinasyonları dahil)
5.2.1.3.Antikolinerjikler (kombinasyonları dahil)
5.2.2. Kortikosteroid Ajanlar
5.2.3.Diprofilin
5.3. Difüz İntertisiyel Akciğer Hastalıkları
5.3.1. İmmünsupresifler
5.3.2. Kortikosteroidler
5.3.3. Sitostatik Ajanlar
5.3.4. Beta 2 Agonistler, Teofilin grubu
5.4. Bronşektazi
5.4.1. Ekspektoranlar
5.4.2. Mukolitikler
5.4.3. Bronkodilatatörler (kombine şekilleri hariç)
5.5. Akciğer Kist Hidatiği
5.5.1. Albendazol
5.5.2. Mebendazol
6. Gastrointestinal Sistem Hastalıkları
6.1. Hepatit B, C, D ve Otoimmün Hepatit
6.1.1. Antiviral ajanlar
6.1.2. Azothioprine
6.1.3. Diüretikler
6.1.4. Hepatit-B İmmünglobulini
6.1.5. İnterferon
6.1.6. Kortikosteroidler
6.1.7. Ursodeoksikolikasit
6.2. Ailevi Akdeniz Ateşi (FMF)
6.2.1. Kolsisin
6.3. İnflamatuar Barsak Hastalıkları:
6.3.1. İmmünsupresifler
6.3.2. İnterferon
6.3.3. Kortikosteroidler
6.3.4. Mesalazin
6.3.5. Olsalazin
6.3.6. Salisilazosulfapiridin
6.3.7. İnfliksimab (sadece Chron Hastalığında)
6.3.8. Parenteral beslenme solüsyonları
6.4. Kronik Karaciğer Hastalıkları
6.4.1. Diüretikler
6.4.2. Ursedeoksikolikasit
6.5. Koroziv Gastrointestinal Yanıklar
6.5.1. Beslenme Ürünleri
(Koroziv Gastrointestinal yaralanmalar, travmatik veya cerrahi sonucu oluşan maksilofasial
defektler, nörolojik yutma bozuklukları vb nedenlerle yutma fonksiyonunun olmaması
durumunda mevcut durum düzelinceye kadar katkı payından muaf verilir.)
6.6. Wilson Hastalığı
6.6.1. D-penisillamin
6.6.2. Çinko preparatları
6.6.3. Trientine Hidrokloride
6.7. Ekzokrin Pankreas Bozuklukları
6.7.1. Enzim Preparatları
7. Endokrin Sistem Hastalıkları
7.1. Hipotalamus-Hipofiz Hastalıkları
7.1.1. Hipofiz Yetmezliği
7.1.1.1. Büyüme Hormonu
7.1.1.2. Kortikosteroidler
7.1.1.3. Tiroid Hormonları
7.1.2. Hipogonadizm
7.1.2.1. FSH, LH ve FSH-LH Kombine Preparatları
7.1.2.2. Koryonik Gonadotropinler
7.1.2.3. Gonodal Steroidler
7.1.3. Diabetes İnsipitus
7.1.3.1. Pitressin ve Sentetikleri
7.1.4. Hipofiz Hormon Fazlalığı (Akromegali, Hiperprolaktinemi)
7.1.4.1. Somatostatin ve Analogları
7.1.4.2. Bromokriptin
7.1.4.3. Kabergolin
7.1.5. Puberte Prekoks
7.1.5.1. LH-RH Analogları
7.1.5.2. Anastrazole
7.1.5.3. Testelacton
7.2. Pankreas Hastalıkları
7.2.1. Diabetes Mellitus
7.2.1.1. İnsülin
7.2.1.2. Oral Antidiabetikler
7.2.1.3. Glucagon
7.2.2. Hiperinsülinemiye Bağlı Hipoglisemiler
7.2.2.1. Diazoxide
7.2.2.2. Somatostatin ve Analogları
7.3. Paratiroid Hastalıklar
7.3.1. Hipoparatiroidi
7.3.1.1. Kalsiyum Preparatları
7.3.1.2. Vitamin D ve Metabolitleri
7.3.2. Hiperparatiroidi
7.3.2.1. Kalsitonin
7.4. Adrenal Hastalıkları
7.4.1. Adrenal Yetmezliği
7.4.1.1. Lorenzo Yağı
7.4.1.2. ACTH
7.4.1.3. Kortikosteroidler
7.4.1.4. Mineralokortikoidler
7.4.2. Adrenal Hiperfonksiyonu
7.4.2.1. Hiperaldosteronizm
7.4.2.1.1. Aldosteron Antagonistleri
7.4.2.1.2. Antihipertansifler
7.5. Kemik Hastalıkları
7.5.1. Rezistan Rickets ve Osteomalazi
7.5.1.1. Vit D ve Metabolitleri
7.5.1.2. Fosfat Preparatları
7.5.1.3. Kalsiyum Preparatları
7.5.2. Senil ve Postmenopozal Osteoporoz Haricinde;
Juvenil Osteoporoz, Kronik Steroid kullanımına bağlı oluşan Osteoporoz, Paget Hastalığı,
Osteogenezis İmperfekta, Osteokondrodisplazi; Sudek Atrofisi
7.5.2.1.Bifosfonatlar
7.5.2.2. Calcitonin
7.5.2.3. Kalsiyum Preparatları (C Vitamini ile Kombine Formları hariç)
7.5.2.4. Vit D ve Metabolitleri
7.6. Fosfor Metabolizması Bozuklukları
7.6.1. Vit D ve Metabolitleri
7.6.2. Fosfor Preparatları
7.7. Nöroendokrin Tümörler
7.7.1. Somatostatin ve Analogları
7.8. Hiperkalsiüri
7.8.1. Hidroklortiyazid
7.9 Tiroid Hastalıkları
7.9.1. Hipotiroidizm
7.9.1.1. Tiroid Hormonları
7.9.2. Hipertiroidizm
7.9.2.1. Propilthiouracil
7.9.2.2. Beta Blokerler
8. Kan Hastalıkları
8.1. Hastalıklar
8.1.1. Aplastik Anemi, Hipoplastik Anemi
8.1.2. Hemolitik Anemiler
8.1.2.1. Non-İmmün Hemolitik Anemi
8.1.2.2. Otoimmün Hemolitik Anemi
8.1.2.3. Paroksismal Noktürnal Hemoglobinuri
8.1.2.4. Trombotik Trombositopenik Purpura
8.1.3. Hemoglobinopatiler
8.1.3.1. Orak (sickle cell) Hücre Anemiler
8.1.3.2. Talasemiler
8.1.4. Kronik Miyeloproliferatif Hastalıklar
8.1.4.1. Kronik Miyelositik Lösemi
8.1.4.2. Miyelofibrozis
8.1.4.3. Polistemia Vera
8.1.4.4. Primer Trombositemi
8.1.5. Miyelodisplastik Sendrom
8.1.6. Akut ve Kronik Lösemiler
8.1.7. Non-hodgkin Lenfoma
8.1.8. Herediter Hemorajik Telenjiektazi
8.1.9. Hodgkin Hastalığı
8.1.10. Multiple Miyeloma ve Plazma Hücre Diskrazileri
8.1.11. Trombositopeni
8.1.12. Nötropeni
8.1.13. Faktör Noksanlıklarına Bağlı Hastalıklar (Hemofililer)
8.1.14. İmmün Yetmezlik
8.1.14.1. Agamaglobulinemi, Hipogamaglobulinemi
- Hiper IgM Sendromu, Kombine İmmün Yetmezlik
8.1.15. Prematüre Anemisi
8.1.16. Primer ve sekonder trombofili olan hastalar
8.1.17. Histiositoz
8.2. Yalnızca bu hastalıkların tedavisine yönelik kullanılan ilaçlar
8.2.1. Hemapoetik Büyüme Faktörleri (Sağlık Bakanlığınca izin verilen endikasyon dışında
kullanımı ancak Sağlık Bakanlığınca verilen onayla mümkün olacaktır)
8.2.2. Şelatörler (Sağlık Bakanlığınca izin verilen endikasyon dışında kullanımı ancak Sağlık
Bakanlığınca verilen onayla mümkün olacaktır)
8.2.3. Faktörler (Sağlık Bakanlığınca izin verilen endikasyon dışında kullanımı ancak Sağlık
Bakanlığınca verilen onayla mümkün olacaktır)
8.2.4. Antikoagülanlar
8.2.5. İmmünomodülatörler (Sağlık Bakanlığınca izin verilen endikasyon dışında kullanımı
ancak Sağlık Bakanlığınca verilen onayla mümkün olacaktır)
8.2.6. Analjezikler ve Narkotik Analjezikler
8.2.7. Antibiyotikler – (hastanın ayaktan tedavisinde heyet raporunda belirtilenler
dışındakiler muaf değildir)
8.2.8. Antineoplastik ilaçlar
8.2.9. Antiviral ilaçlar – (hastanın ayaktan tedavisinde heyet raporunda belirtilenler
dışındakiler muaf değildir)
8.2.10. İmmünglobulin preparatları
8.2.11. İmmünsupresifler
8.2.12. Kanser Tedavisi Sırasında Ortaya Çıkan Yan Etkileri Önlemek Amacıyla Kullanılan
İlaçlar
8.2.13. Oral ve Enteral Beslenme Ürünleri
8.2.14. Radyofarmasötik Ürünler
8.2.15. Bunların Uygulanması ile İlgili Parenteral Sıvılar, Antidotlar, Antiemetikler ve Aşılar
9. Konnektif Doku Hastalıkları
9.1. Hastalıklar
9.1.1. Sistemik Lupus Eritematozus ve İlişkili Sendromlar
9.1.2. Primer Antifosfolipid Antikor Sendromu
9.1.3. Vaskülitler
9.1.3.1. Churg Straus
9.1.3.2. Henoch Schonlein
9.1.3.3. Hipersensitivite vaskülitleri
9.1.3.4. Kawasaki
9.1.3.5. Poliarteritis Nodosa
9.1.3.6. Polimiyalji Romatika
9.1.3.7. Takayashu
9.1.3.8. Temporal arteritis
9.1.3.9. Wegener Granulomatozis
9.1.4. Skleroderma, Mikst Konnektif Doku Hastalığı
9.1.5. Romatoid Artrit ve İlişkili Sendromlar (Sjögren vb)
9.1.6. Seronegatif Spondilortropatiler
9.1.6.1. Andiferansiye Spondilortropati
9.1.6.2. Ankilozan Spondilit
9.1.6.3. Enteropatik Artropatiler
9.1.6.4. Psöriatik Artrit
9.1.6.5. Reiter
9.1.7. İnflamatuar Kas Hastalıkları
9.1.7.1. Dermatomiyozit
9.1.7.2. Polimiyozit
9.1.8. Kristal Artropatiler
9.1.9. Relapsing Polikondritis
9.2. Bu Hastalıkların Tedavisinde Kullanılan İlaçlar
9.2.1. 6-Merkaptopürin
9.2.2. Altın Preparatları
9.2.3. Antimalaryaller
9.2.4. Azatioprin
9.2.5. Dapson
9.2.6. D-Penisillamine
9.2.7. Klorambusil
9.2.8. Kortikosteroidler
9.2.9. Leflunomid
9.2.10. Methotreksate
9.2.11. Siklofosfamid
9.2.12. Siklosporin
9.2.13. Sulfasalazin
9.2.14. Anti TNF İlaçlar
9.2.15. İV İmmünglobulinler (Sadece Kawasaki Hastalığında)
10. Kronik Nörolojik Hastalıklar
10.1. Kas Hastalıkları
10.1.1. Miyopatiler
10.1.1.1. Kortikosteroidler
10.1.2. Mitokondriyal Sitopatiler
10.1.2.1. Karnitin
10.1.2.2. Coenzyme Q
10.1.3. Miyotoniler
10.1.3.1. Hidantoin
10.1.3.2. Karbamazepin
10.2. Nöromusküler Hastalıklar
10.2.1. Myasthenia Gravis
10.2.1.1. İmmünglobulinler
10.2.1.2. İmmünsupresif İlaçlar
10.2.1.3. Kortikosteroidler
10.2.1.4. Neostigmin
10.2.1.5. Pridostigmin
10.2.2. Motor Nöron (A.L.S)
10.2.2.1. Riluzole
10.3. Ekstrapiramidal Sistem Hastalıkları
10.3.1. Parkinson Hastalığı
10.3.1.1. Amantadin
10.3.1.2. Apomorfin
10.3.1.3. Artan v.b.
10.3.1.4. Benztropin
10.3.1.5. Biperidene
10.3.1.6. Bornaprin HCL
10.3.1.7. Bromokriptin
10.3.1.8. Cabergolin
10.3.1.9. Difenhidramin
10.3.1.10. Domperidon
10.3.1.11. Entakapon
10.3.1.12. L-Dopa+Benserazide
10.3.1.13. L-Dopa+Karbidopa ve Kombinasyonları
10.3.1.14. Lisurid
10.3.1.15. Nonergolin Dopa Agonistleri
10.3.1.16. Pergolid
10.3.1.17. Piribedil
10.3.1.18. Pramipeksol
10.3.1.19. Ropinirol
10.3.1.20. Selegilin Hidroklorid
10.3.2. Distoniler, Hemifasyal Spazm
10.3.2.1. Biperiden
10.3.2.2. Botulismus Toksini Tip A
10.3.2.3. Klonazepam
10.4. Epilepsi, Narkolepsi ve Febril Konvülsiyonlar
10.4.1. Asetezolamid
10.4.2. Benzodiazepinler
10.4.3. Ethosuksimide
10.4.4. Felbamat
10.4.5. Fenitoinler
10.4.6. Fenobarbital, Barbekselon
10.4.7. Flunerazin
10.4.8. Gabapentin
10.4.9. Karbamazepin
10.4.10. Klobazam
10.4.11. Klonazepam
10.4.12. Lamotrigin
10.4.13. Okskarbazepin
10.4.14. Pirimidon
10.4.15. Topiramate
10.4.16. Valproatlar
10.4.17. Vigabatrin
10.4.18. Zorasamide
10.4.19. Levatiracetem
10.4.20. Sultiam
10.4.21. Modafinil
10.5. Demiyelinizan Hastalıklar (Lökodistrofi, Multipl Skleroz v.b.)
10.5.1. Antiepileptikler
10.5.2. Baklofen
10.5.3. Copolimer I
10.5.4. İmmünglobulinler
10.5.5. İmmünsupresif İlaçlar
10.5.6. İnterferon
10.5.7. Kortikosteroidler
10.6. Subakut Sklerozan Panansafalit (SSPE) Hastalığı
10.6.1. Antiepileptikler
10.6.2. Antiviraller
10.6.3. İmmünglobulinler
10.6.4. İmmünsupresif ilaçlar
10.6.5. Sitostatikler
10.7. Demans
10.7.1. Donepezil
10.7.2. Rivastigmin
10.7.3. Antipsikotikler (Sağlık Bakanlığınca onaylı endikasyonu bulunanlar)
10.7.4. Galantamin
10.7.5. Memantin
10.8. Oral Beslenmenin Mümkün Olmadığı Kronik Nörolojik ve Kas Hastalıkları
10.8.1. Enteral Beslenme Ürünleri
10.9. Serebral Palsy
10.9.1. Baklofen
10.9.2. Botulinum Toksini (12.7.5.b ilkelerine göre)
10.10. Trigeminal Nevralji
10.10.1. Karbamazepin
10.10.2. Difenil Hidantoin
10.10.3. Oksikarbamazepin
10.11. Spastisite
10.11.1. Baklofen
10.11.2 Botulinizm Toksin A (fokal spastisitede)
10.12. Nöropatik Ağrı
10.12.1. Gabapentin (sadece diabetik nöropati ve postherpetik nöraljide)
10.12.2. Karbamazepin
11. Psikiyatrik Hastalıklar
11.1. Genel Tıbbi Duruma Bağlı Mental Bozukluklar
11.1.1. Antidepresanlar
11.1.2. Antiepileptikler (Sağlık Bakanlığınca onaylı endikasyonu bulunanlar)
11.1.3. Antipsikotikler
11.1.4. Biperiden
11.1.5. Lityum
11.2. Demans
11.2.1. Donepezil
11.2.2. Rivastigmin
11.2.3. Antipsikotikler (Sağlık Bakanlığınca onaylı endikasyonu bulunanlar)
11.2.4. Galantamin
11.2.5. Memantin
11.3. Şizofreni, Şizoaffektif Bozukluk, Sanrısal Bozukluk, Atipik Psikoz, Şizofreniform
Bozukluk, Bipolar Mizaç Bozukluğu
11.3.1. Antidepresanlar
11.3.2. Antiepileptikler (Sağlık Bakanlığınca onaylı endikasyonu bulunanlar)
11.3.3. Antipsikotikler
11.3.4. Biperiden
11.3.5. Lityum
11.4. Anksiyete Bozuklukları (Panik Bozukluk, Sosyal Fobi, Obsesif-Kompulsif Bozukluk,
Travma Sonrası Stres Bozukluğu, Yaygın Anksiyete Bozukluğu, Somatoform
Bozukluk,Yeme Bozuklukları, Depresyon [= Unipolar, Bipolar], Distimik Bozukluk)
11.4.1. Antidepressanlar
11.4.2. Antiepileptikler (Sağlık Bakanlığınca onaylı endikasyonu bulunanlar)
11.4.3. Antipsikotikler
11.4.4. Biperiden
12. Göz Hastalıkları
12.1. Glokom
12.1.1. Bu Hastalıkta Kullanılan Tüm İlaçlar
12.2 Kronik ve Nükseden Üveitler, Tiroide Bağlı Oftalmopati ve Sempatik Oftalmi,
Keratoplasti Red Reaksiyonu
12.2.1. Siklosporin
12.2.2. Kortikosteroidler
12.3. Koroid Neovasküler Membranı Olan Tüm Makula Hastalıkları
12.3.1. Vertaporfin (Sağlık kurulu raporunda en az üç göz hastalıkları uzmanı imzası ile
hasta anamnezi, FFA ve renkli resim rapora eklenecek)
12.4. Kuru Göz Sendromu (Schimer testi 5 mm. ve altında olacak)
12.4.1. Suni Gözyaşları
12.4.2. Siklosporin Topikal Preparatları
13. Cilt Hastalıkları
13.1. Psoriasis,Vitiligo
13.1.1. Kalsipotriol
13.1.2. Kortikosteroidler
13.1.3. Methotreksate
13.1.4. Retinoidler
13.1.5. Siklosporinler
13.1.6. TNF Alfa Blokerleri (Yalnız Psoriazis Vulgariste)
13.2. Ichtiyosis
13.2.1. Retinoidler
13.2.2. Cildi Nemlendirici ve Yağlandırıcı Preparatlar
13.3. Pemfigus
13.3.1. Kortikosteroidler
13.3.2. İmmünsupresifler
13.4. Mukozis Fungoides
13.4.1Antineoplastik ajanlar (Sağlık Bakanlığı endikasyonlarında)
13.5. Hidraadenitis Suppurativa
13.5.1. Kortikosteroidler
13.5.2. Retinoidler
13.6. Epidermolysis Bullosa
13.6.1. Hidantoinler
13.6.2. Kortikosteroidler
13.6.3. Antibiyotikli Pomatlar
13.7. Liken
13.7.1. Siklosporin
13.7.2. Retinoidler
13.7.3. Kortikosteroidler
13.8. Pyoderma Gangronosum
13.8.1. Siklosporin
14. Enfeksiyon Hastalıkları
14.1. Hepatit B,C,D
14.1.1. İnterferon
14.1.2. Antiviral Ajanlar
14.1.3. Hepatit B İmmünglobulini
14.1.4. Azothioprine
14.1.5. Diüretikler
14.1.6. Ursodeoksikolikasit
14.2. AİDS (HIV)
14.2.1. Antiviraller
14.2.2. Antibakteriyeller
14.2.3. Antifungaller
14.2.4. Antituberküloz ilaçlar
15. Diğer Hastalıklar
15.1. Amiloidozis
15.1.1. Kolşisin
15.1.2. Kortikosteroidler
15.1.3. Melfalan
15.2. Behçet Hastalığı
15.2.1. Antikoagülanlar
15.2.2. İmmünsupresif İlaçlar (Sağlık Bakanlığınca izin verilen endikasyonlarda)
15.2.3. İnterferon
15.2.4. Kolşisin
15.2.5. Kortikosteroidler
15.3. Sarkoidosis
15.3.1. Kortikosteroidler
15.4. Doğuştan Metabolik ve Kalıtsal Hastalıklar ve Barsak Operasyonundan Dolayı Oluşan
Malabsorbsiyonlar ve Malnütrisyonlar. İlk iki yaşta inek sütü alerjisi
15.4.1. Enzim Preparatları ve Bu Grup Hastalıkların Tedavisine Yönelik Spesifik İlaçlar ve
Özel Formüllü Besleyiciler
15.4.2. Vitaminler
15.5. Kistik Fibrozis (Mukovizidozis)
15.5.1. Enzim Preparatları
15.5.2. Tobramisin İnhaler
15.6. Alerjik Hastalıklar
15.6.1. Yalnızca Arı Venom Alerjisi Aşıları
15.7. Kuduz Serumları
15.8. Hepatit-A Aşıları ve Hepatit B Serumları
15.9. Tetanoz Serumları
15.10. Radyopak Maddeler
15.11. Osteomiyelit
15.11.1. Antibiyotikler
15.12. Nörojenik Mesane
15.12.1. Tolterodine-L
15.12.2. Oksibutin
15.12.3. Trospium
15.13. Çölyak Hastalığı
15.13.1. Glutensiz Un ve Mamul Ürünler
15.14. RSV İmmünglobulini
NOT: Bu liste, ilaçların etken maddeleri dikkate alınarak düzenlenmiş olmakla birlikte
Bedeli Ödenecek İlaçlar Listesinde (EK-2/D) yer almayan herhangi bir ilacın ödenmesi veya
muafiyeti mümkün değildir.
EK-2/A
SİSTEMİK ANTİMİKROBİK VE DİĞER İLAÇLARIN REÇETELEME KURALLARI
Tedavi için gerekli görülen antibiyotikler, aşağıda belirtilen esaslara göre reçete edilecektir.
Aşağıdaki Listedeki kısaltma ve ibareler için liste sonunda “AÇIKLAMALAR” bulunmaktadır.
1-BETALAKTAM ANTİBİYOTİKLER
A) PENİSİLİNLER
1
KY
2
Amoksisilin
Amoksisilin-Klavulanat (Parenteral)
2.1
Amoksisilin-Klavulanat (Oral)
KY
3
Ampisilin
KY
4
Ampisilin Sulbaktam (Parenteral)
UH-P
4.1
Ampisilin Sulbaktam Oral
KY
5
Azidosilin
KY
6
Bakampisilin
KY
7
Mezlosilin
UH-P, A 72
8
Penisilin (Prokain, Benzatin, Kristalize, Pen V,
Fenoksimetil)
UH-P
KY
9
Piperasilin
UH-P, A 72
10
Piperasilin-Tazobaktam
EHU
12
Tikarsilin Klavulanat
EHU
13
Karbenisilin
UH-P, A 72
B) SEFALOSPORİNLER
1. Kuşak Sefalosporinler
14
Sefadroksil
KY
15
Sefaleksin
KY
16
Sefazolin
KY
17
Sefradin
KY
18
Sefalotin
KY
2. Kuşak Sefalosporinler
19
Sefaklor
KY
20
Sefoksitin
UH-P
21
Sefprozil
KY
22
Sefuroksim (Parenteral)
UH-P
22.1
Sefuroksim Aksetil
KY
23
Lorakarbef
KY
3. Kuşak Sefalosporinler
24
Sefiksim
KY
25
Sefodizim
UH-P
26
Sefoperazon
UH-P, A 72
27
Sefoperazon-Sulbaktam
EHU
28
Sefotaksim
UH-P, A 72
29
Seftazidim
UH-P, A 72
30
Seftizoksim
UH-P, A 72
31
Seftriakson
31/A Sefditoren
UH-P, A 72 APAT’TA
KY (bakınız 7/a)
KY
4. Kuşak Sefalosporinler
32
Sefepim
EHU
C) DİĞER BETALAKTAM ANTİBİYOTİKLER
Monobaktamlar
33
Aztreonam
UH-P, A 72
Karbapenemler
34
İmipenem
EHU
35
Meropenem
EHU
2-MAKROLİD VE LİNKOZAMİD GRUBU ANTİBİYOTİKLER
A) MAKROLİDLER
36
Azitromisin
KY
37
Diritromisin
KY
38
Eritromisin
KY
39.1
Klaritromisin Oral
KY
39.2
Klaritromisin MR
KY
39.3
Klaritromisin Paranteral
UH-P
40
Roksitromisin
KY
41
Spiramisin
KY
42
Treoleandomisin
KY
43
Telitromisin
KY
B) LİNKOZAMİDLER
44
Klindamisin
KY
45
Linkomisin
KY
46
Doksisiklin
KY
47
48
Tetrasiklin
Tetrasiklin – Nistatin
KY
KY
49
Oksitetrasiklin
KY
3- AMFENİKOLLER
50
Kloramfenikol
KY
51
KY
Tiamfenikol
4-AMİNOGLİKOZİD GRUBU ANTİBİYOTİKLER
52
Amikasin
UH-P
53
Gentamisin
KY
54
İsepamisin
EHU
55
Kanamisin ve Türevleri
KY
56
Neomisin ve Kombinasyonları
KY
57
Netilmisin
UH-P
58
Streptomisin
KY
59
Tobramisin Parenteral
UH-P
5-KİNOLON GRUBU ANTİBİYOTİKLER
60
Siprofloksasin Oral
KY
60.1
Siprofloksasin Parenteral
UH-P, A 72
61
Enoksasin
KY
62
Levofloksasin Oral
KY
62.1
Levfoloksasin Parenteral
UH-P, A 72
63
Norfloksasin
KY
64
Ofloksasin Oral
KY
64.1
Ofloksasin Parenteral
UH-P, A 72
65
Pefloksasin Oral
KY
65.1
Pefloksasin Parenteral
KY
66
Moxifloksasin Oral
KY
66.1
Moxifloksasin Parenteral
UH-P, A 72
67
Lomefloksasin
KY
68
ANTİSTAFİLOKOKAL
ANTİBİYOTİKLER
ANTİSTAFİLOKOKAL PENİSİLİNLER
Flukloksasilin
KY
69
Nafsilin
UH-P
6A)
B) GLİKOPEPTİD ANTİBİYOTİKLER
70
Vankomisin
71
Teikoplanin
72
Basitrasin
KY
73
Polimiksin B
KY
EHU**
EHU APAT’TA KY
(bakınız 7/b)
74
Kolistin ve Türevleri
KY
C) DİĞER ANTİSTAFİLOKOKAL ANTİBİYOTİKLER
75
Fusidik Asit ve Tuzları
KY
76
Mupirosin
KY
77
Linezolid
EHU
7- ANSAMİSİNLER
77
Rifabutin
UH-P
78
Rifamisin
KY
79
Rifampisin
KY
8- SULFONAMİD ANTİBİYOTİKLER VE TRİMETOPRİM
KOMBİNASYONLARI
80
Sulfisoxazole
KY
81
Sulfadiazin
KY
82
Sulfametoksipridazin
KY
83
Sulfametoksazol
KY
84
Trimetoprim
KY
85
Trimetoprim Sulfametoksazol
KY
9-ANTİANAEROBİK ETKİLİ ANTİBİYOTİKLER
86
Metronidazol Parenteral
KY
87
Metronidazol (üre kombinasyonları dahil)
KY
88
Ornidazol
KY
89
Seknidazol
KY
90
Tinidazol
KY
10-ANTİFUNGAL ANTİBİYOTİKLER
91
Amfoterisin B (Klasik)
UH-P, A 72
(madde 12.7.23.
92
Kaspofungin
esaslarına uygun
olarak)
93
Flukonazol Parenteral
UH-P, A 72
93.1
Flukonazol Oral ve Diğer Formları
KY
94
Itrakonazol
UH-P
95
Ketokonazol
KY
(madde 12.7.23.
96
Lipid Komplex Amfoterisin B
esaslarına uygun
olarak)
(madde 12.7.23.
97
Lipozomal Amfoterisin B
esaslarına uygun
olarak)
98
Terbinafin
KY
99
Griseofulvin
KY
(madde 12.7.23.
100
Varicanazole
esaslarına uygun
olarak)
101
Sertakonazole
KY
102
Nistatin (Tetrasiklinle kombine şekli dahil)
KY
103
Natamisin (Pimarisin)
KY
104
Mikonazol
KY
105
Oksikonazol
KY
106
İzokonazol
KY
11-ANTİVİRAL İLAÇLAR
A) HIV/AIDS TEDAVİSİNDE KULLANILAN SPESİFİK İLAÇLAR
107
Abacavir
EHU
108
Stavudin
EHU
110
Zalsitabin
EHU
113
İndinavir
EHU
114
Lamivudin 150mg (Zidovudin kombinasyonları
dahil)
EHU
115
Nevirapin
EHU
116
Ritonavir (Lopinavir kombinasyonları dahil)
EHU
117
Zidovudin (Lamivudin kombinasyonları dahil)
EHU
B) DİĞER ANTİVİRALLER
118
Asiklovir Oral
KY
118.1
Asiklovir Parenteral
EHU
119
Famsiklovir
UH-P
120
Gansiklovir
EHU
121
Valasiklovir
UH-P
122
Lamivudin 100 mg
UH-P
123
Ribavirin
UH-P
124
Didanozin
EHU
125
Efavirenz
126
Adefovir Entakavir
127
Zanamivir
UH-P
128
Oseltamivir
UH-P
129
Brivudine Oral
UH-P
EHU
(12.7.13. madde
esaslarına göre)
12-ANTİTÜBERKÜLOZ İLAÇLAR *
130
131
Etambutol (İzonikotinik Asit Hidrazidi ile
kombinasyonları dahil)
İzoniazid (B6 Vitamini, Rifampisin ve
Etambutol kombinasyonları dahil)
KY
KY
132
P-Aminosalisilik Asit ve Tuzları
UH-P
133
Pirazinamid
KY
134
135
Etionamid
Sikloserin
UH-P
UH-P
136
Tiasetazon
UH-P
137
Morfozinamid
KY
138
Protionamid
UH-P
139
Rifabutin
UH-P
140
141
Rifampisin
Streptomisin
KY
KY
* Tedavi başlangıcında UD veya Verem Savaş Dispanserlerinde yazılması durumunda ve
idamesinde KY
13- DİĞERLERİ
142
Üriner Antiseptikler
KY
Fosfomisin
143
KY
144
Nimesulid, Etodolak 400 mg
KY
145
Morfin, Petidin
UH-P
146
Rosiglitazon, Pioglitazon,
Glukagon, İnsulin
UH-P
AVANDIA TB
ROSENDA TAB
GLIFIX TAB
GLUCAGEN
ACTRAPID
HUMULIN, MIXTARD
ORGASULIN,
NOVOMIX
NOVORAPİD
LANTUS
INSULATARD
HUMALOG
147
Fenofibrat, Gemfibrozil,
Atorvastatin, Lovastatin,
Simvastatin, Fluvastatin,
Provastatin, Rosuvastatin,
Kolestramin
Amlodipin+Atorvastatin
LIPANTHYL, LIPOFEN
GEMFIBRIL, LOPİD
ATOR, KOLESTOR
LIPITAKSIN,
LIPITOR
SAPHIRE
TARDEN
LOVAKOR
MEVACOR
LIPOVAS
SİMVAKOL
ZOCOR
ZOVATİN
LESCOL
LESCOL XL
KOLESTRAN
Daha önce ilaç kullanmayan
hastalarda
ilaca
başlanma
kriterleri:
a) Statin dışındaki lipid düşürücü
ilaçlar,
trigiliserit
düzeyinin
300’ün
(Diabetes mellitus
hastalarında 150) üstünde olduğu
durumlarda,
b) Statinler için LDL düzeyinin
160’ın (Diabetes mellitus, akut
koroner sendrom ve geçirilmiş
MI’da 130) üstünde olduğu
durumlarda
sadece
(01x01)
dozda,
-Dahiliye, çocuk hastalıkları,
kardiyoloji,
kalp
damar
cerrahisi, nöroloji ile aile
hekimliği uzman hekimlerinden
birinin
düzenlediği,
ilaca
başlama kriterlerinin belirtildiği
ilaç
kullanım
raporuna
dayanılarak iki yıl süreyle tüm
hekimlerce,
-Raporsuz
reçete
edilmesi
halinde ise, tüm hekimlerce her
altı ayda bir yapılan tetkik
sonuçlarının bir örneğinin her
reçeteye eklenmesi kaydıyla
yazılır.
İlaç tedavisi altındaki hastalarda
ilaç kesilme kriterleri (istenmeyen
etkiler hariç):
-LDL düzeyinin; yukarıda “b”
bendinde belirtilen hastalıkları
olan
hastalar
haricindeki
kişilerde, 100’ün altına düşmesi
halinde kesilir.
-Yukarıda
“b”
bendinde
belirtilen
hastalıkları
olan
hastalarda
100’ün
altına
düştükten sonra idame doza
geçilmesini takiben devam
edilir veya kesilir.”
148
UH-P
Alfuzosin,Tamsulosin,
Terazosin
XATRAL , FLOMAX,
HYTRIN
149
İrbesartan, Kandesartan,
UH-P
Losartan, Telmisartan,
Valsartan, Rilmeniden,
Moksonidin, Olmesartan,
Eprosartan Mesilat
KARVEA, KARVEZİDE
ATACAND, AYRA
COZAAR, EKLİPS
SARVAS, MİCARDİS
PRİTOR, DİOVAN
CO-DİOVAN,
HYPERIUM
CYNT, PHYSIOTENS
150
Apomorfin
UH-P
151
Finasterid
UH-P
152/a
Esomeprazol, Rabeprazol
NEXIUM
PARIET
İki ay süreyle diğer proton
pompa inhibitörleri ile tedavi
görmesine rağmen iyileşme
sağlanamadığı ikinci ayın
sonundaki endoskopi raporuyla
belgelenen hastalarda; reçete
edilir. Altıncı ayın sonunda
hasta değerlendirilir ve
gerektiğinde, aynı protokole
göre tedavisi yapılır. Bu
hususlar reçetede belirtilir
152/b
UH-P
Pantoprazol
PANTPAS
PANTHEC
PANTO
PROTONEX
PULCET
ULCOREKS
153
Suni gözyaşı
154
Kortikosteroidli tek doz göz
damlaları
Göz hastalıkları uzman hekimi
veya bu hekimin bulunduğu heyet
raporuyla tüm hekimlerce
Göz hastalıkları uzman hekimi
veya bu hekimin bulunduğu heyet
raporuyla tüm hekimlerce
İç hastalıkları ve Çocuk
hastalıkları uzman hekimi veya
bu hekimlerden birinin bulunduğu
heyet raporuyla tüm hekimlerce
Psikiyatri uzmanı veya bu
hekimin bulunduğu heyet
raporuyla tüm hekimlerce
UH-P
155
Oksimetolon
156
Disülfiram
157
Kabergolin
158
Kenodoksikolik Asit
159
Entakapon ve
kombinasyonları, rasajilin
160
Allantoin + heparin +
excractum cepae
161
Demir-Dextran
UH-P
162
Deferoksamin metansülfonat
163
Lizürid Maleat
İç hastalıkları, Çocuk hastalıkları
uzman hekimi veya bu
hekimlerden birinin bulunduğu
heyet raporuyla tüm hekimlerce
UH-P
165
Amifostin
166
Üre içeren preparatlar
167
Fondaparinux
168
Deferipron
İç hastalıkları ve Genel cerrahi
uzmanı veya bu hekimlerden
birinin bulunduğu heyet raporuyla
tüm hekimlerce
Nöroloji uzmanı tarafından veya
bu uzmanın bulunduğu sağlık
kurulu raporu ile tüm hekimlerce
UH-P
Kemoterapi ve radyoterapide
raporla
UH-P , Sadece ihtiyozis veya
kseroderma endikasyonlarında
ödenir.
Ortopedi uzmanınca
Kollojen
Erişkin veya Çocuk Hematoloji
uzmanının bulunduğu sağlık
kurulu raporu ile tüm hekimlerce
UH-P
8- Metoksipsoralen
UH-P
İloprost trometamol
(İntravenöz formları)
Üniversite, Eğitim ve Araştırma
Hastanelerinde tanıyı doğrulayan
resmi kurumca onaylanmış
görüntüleme tetkik raporları
eklenmiş; Ortopedi, Genel
Cerrahi, Kardiyoloji ve Çocuk
Kardiyoloji veya Kalp Damar
Cerrahi Uzman Hekimlerinden
birinin bulunduğu sağlık kurulu
raporu ile yalnızca Sağlık
169
170
171
Modafinil
Bakanlığınca izin verilen
endikasyonlarda kullanılabilir.
UH-P
172
Pergolid mezilat
173
Pramipexol Hidroklorür
174
Bornaprin Hidroklorür
175
Dornaz alfa
176
Ranitidin Bizmut Sitrat
Nöroloji uzmanı veya bu uzmanın
bulunduğu heyet raporu ile tüm
hekimlerce
Nöroloji uzmanı veya bu uzmanın
bulunduğu heyet raporu ile tüm
hekimlerce
Nöroloji uzmanının yer aldığı
heyet raporu ile tüm hekimlerce
Yalnızca kistik fibrozisli
hastalarda Eğitim ve Araştırma
Hastanelerinin verdiği heyet
raporu ile tüm hekimlerce
UH-P
177
Ropinirol
Nöroloji uzmanının yer aldığı
heyet raporu ile tüm hekimlerce
Tolterodine-L
Üroloji ve Nöroloji (erişkin ve
çocuk), pediatri, kadın doğum,
pediatrik cerrahi, FTR, geriatri
uzman hekimlerince reçete
edilebilir. Sağlık kurulu
raporlarında üroloji ve nöroloji
(erişkin ve çocuk) uzmanları
bulunmak zorundadır. Heyet
raporuyla tüm hekimlerce
yazılabilir.
UH-P
178
179
Oksibutinin
180
Trospiyum
181
Naferalin Asetat
182
Testosteron
183
Ursedoksikolik Asit
184
Demir III hidroksit Sükroz
Üroloji, Endokrin, Çocuk Cerrahi
Uzman hekimlerince veya bu
hekimlerden birinin bulunduğu
heyet raporuyla bütün hekimlerce
İç hastalıkları ve genel cerrahi
uzman hekimlerince veya bu
hekimlerden birinin bulunduğu
heyet raporuyla bütün hekimlerce
UH-P
185
Tagaserod maleat
186
Potasyum sitrat (5 mEq ve
187
2,4277 gram)
Gastroenteroloji veya İç
hastalıkları uzman hekimlerince
veya bu hekimlerden birinin
bulunduğu heyet raporuyla bütün
hekimlerce
Nefroloji ve üroloji uzman
hekimlerince, bu hekimlerin
bulunduğu ilaç kullanım raporu
ile tüm hekimlerce
188
İsotretinoin+Eritromisin
Sadece cilt hastalıkları uzman hekimlerince
189
Multivitamin Pronatal
Sadece gebelikte
191
Darifenasin
Üroloji ve nöroloji (erişkin ve çocuk), pediatri,
kadın doğum, pediatrik cerrahi, FTR, geriatri
uzman hekimlerince reçete edilebilir. Sağlık kurulu raporlarında üroloji ve nöroloji (erişkin ve
çocuk) uzmanları bulunmak zorundadır. Heyet raporuyla tüm hekimlerce yazılabilir.
NOT: Antibiyotiklerin topik formları bu hükümler dışındadır.
AÇIKLAMALAR:
1.
KY:
Kısıtlama olmayan antibiyotikler.
2.UH-P: Ayaktan tedavide uzman hekimlerce veya ilaç kullanım raporuna bağlı olarak
pratisyen hekimler dahil tüm hekimlerce, yatarak tedavide ise tüm hekimlerce reçete
edilebilir.
3.
4.
EHU*: Böbrek yetmezliği, kanser, HIV/AIDS enfeksiyonu, splenektomi olanlar ve
immünsupresif tedavi alanlara bu hastalıklar kurul raporunda belirtilmek kaydıyla.
EHU: (ENFEKSİYON HASTALIKLARI UZMANI): Bu antibiyotikler, enfeksiyon
hastalıkları uzmanının (EHU) yazabileceği, EHU’nın olmadığı yerlerde İç Hastalıkları
Uzmanının yazabileceği, Çocuk hastalarda, Çocuk Enfeksiyon Hastalıkları Uzmanı
olmadığı yerlerde Çocuk Hastalıkları Uzmanının yazabileceği antibiyotikler.
Acil durumlarda, (endikasyonları dahilinde kullanılmak kaydıyla) iç hastalıkları ve çocuk
hastalıkları uzmanları tedaviye başlayabilir, ancak takip eden ilk iş günü, bu uzmanlar tarafından
yazılan reçetenin EHU tarafından onaylanması zorunludur.
Hastane enfeksiyon komitesinin belirlediği kurallar ve/veya protokollere uygun olarak
enfeksiyon hastalıkları uzmanı aranmaksızın hastayı tedavi etmekte olan uzman hekim tarafından da
yazılabilecektir.
5.
EHU** :
Bu antibiyotikler, enfeksiyon hastalıkları uzmanının (EHU)
yazabileceği, EHU’nın olmadığı yerlerde iç hastalıkları uzmanının veya göğüs
hastalıkları uzmanının; çocuk hastalarda, çocuk enfeksiyon hastalıkları uzmanının
olmadığı yerlerde çocuk hastalıkları uzmanının yazabileceği antibiyotikler.”
6. A–72: Reçete edilme için EHU onayı gerekmeyen, ancak, aynı ilaç 72 saatten daha uzun süre
kullanılacak ise (en geç ilk 72 saat içinde ) EHU’nun onayının alınması gereken antibiyotikler.
Bu antibiyotikler için enfeksiyon hastalıkları uzmanının olmadığı yerlerde pnömoni,
bronşektazi, KOAH akut alevlenme ve invaziv pulmoner aspergillozis endikasyonları ile
ilgili olarak göğüs hastalıkları veya iç hastalıkları veya çocuk hastalıkları uzman
hekimlerinin onayı; bu endikasyonlar dışında kalan endikasyonlar için ise enfeksiyon
hastalıkları uzmanı olmayan yerlerde iç hastalıkları veya çocuk hastalıkları uzmanının
onayı yeterlidir
7. APAT: “AYAKTAN PARENTERAL ANTİBİYOTİK TEDAVİSİ”
Bu uygulama, hastanın ayaktan parenteral antibiyotik tedavisinin uygun olduğunu gösteren “APAT”
ibaresinin reçetede belirtilmesi ile işleme alınır.
A–72 kapsamındaki ilaçlardan biri kullanıldıktan sonra diğerleri EHU olmaksızın peş peşe
kullanılamaz.
APAT uygulamasına aşağıdaki durumlar girer:
a. Akut Bakteriyel menenjitte tek doz Seftriakson 2 gr. KY. Hasta, LP’nin yapılabileceği
merkeze ortalama 4 saatten daha uzak ise 2 gram seftriakson yapılabilir.
b. Hastanın enfeksiyonunun APAT’a uygun olduğunu belgeleyen EHU’ nun da içinde
bulunduğu bir sağlık kurulu raporu ile KY
8. Cerrahi proflakside kullanılmayacak antibiyotikler: 9–13, 24–35, 36–42, 52–59, 60,
60.1, 66, 66.1, 70, 71 (Bu antibiyotikler cerrahi proflaksi amacıyla ancak “Açıklama 5” şartları
dahilinde kullanılabilir)
NOT: Bu liste, ilaçların etken maddeleri dikkate alınarak düzenlenmiş olmakla birlikte Bedeli
Ödenecek İlaçlar Listesinde (EK-2/D) yer almayan herhangi bir ilacın ödenmesi mümkün değildir.
EK-2/B
SADECE YATAN HASTALARDA KULLANIMI HALİNDE BEDELLERİ
ÖDENECEK İLAÇLAR
1. Active protein-C (Madde 12.7.22’ye göre)
2. Amfoterisin-B formları, Kaspofungin ve Vorikanozol (parenteral formları) (Madde
12.7.23’e göre)
3. Antihuman lenfosit globulinler
4. Aztreonam, Vankomisin, İmipenem, Meropenem, Linezolid.
5. Sefodizim,
Sefoperazon,
Sefaperazon-Sulbaktam,
Sefotaksim,
Seftazidim,
Seftizoksim, Siprofloksasin Parenteral, Levfloksasin Parenteral, Ofloksasin Parenteral,
Moksifloksasin Parenteral, Teikoplanin (EHU APAT'TA KY), Gansiklovir (Kanser
Hastalarında, Tüberküloz Hastalarında, Bronşektazide, Pnömonide, Diyaliz tedavisi
gören ve Kronik Böbrek Hastalarında, Nefrotik Sendromda, Osteomiyelitte,
Tromboflebitte, Kistik Fibroziste, Antibiyotik kullanımı gerektiren immün bozukluğu
olan hastalarda, Kronik Karaciğer Hastalıklarında, Diyabetli Hastalarda, Bir aydan
küçük yenidoğan bebeklerdeki enfeksiyonlarda, orbital selülitte, yatarak tedavide
başlanan antibiyotiğin hastaneden çıkışta devamı gerektiğinde bu ilaçların antibiyotik
tablosunda belirtilen şartlarda ayaktan verilebilecektir.)
6. İrrigasyon solüsyonları
7. Amiodarone Ampul
8. Dopamin
9. Dobutamin
10. Droperidol ve Midazolam (klinik şartlarda yapılacak tetkik ve müdahaleler için gerekli
görüldüğü takdirde ayaktan tedavide de verilebilir)
11. Fenitoinler (ampul formları)
12. Human Albumin (Madde 12.7.13 esaslarına göre)
13. İnterlökinler
14. İntravenöz inhalasyon anestezikleri (kanser hastalarında rapora dayanılarak ayaktan
verilir)
15. Karbakol
16. Levosimendan (Madde 12.7.26 esaslarına göre)
17. Muromonap-CD3
18. Nitrogliserin paranteral
19. Nitroprussit
20. Nöromuskuler kavşak bloke edici ilaçlar
21. Paranteral antifungal
22. Paranteral beta-blokerler
23. Paranteral peptik ülser ilaçlarından proton pompa inhibitörleri ve H2 reseptör
antagonistleri
24. Servikal prostaglandinler
25. Surfaktanlar
26. Streptopal
27. Streptokinaz, ürokinaz, trofiban, plazminojen aktivatörleri (kardiyoloji, kalp damar
cerrahisi, dahiliye ve acil tıp uzmanları tarafından reçete edilebilir)
28. Tedavide Kullanılan Anestezik Antidotlar (Flumazenil, Opioid Antagonistler)
29. Traneksamik asit parenteral formları (hemofili hastasında ayaktan tedavide de ödenir)
30. Gözde kullanılan viskoelastikler
31. Terlipresin
32. Dekstemedetomidin
33. Aprotinin
34. Fondaparinux
35. Faktör VIIa (Madde 12.7.27-A’ya göre)
36. Rasburicase (Madde 12.7.4’e göre)
37. İntravenöz parasetamol
38. Fibrinojen ve kombinasyonları
39. L-Ornithin-L-Aspartat (İç hastalıkları veya Pediatri Uzmanları tarafından Sağlık
Bakanlığınca onaylanmış endikasyonlarında reçete edilir.
40. İntravenöz Anti Rh Preparatları (Ayaktan tedavide ITP endikasyonunda; Faktör ve
Diğer Kan Ürünlerinin Reçete Edilme İlkeleri başlıklı (12.7.27) maddenin, B) Anti
Rh Kullanım İlkeleri fıkrasının d alt bendinde yer alan “Idiopatik (İmmün)
Trombositopeni’de Kullanımı koşullarına göre)
41. Hemofiltrasyon ürünleri (yoğun bakımda akut böbrek yetmezliğinde )
NOT: Bu liste, ilaçların etken maddeleri dikkate alınarak düzenlenmiş olmakla birlikte Bedeli
Ödenecek İlaçlar Listesinde (EK–2/D) yer almayan herhangi bir ilacın ödenmesi mümkün
değildir.
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
EK-2/C
AYAKTAN TEDAVİDE SAĞLIK KURULU RAPORU
İLE VERİLEBİLECEK İLAÇLAR
İmmünsupresifler (TOPİKAL FORMLARI DAHİL)
Betanekol
Bifosfonatlar (Madde 12.7.17’ye göre)
Bosentan, Iloprost trometamol inhale formları (madde 12.7.30.’a göre)
Büyüme hormonları (Madde 12.7.6’ya göre)
Calcitriol, calcitonin, alfa calcitol
Clostridium botulinum toxini (Madde 12.7.5’e göre)
Corynebacterium parvum
Danazol
Desmopressin (Primer enurezis nokturna endikasyonunda uzman hekimce de reçete
edilebilir.)
Donepezil HCI (Nöroloji, geriatri, psikiyatri uzmanları tarafından reçete edilebilir.)
Edrofonyum
Eritropoietin, darbepoietin (Madde 12.7.9’a göre)
a)Ezetimib: Kardiyoloji, iç hastalıkları, kalp damar cerrahi veya nöroloji
uzmanının bulunduğu sağlık kurulu raporu ile statinlerle sonuç alınamayan veya
karaciğer toksisitesinin başladığı vakalarda, bu durumun sağlık kurulu raporunda
belirtilmesi ve kullanılan statin dozunun azaltılması koşuluyla kullanılabilir.
b) (Ezetimib+statin) kombinasyon tedavisi; Kardiyoloji, iç hastalıkları, kalp damar
cerrahi veya nöroloji uzmanının bulunduğu sağlık kurulu raporu ile tek başına
statinlerle sonuç alınamayan veya karaciğer toksisitesinin başladığı vakalarda, bu
durumun sağlık kurulu raporunda belirtilmesi ve kullanılan diğer statin ve ezetimibin
kesilmesi koşuluyla, günlük maksimum (01x01) dozla kullanılabilir. Ayrıca (EK-2/A)
14.
listesinin 147 inci maddesinde belirtilen şartlar bu kombinasyon için geçerlidir.
15. Faktör VII,VIII, IX, X (Madde 12.7.27-A’ya göre, Faktör VIIa hariç)
16. Fentanyl Transdermal TTS, Fentanyl sitratın oral ve pastil formları
17. Gabapentin, Pregabalin “(Nöroloji, nöroşirurji, pediatri, endokrinoloji ve
fizik
tedavi ve rehabilitasyon uzmanlarınca reçete edilebilir” şeklinde değiştirilmiştir.
18. Galantamine (Nöroloji, geriatri, psikiyatri uzmanları tarafından reçete edilebilir)
19. Gonadotropinler (FSH, LH,HCG, kombinasyonları) ve Gonadotropinleri etkileyen ilaçlar
(Ganireliks, Setroreliks)(infertilite ve tüp bebek tedavisinde 10.3.1 maddesindeki
hükümler geçerlidir) (çocuk cerrahisi uzmanı hekimlerce de reçete edilebilir)
20. Granisetron parenteral
21. Her türlü immün serum, hiperimmün gammaglobinler (hepatit B, kuduz ve tetanoz
immün serumları hariç)
22. Her türlü enteral ve parenteral beslenme ürünleri (Lipid, protein, aminoasit solüsyonları
gibi ; Madde 12.7.8’e göre)
23. İmmünglobulinler
24. İnterferonlar (Madde 12.7.13’e göre)
25. Koloni stimüle eden faktörler (Granülosit, Makrofaj, Filgrastim, Lenograstim, vb.)
26. Kontraseptifler (prospektüsündeki mevcut dismenore, endometriozis, over kistleri,
polikistik over ve hirsutismus endikasyonları dışında ödenmez)
27. Memantine (Nöroloji, geriatri, psikiyatri uzmanları tarafından reçete edilebilir)
28. Metil Fenidat Hcl içeren ilaçlar: hiperaktivite ve dikkat eksikliği tedavisinde, 18 yaş
altında, tedavi şemasını içeren, çocuk/erişkin psikiyatrisi uzmanının bulunduğu sağlık
kurulu raporuna dayanılarak, çocuk/erişkin psikiyatrisi, çocuk nörolojisi, nöroloji ve
çocuk hastalıkları uzmanlarınca yazılabilir
29. Ondansetron parenteral
30. Kanser kemoterapötikleri (Madde 12.7.14’e göre)
31.
32.
33.
34.
35.
36.
37.
38.
39.
40.
41.
42.
43.
44.
45.
46.
47.
48.
49.
50.
51.
52.
53.
54.
55.
56.
57.
58.
59.
60.
61.
62.
63.
64.
Parenteral Asiklovir
Parenteral Zidowudin
Periton ve hemodiyaliz solüsyonları
Raloxifen (Maddeler 12.7.14 ve 12.7.17’ye göre)
Rivastigmin (Nöroloji, geriatri, psikiyatri uzmanları tarafından reçete edilebilir)
Siproteron acetate (düşük doz kombine preparatlar hariç)
Somatostatin ve analogları
Paranteral Triptanlar (Madde 12.7.19’a göre)
Sülfosalazin ve mesalazin
Tropisetron parenteral
Vazopresin
Verteporfirin
Riluzol (Nöroloji, geriatri, psikiyatri uzmanları tarafından reçete edilebilir)
Altın Preparatları (Madde 12.7.1’de belirtilen uzmanların katıldığı ilaç raporu ile)
Etanersept (Madde 12.7.1’de belirtilen uzmanların katıldığı ilaç raporu ile)
İnfliksimab (Madde 12.7.1’de belirtilen uzmanların katıldığı ilaç raporu ile)
Adalimumab (Madde 12.7.1’de belirtilen uzmanların katıldığı ilaç raporu ile)
Leflunomid (Madde 12.7.1’de belirtilen uzmanların katıldığı ilaç raporu ile)
Alerji aşıları (Madde 12.7.3’de belirtilen uzmanların katıldığı ilaç raporu ile)
Botilismus Antitoksini Tip A (Madde 12.7.5’de belirtilen uzmanların katıldığı ilaç raporu
ile)
Sevelamer (Madde 12.7.9’de belirtilen uzmanların katıldığı ilaç raporu ile)
Copolymer (Madde 12.7.13’e göre)
Klopidogrel (Madde 12.7.15’e göre)
Metabolik hastalıklarda kullanılan mamalar (Madde 12.7.16’ya göre)
Palivizimab (Madde 12.7.20’ye göre)
Antitrombin III (Madde 12.7.27’ye göre)
Strontium Renelate (Madde 12.7.17’ye göre)
Özel amaçlı tıbbi mamalar (Madde 12.7.16’ya göre)
Vorikanazol oral (Madde 12.7.23’e göre)
Thalidomid (Madde 12.7.14’e göre)
Orlistat ve sibutramin (Madde 12.7.18’e göre)
Subkütan Metotreksat (Madde 12.7.1’e göre)
Anagrelid ( Madde 12.7.21’e göre)
Apretitant (Yüksek doz cisplatin 50mg/m2 ve üzeri) kemoterapi rejimleri ile gelişen ya da
kök hücre destekli yüksek doz kemoterapi uygulamaları sonrası gelişen emezisin
önlenmesinde, bu durumların sağlık kurulu raporuyla belirtilmesi halinde ödenir.
NOT: Bu liste, ilaçların etken maddeleri dikkate alınarak düzenlenmiş olmakla birlikte Bedeli
Ödenecek İlaçlar Listesinde (EK-2/D) yer almayan herhangi bir ilacın ödenmesi mümkün değildir.